Secuestro pulmonar intralobar como causa de neumonías recurrentes en una mujer adulta: reporte de caso.
Intralobar pulmonary
sequestration as a cause of recurrent pneumonias in an adult woman: a case
report.
Autores:
Luz M. Moyano Vidal 1,2; Ricardo Taipe-Mallqui 3,4,a; Roly Gonzaga-Vílchez 1,5,; Narcisa Reto Otero 6,b; Raquel Herrer-Ticse 6,c
1. Escuela Profesional de Medicina Humana, Facultad de Ciencias de la Salud. Universidad Nacional de Tumbes. Tumbes, Perú.
2. Unidad Médico Legal I Contralmirante Villar. Instituto de Medicina Legal y Ciencias Forenses. Tumbes, Perú.
3. Consejo Regional III Lima. Lima, Perú.
4. Servicio de Cirugía de Tórax. Hospital Guillermo Almenara Irigoyen, nivel IV. EsSalud. Lima, Perú.
5. Sociedad Científica de Estudiantes de Medicina. Escuela Profesional de Medicina Humana. Universidad Nacional de Tumbes. Tumbes, Perú.
6. Servicio de Medicina. Hospital Carlos Cortez Jiménez. EsSalud. Tumbes, Perú.
a. Médico Especialista en Cirugía Torácica y Cardiovascular.
b. Médica Especialista en Neurología.
c. Médico Especialista en Medicina Interna
*Grupo de Investigación de Enfermedades Negligentes en Regiones Tropicales (INERTROP).
ORCID:
Luz M. Moyano Vidal ORCID: 0000-0002-5878-5782
Ricardo Taipe-Mallqui ORCID: 0000-0002-5989-493X
Roly Gonzaga-Vílchez ORCID: 0000-0001-7504-4583
Narcisa Reto Otero ORCID: 0000-0002-8107-1657
Raquel Herrer-Ticse ORCID: 0000-0002-8103-7141
Autor corresponsal
Roly Pablo Gonzaga Vilchez
Correo: 190167221@untumbes.edu.pe
Teléfono: +51 940 962 809
Fuentes de financiamiento: Autofinanciado
Conflicto de interés: Los autores declaran no tener conflictos de interés.
Agradecimientos: LMMV quiere agradecer a todos los médicos cardiotorácicos del HNGAM por su ayuda y colaboración en la elaboración de este reporte de casos.
Declaración de uso de IA. Durante la realización de este trabajo, Luz M.Moyano (n) utilizó [Chat Gpt 4.0, Open evidence, Medsearch, Scopus IA] para [Integrar los datos de la historia clínica, para reducir redundancia de palabras, mejorar ortografía y mejorar claridad de párrafos.; así como búsqueda de evidencia científica real actual del tema, armar la discusión y para confirmar referencias]. Después de usar esta herramienta/servicio/tecnología, los autores revisaron y editaron el contenido según fuese necesario y asumen toda la responsabilidad por el contenido de la publicación.(24)
Contribución de los autores.
Redacción del borrador original: LMMV, RTM, RGV; Redacción, revisión y edición: LMMV, RTM, NRO, RHT; Supervisión: LMMV, RTM;Aprobación final del manuscrito: todos los autores.
RESUMEN.
Introducción: El secuestro pulmonar intralobar (SPI) es una malformación congénita infrecuente en adultos, caracterizada por parénquima pulmonar no funcional irrigado por una arteria sistémica aberrante. Su presentación clínica puede simular neumonías recurrentes o masas pulmonares sospechosas de neoplasia, dificultando el diagnóstico oportuno. Reporte de caso: Presentamos el caso de una mujer de 49 años con antecedentes de asma y resistencia a la insulina, que desde 2018 experimentó episodios recurrentes de neumonía en el lóbulo inferior derecho. En diciembre de 2023, durante el episodio más severo, una tomografía inicial sugirió una posible neoplasia pulmonar; sin embargo, una segunda interpretación identificó una pseudomasa basal con una arteria sistémica aberrante compatible con secuestro pulmonar. Estudios en hospitales de referencia confirmaron irrigación anómala desde la aorta torácica. En mayo de 2024 se realizó una lobectomía inferior derecha mediante toracotomía, identificándose la arteria aberrante intraparenquimal. La anatomía patológica confirmó SPI complicado con fibrosis, bronquiectasias e inflamación crónica. Conclusión: el SPI debe considerarse en adultos con neumonías recurrentes y lesiones pulmonares basales. La correlación entre clínica e imagenología, especialmente la identificación de la arteria aberrante es fundamental para establecer el diagnóstico y definir el tratamiento adecuado.
Palabras clave: Secuestro pulmonar; Neumonía recurrente; Informes de casos. (Fuente: DeCS-BIREME)
ABSTRACT.
Introduction: Intralobar pulmonary sequestration (IPS) is an uncommon congenital malformation in adults, characterized by non-functioning lung tissue supplied by an aberrant systemic artery. Its clinical and radiologic presentation may mimic recurrent pneumonias or pulmonary neoplasms, leading to diagnostic delays. Case of report: We report the case of a 49-year-old woman with a history of asthma and insulin resistance, who had recurrent right lower lobe pneumonias since 2018. In December 2023, during the most severe episode, initial chest CT suggested a possible pulmonary neoplasm; however, a second radiologic interpretation identified a basal pseudomass with an aberrant systemic artery consistent with pulmonary sequestration. Further imaging at referral centers confirmed anomalous arterial supply from the thoracic aorta. In May 2024, a right lower lobectomy was performed via thoracotomy, revealing an intraparenchymal aberrant artery. Pathology confirmed complicated IPS with fibrosis, bronchiectasis, and chronic inflammation. Conclusion: IPS should be considered in adults presenting with recurrent pneumonias and basal lung lesions. Clinical–radiologic correlation, particularly the identification of an aberrant systemic artery, is essential for establishing the correct diagnosis and guiding definitive treatment.
Keywords: Pulmonary sequestration; Pneumonia, Recurrent; Case Reports. (Source: DeCS-BIREME)
INTRODUCCIÓN
El secuestro pulmonar es una malformación congénita poco frecuente, responsable del 1–6% de las anomalías pulmonares reportadas(1) . Se caracteriza por la presencia de parénquima pulmonar no funcional, sin comunicación con el árbol bronquial y con irrigación proveniente de una arteria sistémica aberrante(2,3). Existen dos variantes: el secuestro pulmonar intralobar (SPI), la forma más común, que comparte pleura visceral con el pulmón normal, y el secuestro extralobar (SPE), separado completamente del parénquima pulmonar y diagnosticado con mayor frecuencia en la infancia(4,5). El SPI puede manifestarse en la adultez, generalmente con neumonías recurrentes, hemoptisis o masas basales que simulan neoplasias, lo que genera una alta tasa de error diagnóstico preoperatorio, reportada por encima del 50% (6). La similitud radiológica con tumores pulmonares, bronquiectasias complejas o procesos infecciosos crónicos explica parte de esta confusión diagnóstica. Incluso se han descrito casos con elevación de marcadores tumorales como CEA y NSE (7,8), lo cual puede reforzar la sospecha equivocada de malignidad.
El diagnóstico se basa en la tomografía computarizada contrastada con reconstrucción vascular, que permite identificar la arteria sistémica aberrante, hallazgo patognomónico del secuestro pulmonar (1,9,10). La confirmación suele complementarse con estudios angiográficos o con hallazgos quirúrgicos. El tratamiento de elección es la resección quirúrgica mediante lobectomía, abierta o asistida por video, que ofrece buenos resultados y baja tasa de complicaciones (11,12).
En este reporte describe el caso de una mujer adulta con SPI inicialmente interpretado como neoplasia pulmonar, destacando los desafíos diagnósticos y la importancia de la correlación clínica e imagenológica para evitar errores y orientar un manejo adecuado.
PRESENTACIÓN DEL CASO.
Mujer de 49 años, médica legista y docente universitaria, con antecedentes de asma bronquial desde los 24 años, resistencia a la insulina, obesidad tipo II y exposición ambiental crónica a plaguicidas por residencia cercana a zonas agrícolas en Tumbes. Desde 2018 presentó episodios recurrentes de neumonía en el lóbulo inferior derecho, caracterizados por fiebre alta, tos seca y dolor costal derecho.
Primer episodio (agosto 2018). Cursó con fiebre de 39.5 °C sin síntomas respiratorios mayores. La radiografía de tórax mostró una imagen compatible con “neumonía redonda atípica”. Fue tratada ambulatoriamente con azitromicina y acetaminofén, con resolución clínica temprana.
Segundo episodio (junio 2020). En contexto de pandemia por COVID-19, presentó fiebre de 40 °C, tos seca y malestar general. La tomografía computarizada sin contraste reveló bronquiectasias dilatadas e infectadas en el lóbulo inferior derecho. Fue manejada con ceftriaxona EV, metamizol y paracetamol, con mejoría progresiva.
Tercer episodio (diciembre 2023). Fiebre de 40 °C, hiporexia y tos persistente motivaron hospitalización por 15 días en EsSalud. Exámenes mostraron leucocitosis de 19 000/mm³ con linfocitosis. Se administró ceftriaxona EV, sin respuesta clínica, añadiéndose luego clindamicina. La tomografía computarizada contrastada inicial reportó un nódulo pulmonar espiculada sugestivo de neoplasia. Una segunda lectura en un centro privado describió una pseudomasa basal medial derecha con bronquiectasias y una arteria aberrante dependiente de la aorta torácica, compatible con secuestro pulmonar intralobar ( ver Figura 3 suplementaria).
Estudios complementarios. Tomografías adicionales realizadas en hospitales de referencia nacional (enero–mayo 2024) confirmaron un área focal seudonodular en el lóbulo inferior derecho, asociada a un vaso sistémico aberrante proveniente de la aorta torácica (ver figuras 1A,1B,1C).
Intervención quirúrgica (mayo 2024). La paciente ingresó al Servicio de Cirugía de Tórax del Hospital Nacional Guillermo Almenara Irigoyen para manejo definitivo. Se realizó una lobectomía inferior derecha por toracotomía axilar vertical, accediendo por el quinto espacio intercostal. Se identificó una arteria sistémica aberrante intraparenquimal con ramas originadas en el seno cardiofrénico derecho (ver figura 2 a*). Se ligaron la vena pulmonar inferior, la arteria del lóbulo inferior y el bronquio lobar, extrayéndose la pieza quirúrgica sin complicaciones intraoperatorias.
Estudio anatomopatológico. La pieza mostró pleura congestiva, parénquima antracótico con bronquiectasias, fibrosis intersticial severa, inflamación crónica moderada, atelectasia y calcificación distrófica psamomatosa. Los hallazgos fueron consistentes con secuestro pulmonar intralobar complicado (ver Figura 2a ).
Evolución posoperatoria. La evolución clínica fue favorable, sin complicaciones respiratorias, reintegrándose a sus actividades habituales tras el periodo de recuperación (ver Figuras suplementarias) .
Figuras 1. Estudios complementarios
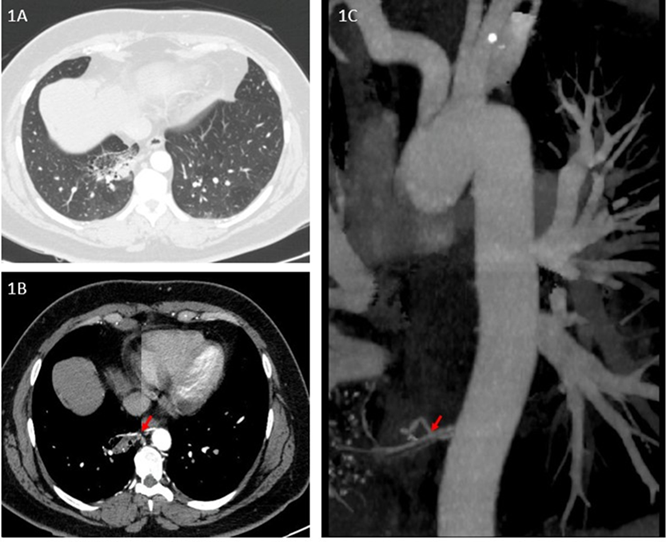
Figura 1ª. Angiotomografía de tórax muestra parénquima pulmonar del lóbulo inferior derecho con bronquiectasias quísticas. 1B. Ventana mediastinal muestra flecha roja señala arteria anómala que nutre secuestro pulmonar. 1C. En reconstrucción de aorta torácica y sus ramas, flecha roja marca el origen de la arteria anómala en la aorta torácica que confirma secuestro pulmonar.
Figuras 2. Intervención quirúrgica y hallazgo anatomopatológico.
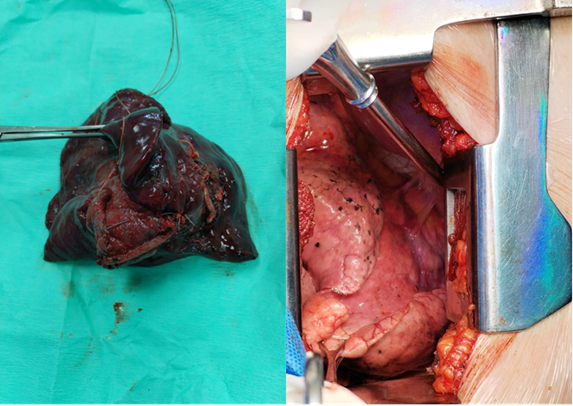
Figura 2ª. Pieza quirurgica resecada, donde se evidencia cambio en la coloración del lóbulo inferior derecho y fibrosis del parenquima. 2 a* arterias aberrantes visualizadas procedente de la arteria aortica pulmonar.
DISCUSIÓN.
El secuestro pulmonar (SP) presenta una tasa de prevalencia que oscila entre el 1 y 6% de todas las malformaciones pulmonares congénitas, y es la segunda más común diagnosticada (1); su tasa de incidencia de 1 por cada 5000 nacimientos entre todas las patologías pulmonares (13) ,variando entre 0.15-6.4% en diferentes reportes de caso (14,15); pero su tasa de incidencia es de 3.4% en casos de pacientes pediátricos con hernia diafragmática congénita (16).
Nuestro caso es un SPI cuyo estudio tomográfico en diciembre del 2023 en EsSalud describió la presencia de una masa basal espiculada , con sospecha de neoplasia pulmonar, sin mención de estructuras vasculares anómalas (1); y sin considerar los antecedentes clínicos del paciente, lo que limitó seriamente la capacidad diagnóstica del radiólogo de la primera lectura (Essalud) conduciéndolo a un diagnóstico erróneo. En contraste con el informe radiológico del centro de imágenes oncológicas que integro la información clínica complementaria, identificando la arteria aberrante hallazgo patognomónico de SIP.
Este suceso pone en evidencia una problemática existente en cuanto al diagnóstico de esta malformación congénita pulmonar, siendo malinterpretada como una neoplasia, específicamente en adultos, por aspectos como: a) su morfología en imágenes (anatomías vasculares anómalas múltiples y distribución atípica, lo que aumenta la complejidad diagnóstica) (11,12), b) localización pleural y c) comportamiento hipercaptantes en estudios PET/CT que imitan tumores, infecciones granulomatosas o bronquiectasias crónicas (2,3).
En una serie retrospectiva de 2625 casos, se reportó una tasa de preoperatorio incorrecto del 58.6%, identificacion como un quiste pulmonar (36.19%) e identificación como neoplasia (21.04%) (17). Se han reportado casos de SIL con marcadores tumorales elevados, como el antígeno carcinoembrionario (CEA) o enolasa neuronal específica (NSE), lo que remarca la dificultad diagnóstica(7,8). El hallazgo de infección o hemotorax puede intensificar la similitud con patologías malignas (18). Para reducir la tasa de desaciertos una evaluación multidisciplinaria que incluya estudios de imagen y un análisis clínico-radiológico integral sería lo más recomendable, los médicos radiologos de la seguridad social y de las clínicas privadas tienen acceso a poder leer el historial de los pacientes .
El SIP es más frecuente en pacientes pediátricos y adolescentes(19) a diferencia de nuestro caso que se presenta pasado los 40 años, por lo que en un paciente adulto con neumonía a repetición se debe considerar en el diagnostico diferencial. A diferencia del extralobar, el SIP puede drenar al árbol bronquial y a las venas pulmonares, permitiendo cierta ventilación y perfusión funcional y esto hace que el pulmón comprometido no genere síntomas por décadas(20) . Por otro lado, en el 60 a 70% de casos se localiza en lóbulo inferior izquierdo; sin embargo, en nuestro caso se localiza en el lóbulo inferior derecho por lo que se hace más difícil el diagnostico ya que el lóbulo inferior derecho es más difícil de distinguir en una radiografía simple de tórax por la presencia de la silueta cardiaca (21).
En Perú un reporte realizado por Nuñez-Paucar et al en el Instituto nacional del niño, de los 70 casos reportado de malformaciones congénitas pulmonares el (9/70) 12% fueron SPE y (7/70) 10% SPI en una población infantil oscilante entre de 0.5 a 168 meses de edad. El 87% de las malformaciones requirió una lobectomía , sin muertes asociadas, siendo la neumonía la complicación posoperatoria más frecuente en niños (22).
La lobectomía es la técnica y la solución quirurgica más frecuente para el Secuestro pulmonar; la toracotomía convencional, así como la cirugía toracoscopia videoasistida (VATS), tienen baja tasa de complicaciones y recuperación rápida especialmente en los casos de SPI (4,5,11). Estas intervenciones quirúrgicas evitan continuidad de síntomas, las complicaciones infecciosas y la transformación maligna, muy rara estos casos (23). En algunos casos puede ser valorado la posibilidad de segmentectomía o resección en cuña , pero la lobectomía sigue siendo la opción más segura (12).
Conclusiones.
La integración de la historia clínica en la interpretación radiológica es esencial para el diagnóstico correcto de entidades raras. El hallazgo de una arteria sistémica aberrante en estudios contrastados debe alertar sobre la posibilidad de secuestro pulmonar. La resección quirúrgica es curativa y debe ser considerada en pacientes sintomáticos con infecciones recurrentes.
REFERENCIAS BIBLIOGRÁFICAS
1. Rastegar N, Maldjian PD. Bronchopulmonary Sequestration: Spectrum of Appearance on CT. Contemp Diagn Radiol. 15 de febrero de 2019;42(4):1.
2. Galanis M, Sommer E, Gioutsos K, Nguyen TL, Dorn P. Pulmonary Sequestration: A Monocentric Case Series Report. J Clin Med. enero de 2024;13(19):5784.
3. Song JY, Park SG, Lee HY, Kim SR, Kim HG, Shin SH, et al. Comparison of clinical outcomes of pulmonary sequestration in adults between surgery and non-surgery groups. J Thorac Dis. octubre de 2022;14(10):3876-85.
4. Wu Y, Ye Z, He Z, He X, Hong X, Chen F, et al. Video-assisted thoracoscopic surgery lobectomy for giant intralobar pulmonary sequestration: A case report. Medicine (Baltimore). 22 de julio de 2022;101(29):e29284.
5. Grossi W, Londero F, Vit A, De Franceschi E, Masullo G, Sponza M, et al. Hybrid minimally invasive treatment of intralobar pulmonary sequestration: a single-centre experience. Interact Cardiovasc Thorac Surg. 18 de enero de 2022;34(2):255-7.
6. He B, Sun MS, Niu Y, Zhang JB, Nie QQ, Zheng X, et al. Hybrid and Endovascular Treatment of Pulmonary Sequestration: Two Case Reports and Literature Review. Ann Vasc Surg. noviembre de 2020;69:447.e1-447.e8.
7. Kong FW, Wang WM, Gong L, Wu W, Zhang M. Extralobar pulmonary sequestration with elevated serum neuron-specific enolase. Medicine (Baltimore). 2 de octubre de 2020;99(40):e22574.
8. Luo W, Hu T chen, Luo L, Li Y lun. Pulmonary sequestration with Aspergillus infection presenting as massive hemoptysis and hemothorax with highly elevated carcinoembryonic antigen in pleural effusion that mimics advanced lung malignancy. Eur J Med Res. 25 de mayo de 2021;26:48.
9. Xu G, Zhou J, Zeng S, Zhang M, Ouyang Z, Zhao Y, et al. Prenatal diagnosis of fetal intraabdominal extralobar pulmonary sequestration: a 12-year 3-center experience in China. Sci Rep. 30 de enero de 2019;9(1):943.
10. Pauels L, De Waele M, Medart L, Debruche M. Two unusual variants of pulmonary intra-lobar sequestration. Interact Cardiovasc Thorac Surg. 21 de julio de 2022;35(2):ivac189.
11. Wan IYP, Lee TW, Sihoe ADL, Ng CSH, Yim APC. Video-assisted thoracic surgery lobectomy for pulmonary sequestration. Ann Thorac Surg. febrero de 2002;73(2):639-40.
12. Lin TH, Huang WL, Chang CC, Yen YT, Lai WW, Tseng YL, et al. Uniportal video-assisted thoracoscopic surgery lobectomy and segmentectomy for pulmonary sequestration. J Thorac Dis. junio de 2018;10(6):3722-8.
13. Pérez-Wulff J, Márquez C D, Lugo L C, Ayala H V, Robles T S, Di Muro J, et al. Fotocoagulación láser guiada por ultrasonido para el tratamiento del secuestro broncopulmonar fetal. Reporte de dos casos exitosos en Venezuela. Rev Obstet Ginecol Venezuela. junio de 2024;84(2):205-11.
14. Mahmood H, Plumb A, Vega R, Windsor A. Incidental finding - the discovery of a bronchopulmonary foregut malformation through investigations for Crohn’s disease. J Radiol Case Rep. 29 de abril de 2017;11(4):10-9.
15. Khen-Dunlop N, Farmakis K, Berteloot L, Gobbo F, Stirnemann J, De Blic J, et al. Bronchopulmonary sequestrations in a paediatric centre: ongoing practices and debated management. Eur J Cardiothorac Surg. 1 de agosto de 2018;54(2):246-51.
16. Coughlin MA, Gupta VS, Ebanks AH, Harting MT, Lally KP, Congenital Diaphragmatic Hernia Study Group. Incidence and outcomes of patients with congenital diaphragmatic hernia and pulmonary sequestration. J Pediatr Surg. junio de 2021;56(6):1126-9.
17. Wei Y, Li F. Pulmonary sequestration: a retrospective analysis of 2625 cases in China. Eur J Cardio-Thorac Surg Off J Eur Assoc Cardio-Thorac Surg. julio de 2011;40(1):e39-42.
18. Sippel JM, Ravichandran PS, Antonovic R, Holden WE. Extralobar pulmonary sequestration presenting as a mediastinal malignancy. Ann Thorac Surg. abril de 1997;63(4):1169-71.
19. González L R, Riquelme U A, Arancibia Z H, Reyes M, Spencer L., Alarcón O, et al. SECUESTRO PULMONAR: CARACTERIZACIÓN Y TRATAMIENTO EN PACIENTES ADULTOS Y PEDIÁTRICOS. Rev Cir [Internet]. 27 de mayo de 2021 [citado 6 de junio de 2025];73(3). Disponible en: https://revistacirugia.cl/index.php/revistacirugia/article/view/831
20. Flye MW, Conley M, Silver D. Spectrum of pulmonary sequestration. Ann Thorac Surg. noviembre de 1976;22(5):478-82.
21. O’Brien M, Ireland ME, Hollings N, Elzain O. A Case of an Uncommon Cause of Pulmonary Abscess: Intralobar Bronchopulmonary Sequestration. J Chest Surg. 5 de mayo de 2025;58(3):114-7.
22. Nuñez-Paucar H, Atamari-Anahui N, Valera-Moreno C. Congenital pulmonary malformations in children in a pediatric hospital in Peru, 2010-2020. Bol Méd Hosp Infant México. 5 de septiembre de 2023;80(4):235-41.
23. Gompelmann D, Eberhardt R, Heussel CP, Hoffmann H, Dienemann H, Schuhmann M, et al. Lung sequestration: a rare cause for pulmonary symptoms in adulthood. Respir Int Rev Thorac Dis. 2011;82(5):445-50.
24. Leal JA, Gutiérrez Zúñiga D, Renza S, Valbuena F. Validación y adaptación cultural al español de la Rúbrica de retroalimentación del desempeño quirúrgico (SPR). Educ Médica. 1 de julio de 2025;26(4):101022.