RICSA, 3(1),37-46. (2026)
Fisiología
del eje hipotálamo-hipófisis-ovario en la
regulación del ciclo menstrual de mujeres en etapa
perimenopáusica
Physiology of the hypothalamic-pituitary-ovarian axis in
the regulation of the menstrual cycle in perimenopausal women
Brisayda Torrealva
Lázaro1,a, Ariana Silva Carranza1,a, Nayely
Soto Aguilar1,a, Jheremy
Teodoro Maza1,a ; Oscar Lenin
López Amaya1,b
Filiación:
1. Escuela profesional de Medicina Humana,
Universidad Nacional del Santa, Nuevo Chimbote, Perú.
a. Estudiante de medicina
b. Profesor.
Correspondencia: Lenin Amaya L., olopeza@uns.edu.pe
ID ORCID
de los autores
Silva
Carranza Ariana Valeria htttp://orcid.org/0009-0005-5691-7883 Soto Aguilar Nayely Xiomara htttp://orcid.org/0009-0009-4844-5846 Teodoro Maza Jheremy Jherly htttp://orcid.org/0009-0006-8854-9429 Torrealva Lázaro Brisayda
Mabet htttp://orcid.org/0009-0006-4800-6104 Oscar Lenin López Amaya htttp://orcid.org/0000-0002-4200-5120
Declaración de autoría: Los
autores declaran que participaron en conceptualización, Metodología, Software, Investigación, Curación de datos,
Redacción-Borrador Original, Redacción-Revisión y edición.
Declaración de conflicto de interés: Los autores
declaran no tener conflictos de interés financieros, personales o
institucionales que puedan influir en los resultados o interpretación del
estudio.
Financiamiento: El presente estudio
fue financiado con recursos propios
del autor y no contó
con financiamiento externo de
instituciones públicas o privadas.
Recibido: 05-12-2025.
Aceptado: 15-02-2026.
Publicado: 31-03-2026.
Esta obra
está publicada bajo la licencia
CC BY 4.0
DOI:
https://doi.org/10.57188/ricsa.2026.006
RESUMEN
Se describe la fisiologí´a del eje
hipota´lamo-hipo´fisis-ovario (HHO), su regulacio´n neuroendocrina y su papel
en la variabilidad del ciclo menstrual durante la perimenopausia. Se realizo´ una revisio´n narrativa
centrada en la secrecio´n
pulsa´til de GnRH, la respuesta hipofisaria de FSH y LH, la esteroidoge´nesis
ova´rica y los cambios asociados al
envejecimiento ova´rico. La perimenopausia se caracteriza por una alteracio´n
progresiva de la retroalimentacio´n negativa, con disminucio´n
de inhibina B y hormona antimülleriana, fluctuaciones de estradiol y elevacio´n irregular de FSH, lo que
favorece ciclos anovulatorios e irregularidad menstrual. Asimismo, la variabilidad hormonal impacta el sistema nervioso
central, modulando neurotransmisores, termorregulacio´n y metabolismo cerebral. Comprender estos
mecanismos permite explicar los sí´ntomas neuroendocrinos y orientar
estrategias clí´nicas basadas
en educacio´n hormonal,
manejo individualizado y vigilancia metabo´lica.
Palabras clave: Perimenopausia; eje
hipota´lamo-hipo´fisis-ovario; gonadotropinas; estradiol; fisiologí´a reproductiva. (Fuente: DeCS-BIREME)
ABSTRACT
This
review describes the physiology of the hypothalamic–pituitary–ovarian (HPO)
axis, its neuroendocrine regulation,
and its role in menstrual cycle variability during the perimenopausal
transition. A narrative review was conducted focusing on pulsatile GnRH
secretion, pituitary responses of FSH and LH, ovarian steroidogenesis, and age-related ovarian changes. Perimenopause is characterized by progressive disruption of negative feedback
mechanisms, with decreased inhibin B and anti-Müllerian hormone levels, marked estradiol fluctuations, and irregular
elevations of FSH, leading to anovulatory cycles and menstrual irregularity. Hormonal variability also affects the central
nervous system, modulating neurotransmitters, thermoregulation, and cerebral
metabolism. Understanding
these mechanisms helps
explain neuroendocrine symptoms and supports clinical strategies based on hormonal education, individualized
management, and metabolic monitoring.
Keywords: Type 2 Diabetes Mellitus (DM II); Obesity; HCV; HBV;
HIV; Hepatic Steatosis; Gender. (Source: DeCS-BIREME)
INTRODUCCIÓN
La
fisiología reproductiva femenina está determinada
por la acción coordinada del eje hipotálamo-hipófisis-ovario
(HHO), el cual regula de manera
precisa la maduración folicular, la ovulación
y la preparación endometrial para una eventual
gestación. Este eje integra señales neuroendocrinas
y moleculares, sustentadas en la liberación
pulsátil de GnRH, la secreción de LH y FSH,
y la síntesis de esteroides ováricos como el
estradiol y la progesterona, lo que asegura la continuidad del ciclo menstrual en la mujer sana (1).
La
perimenopausia constituye una etapa de transición
dentro de la vida reproductiva, caracterizada
por la progresiva variabilidad de los ciclos
menstruales. Este periodo abarca desde el inicio
de la irregularidad menstrual hasta un año después
de la última menstruación (FMP) y suele dividirse
en dos fases: una temprana, con ciclos relativamente regulares, y una tardía,
marcada por períodos
prolongados de amenorrea hasta llegar al FMP (2). Su duración
es variable, oscilando entre 1 y 5 años,
y culmina en la menopausia, definida tras 12 meses de ausencia menstrual (3).
Durante
la perimenopausia, los cambios hormonales
no siguen una trayectoria lineal. En lugar
de un descenso constante, los niveles de estradiol y progesterona presentan
fluctuaciones y picos, mientras que la secreción
de cortisol refleja
la
interacción del eje HHO con el eje hipotálamo-
hipófisis-adrenal (4). Estas variaciones endocrinas se acompañan de un incremento progresivo de las gonadotropinas, en especial de la FSH, considerada un marcador clave de la transición reproductiva. La LH y la FSH no solo
actúan en el ovario, sino también en
tejidos extragonadales como hueso, hígado,
vasos sanguíneos y cerebro, lo que amplía su
impacto en la fisiología femenina más allá de la fertilidad (5).
En
este contexto, la regulación del ciclo menstrual en la mujer perimenopáusica no puede entenderse como una simple pérdida de hormonas sexuales, sino como un proceso complejo de retroalimentaciones dinámicas. La
evidencia longitudinal demuestra que
la perimenopausia implica una
sucesión de oscilaciones hormonales que
reflejan la disminución gradual de la reserva
ovárica y la adaptación del eje HHO (6).
El
estudio fisiológico de esta etapa en mujeres
sanas ofrece una perspectiva única para
comprender los mecanismos que sostienen la homeostasis reproductiva, integrando la neurofisiología, la endocrinología y los procesos moleculares que caracterizan la transición hacia el fin de la vida fértil.
Además, su análisis
reviste gran importancia clínica y científica, ya que
permite entender mejor la base fisiológica
en
los cambios de
la transición reproductiva y comprender estos
mecanismos permite avanzar
en el manejo integral de la salud femenina durante esta etapa de transición.
El
presente artículo tiene como objetivo fundamentar
la fisiología del eje hipotálamo- hipófisis-ovario
en la regulación del ciclo menstrual
de mujeres en etapa perimenopáusica, integrando
los niveles neuroendocrinos, celular y molecular,
con el fin de comprender los mecanismos
de control reproductivo durante esta etapa
de transición.
El
estudio de la fisiologí´a del eje HHO durante la perimenopausia resulta
esencial para comprender los mecanismos que regulan el ciclo
menstrual en mujeres sanas en una
etapa de transicio´n reproductiva
(2,3,6). Lejos de reducirse a una simple “pe´rdida
hormonal”, este proceso
refleja la capacidad de adaptacio´n neuroendocrina
del organismo femenino, en el que los pulsos de GnRH, la secrecio´n de FSH y LH y la produccio´n
de estro´genos y progesterona
experimentan fluctuaciones
significativas que impactan tanto en la
dina´mica del ciclo menstrual como en la interaccio´n
con otros ejes hormonales, como el hipota´lamo-hipo´fisis-adrenal (1,4).
Desde una perspectiva acade´mica y cientí´fica, esta revisio´n
bibliogra´fica aporta una visio´n integral de los cambios fisiolo´gicos de la
perimenopausia, integrando niveles
celulares, moleculares y neuroendocrinos (1, 5). Ello contribuye a fortalecer la formacio´n me´dica, diferenciar
procesos fisiolo´gicos normales de
alteraciones clí´nicas y generar un
marco de referencia actualizado que sustente
una pra´ctica profesional ma´s precisa y fundamentada.
En
el plano social y cultural, este estudio es igualmente
relevante, ya que la perimenopausia suele
estar rodeada de tabu´es y prejuicios que la
asocian con deterioro o pe´rdida de feminidad (7). Reconocerla como un proceso fisiolo´gico
de transicio´n, y no como un
trastorno, permite resignificar esta
etapa de la vida femenina, promover
una educacio´n sanitaria adecuada y mejorar la calidad de vida de las mujeres
mediante un enfoque
preventivo, empa´tico e integral.
En
conjunto, la comprensio´n y divulgacio´n de los procesos fisiolo´gicos de la perimenopausia no solo fundamenta la importancia biome´dica
de este eje,
sino
que tambie´n ofrece herramientas para una atencio´n
clí´nica y social ma´s justa, respetuosa y humanizada
(2,6).
La
regulacio´n del ciclo menstrual depende del eje HHO, que coordina
la secrecio´n pulsa´til
de GnRH y la liberacio´n de
FSH y LH, responsables del crecimiento folicular
y la produccio´n de estradiol
y progesterona (1). Con la edad disminuye
la reserva folicular y se altera la sensibilidad del
eje, generando fallas en la retroalimentacio´n hormonal y cambios propios de la perimenopausia
(8).
El
envejecimiento ova´rico es variable entre mujeres
y esta´ influido por factores gene´ticos, metabo´licos
y ambientales (3). A nivel celular, el estre´s
oxidativo y el deterioro mitocondrial reducen
la produccio´n hormonal y modifican la dina´mica
del ciclo menstrual (8,4), explicando la diversidad
en la aparicio´n de sí´ntomas vasomotores
y emocionales.
Durante
la perimenopausia son frecuentes los ciclos
anovulatorios y las variaciones en su duracio´n.
Ciclos mayores de 40 dí´as son un marcador clave de la transicio´n menopa´usica
(8). El sistema STRAW+10
ayuda a clasificar con precisio´n estas etapas (9).
Las
fluctuaciones de estradiol afectan neurotransmisores
como serotonina, dopamina y GABA,
influyendo en suen˜o, memoria, termorregulacio´n
y estado de a´nimo (3). La disminucio´n
estroge´nica aumenta el estre´s oxidativo
y favorece sí´ntomas cognitivos y emocionales (3,6).
La
secrecio´n hormonal se vuelve altamente variable
debido al agotamiento folicular, lo que altera la estabilidad del eje HHO (6). Factores
como IMC, tabaquismo, etnicidad y estilo de vida tambie´n modulan sí´ntomas metabo´licos,
vasomotores y psicolo´gicos (10). Los
sofocos se relacionan con cambios en el centro termorregulador mediado
por neuronas KNDy.
Finalmente,
la menopausia marca el cese de la funcio´n
ova´rica, con caí´da de estradiol e inhibinas y aumento sostenido de FSH y LH por pe´rdida
de retroalimentacio´n negativa (11),
lo que explica sí´ntomas persistentes
como sofocos, cambios genitourinarios
y alteraciones o´seas.
Fisiología normal del eje HHO
El
eje HHO constituye una unidad funcional integrada
que depende de interacciones anato´micas y fisiolo´gicas precisas.
El hipota´lamo, localizado en la base del cerebro,
contiene neuronas especializadas que sintetizan la hormona liberadora de gonadotropinas (GnRH), un decape´ptido cuya liberacio´n pulsa´til
determina el funcionamiento correcto del eje reproductor. Estas
neuronas se agrupan principalmente en los nu´cleos arcuato y preo´ptico, desde
donde proyectan sus axones hacia la
eminencia media. Dado que no existe
una conexio´n nerviosa directa con la hipo´fisis
anterior, la comunicacio´n se realiza a trave´s
del sistema porta hipota´lamo-hipofisario, una
red de capilares que transporta la GnRH hacia
la adenohipo´fisis (1). La GnRH posee una vida media muy corta (2–4 minutos), por lo que su secrecio´n
pulsátil es indispensable: la frecuencia y amplitud de estos pulsos determinan si la hipo´fisis producira´ preferentemente LH o FSH. Pulsos
rápidos estimulan la liberacio´n de LH, mientras que pulsos
ma´s lentos favorecen la secrecio´n de FSH (1) (12).
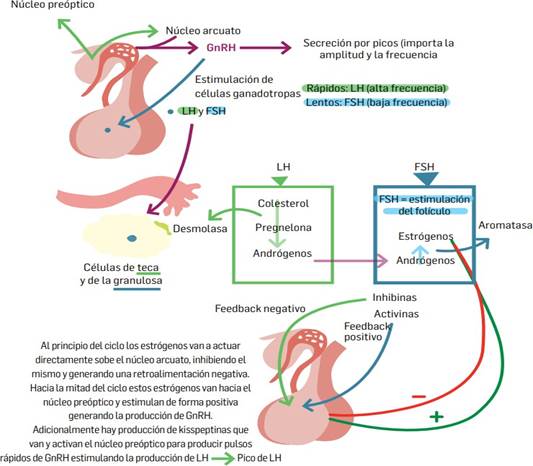
Figura 1. Eje hipota´lamo-hipo´fisis-ovario (1)
La
accio´n de la GnRH sobre ce´lulas gonadotropas
depende de un receptor acoplado a proteí´na G, activando segundos mensajeros como IP3, diacilglicerol y AMPc, promoviendo el ingreso y liberacio´n de calcio intracelular
necesario para la exocitosis hormonal
(12). El eje incluye mecanismos de retroalimentacio´n
largos, cortos y ultracortos que
modulan la secrecio´n hormonal, donde
los esteroides ova´ricos desempen˜an un papel
clave. La regulacio´n local se complementa con
la inhibina, activina y folistatina, pe´ptidos
derivados principalmente de las ce´lulas de la granulosa que modulan la FSH: la inhibina la suprime
selectivamente, la activina
la estimula, y la folistatina inhibe su accio´n
unie´ndose a la activina (1).
En el ovario, la FSH y la LH actu´an sobre un sistema
coordinado de dos ce´lulas. La LH estimula las ce´lulas de la teca para producir andro´genos, que luego las ce´lulas de la granulosa
aromatizan a estro´genos bajo el
estí´mulo de la FSH (1).
El
ciclo folicular inicia varios meses antes de la ovulacio´n, cuando un grupo
de folí´culos comienza a crecer
de manera coordinada. Desde la vida fetal existe
un nu´mero limitado de folí´culos que disminuye progresivamente desde los 6-7 millones iniciales hasta aproximadamente 300 000 en
la pubertad, de los cuales solo unos 400-500 llegara´n
a ovular. En los primeros dí´as del ciclo, la FSH rescata de la atresia a un grupo de folí´culos (reclutamiento), que luego avanzan
hacia los
estadios
preantral y antral (1). La seleccio´n del folí´culo
dominante se logra gracias a un aumento local
de estro´genos y a su accio´n dual: positivamente
sobre el folí´culo en crecimiento e inhibiendo
siste´micamente la FSH, provocando la atresia
de los folí´culos no seleccionados (1).
A
medida que el folí´culo preovulatorio crece,
aumenta la produccio´n de estro´genos, alcanzando un pico sostenido que supera los 200 pg/mL durante aproximadamente 50 horas. Este
nivel elevado genera un inusual
efecto positivo sobre el hipota´lamo y la hipo´fisis, desencadenando el pico de
LH, evento esencial para la ovulacio´n (1). La
ovulacio´n se produce
cuando el folí´culo
rompe su pared tras una serie de procesos
inflamatorios, enzima´ticos y
vasculares estimulados por la LH. Posterior a la ovulacio´n, las ce´lulas de la
granulosa y la teca se
luteinizan formando el cuerpo lu´teo, estructura
endocrina transitoria encargada de la produccio´n
de progesterona. Esta hormona prepara el endometrio para la implantacio´n y, si no ocurre
embarazo, el cuerpo lu´teo degenera entre los
dí´as 9 y 11 postovulatorios, disminuyen los
niveles de progesterona, estradiol e inhibina
A, y se libera nuevamente
la FSH para iniciar un nuevo ciclo
(1).
El ciclo menstrual refleja
estos cambios ova´ricos a nivel del
endometrio, que atraviesa una fase proliferativa bajo estí´mulo estroge´nico y una fase secretora
dependiente de la progesterona (1). Las variaciones en la duracio´n del ciclo son frecuentes en la adolescencia y la perimenopausia, pero en la etapa reproductiva suele mantenerse entre
24 y 38 dí´as, con
sangrado entre 4 y 8 dí´as (1). El funcionamiento
integrado del eje hipota´lamo- hipo´fisis-ovario
es fundamental para la funcio´n menstrual
y reproductiva, y cualquier alteracio´n en la secrecio´n de GnRH, en la respuesta hipofisaria o en la funcio´n ova´rica puede originar
mu´ltiples patologí´as endocrinas y
ginecolo´gicas (12).
Envejecimiento
ovárico y disminución de la reserva
folicular
El
envejecimiento ova´rico es un proceso fisiolo´gico progresivo que acompan˜a a la mujer desde la vida fetal hasta el final de su vida
reproductiva. Este feno´meno se
caracteriza por una disminucio´n cuantitativa y cualitativa de los folí´culos ova´ricos, que
constituyen la unidad funcional y estructural
del ovario.
Desde
la etapa intrauterina se forman entre seis y
siete millones de folí´culos primordiales, pero al momento del nacimiento esta cifra se
reduce a aproximadamente uno a dos
millones por un proceso continuo de
atresia. Para la pubertad sobreviven
alrededor de 300 000 folí´culos, de los cuales solo entre 400 y 500 llegara´n a completar la ovulacio´n
durante la vida reproductiva. Esta pe´rdida
constante se acelera significativamente a partir
de los 35–38 an˜os, cuando la reserva folicular desciende
a niveles crí´ticos
que marcan el inicio
de las etapas finales del envejecimiento ova´rico (4).
La
disminucio´n de la reserva folicular no implica u´nicamente una reduccio´n en el nu´mero de folí´culos disponibles, sino tambie´n un
deterioro progresivo de la calidad
ovocitaria. Los ovocitos envejecidos
presentan alteraciones estructurales del
huso meio´tico, fallos en la segregacio´n cromoso´mica
y un incremento notable de aneuploidí´as.
Este deterioro se relaciona con el dan˜o acumulado
en el ADN nuclear y mitocondrial, lo que afecta directamente la viabilidad
del embrio´n y reduce las tasas de implantacio´n. Así´, el envejecimiento ovocitaria constituye una
de las causas principales de la disminucio´n de la fertilidad y del aumento del riesgo reproductivo en
mujeres mayores de 35 an˜os (8).
En
te´rminos celulares, el envejecimiento ova´rico esta´ condicionado por un incremento del estre´s oxidativo en el microambiente folicular.
Los radicales libres, junto con la
disminucio´n de los sistemas
antioxidantes endo´genos, generan un dan˜o
acumulativo en las membranas, proteí´nas y material
gene´tico del ovocito. Este desequilibrio oxidativo
promueve la atresia folicular y compromete
la competencia del ovocito para completar
adecuadamente la meiosis. Paralelamente, se ha demostrado que la disfuncio´n mitocondrial es un elemento central en el envejecimiento ova´rico. Las mitocondrias, responsables de la produccio´n de ATP
necesario para la maduracio´n del
ovocito, exhiben mutaciones
progresivas en su ADN y una disminucio´n en su capacidad bioenerge´tica con el
avance
de la edad. Esto deteriora la dina´mica mitocondrial,
reduce la distribucio´n adecuada de energí´a
y limita la capacidad del ovocito para sostener
la divisio´n meio´tica, favoreciendo errores cromoso´micos y fallos reproductivos (8).
Los
cambios endocrinos que acompan˜an al envejecimiento
ova´rico tambie´n son fundamentales.
La disminucio´n de folí´culos en crecimiento
reduce la produccio´n de inhibina B y estradiol,
hormonas que normalmente ejercen retroalimentacio´n
negativa sobre la FSH. Como resultado,
la FSH aumenta progresivamente en los primeros
dí´as del ciclo menstrual, lo que inicialmente estimula la maduracio´n
folicular, pero con menor
eficacia debido a la baja
sensibilidad de los folí´culos envejecidos. La respuesta disminuida a la FSH y LH se traduce en ciclos
anovulatorios, cuerpos lu´teos
deficientes y menor
produccio´n de progesterona. Estos cambios endocrinos
explican la irregularidad menstrual
caracterí´stica de la transicio´n hacia la menopausia y la disminucio´n de la capacidad reproductiva (4).
En
las etapas finales del envejecimiento ova´rico, descritas como trayectorias funcionales divergentes, el ovario experimenta cambios anato´micos y funcionales ma´s dra´sticos. El estroma ova´rico adquiere mayor fibrosis, se
reduce el volumen ova´rico y se
observa una disminucio´n marcada del
nu´mero de folí´culos antrales. La corteza
ova´rica se adelgaza y el tejido intersticial
pierde su organizacio´n estructural, lo que compromete au´n ma´s la funcio´n endocrina y gametoge´nica del o´rgano. Adema´s, se
generan variaciones individuales en
la velocidad del deterioro, lo cual
explica por que´ mujeres de la misma
edad pueden mostrar niveles distintos de reserva ova´rica
y patrones menstruales diferentes. Estos
trayectos divergentes esta´n influenciados por factores
gene´ticos, metabo´licos y ambientales que modulan la vulnerabilidad del ovario
al dan˜o oxidativo, la reparacio´n
del ADN y la eficiencia mitocondrial (4).
Finalmente,
la hormona antimülleriana (AMH) es uno de los marcadores
ma´s confiables para evaluar la
reserva folicular durante el envejecimiento. Dado que la
AMH es secretada
por folí´culos preantrales y antrales
pequen˜os, su descenso progresivo refleja con
precisio´n la disminucio´n de la cohorte folicular. La AMH cae an˜os antes de la aparicio´n de irregularidades menstruales, lo que la convierte en un indicador
precoz del envejecimiento ova´rico y en
una herramienta clí´nica de gran utilidad para
estimar la capacidad reproductiva y el tiempo aproximado hacia la transicio´n menopa´usica (8).
En
conjunto, el envejecimiento ova´rico constituye un proceso complejo, multifactorial y progresivo que involucra cambios anato´micos,
endocrinos, celulares y moleculares. La reduccio´n acelerada
de la reserva folicular, el
deterioro ovocitario, la disfuncio´n
mitocondrial, el aumento del estre´s oxidativo y la alteracio´n en las retroalimentaciones hormonales convergen para producir
una disminucio´n gradual de la
fertilidad y una transicio´n hacia
ciclos irregulares que culminan finalmente
en la menopausia.
Fisiología del
eje HHO durante la perimenopausia
El
eje HHO durante la perimenopausia, muestra una
reconfiguracio´n multifactorial: el nu´mero de
folí´culos en reserva disminuye progresivamente, con declive de AMH e inhibina B que reduce la retroalimentacio´n inhibidora sobre FSH;
como resultado hay una elevacio´n compensatoria de FSH y aumentos variables
de LH que reflejan la pe´rdida de sensibilidad hipotala´mica a los estro´genos. Sin embargo, la
perimenopausia no es una simple reduccio´n
lineal de hormonas: el estradiol presenta fluctuaciones intensas e impredecibles — incluyendo picos altos intercalados con
caí´das marcadas— mientras la
progesterona tiende a disminuir de forma sostenida
por mayor frecuencia de ciclos anovulatorios; estas alteraciones explican
la amplia variabilidad de patrones menstruales y sí´ntomas entre mujeres. (3,9)
La
desorganizacio´n del patro´n pulsa´til de GnRH en perimenopausia se
explica por la pe´rdida de la retroalimentacio´n
negativa efectiva: con menos folí´culos
que producen inhibinas y estradiol sostenido,
las neuronas KNDy y las ví´as hipotala´micas
modifican su actividad (mayor frecuencia
e irregularidad de pulsos), lo que conduce a respuestas
hipofisarias ma´s erra´ticas y a una secrecio´n gonadotro´pica ma´s elevada
y variable; a su vez, la alteracio´n
del balance kisspeptina/NKB/dinorfina
se relaciona tanto con los sofocos
como con la alteracio´n del pulso GnRH. (7,11)
Adema´s de estas
alteraciones neuroendocrinas,
la esteroidoge´nesis cambia:
a medida que la funcio´n
folicular declina hay una reorientacio´n relativa
de
las
ví´as delta-4 y delta-5 y un mayor aporte suprarrenal
de precursores (DHEAS, androstenediona)
que modifica la mezcla de esteroides
circulantes —en etapas tardí´as se observa mayor correlacio´n de LH con andro´genos y una asociacio´n negativa de FSH con
estradiol—; esto contribuye a un
fenotipo hormonal donde los andro´genos
no caen tan ra´pidamente como los estro´genos y donde estrona (metabolito perife´rico) puede tener mayor relevancia. (4)
La
variabilidad en la duracio´n y el patro´n del
sangrado menstrual durante la perimenopausia
es una consecuencia directa de lo
anterior: los ciclos pueden acortarse
(por rescate precoz
de folí´culos) o alargarse (por anovulacio´n u oligo/amenorrea), y los cambios ma´s marcados en la longitud
del ciclo tienden a aparecer en los an˜os
ma´s pro´ximos a la u´ltima menstruacio´n, con un gran aumento
de ciclos largos en el an˜o final antes de la FMP (u´ltima menstruacio´n) estas caracterí´sticas pueden usarse como marcadores clí´nicos de proximidad a
la menopausia. (5)
A
nivel ova´rico celular y molecular, el envejecimiento
ova´rico que subyace a la perimenopausia
implica reduccio´n de la reserva primordial
y de los grupos de folí´culos en crecimiento,
disminucio´n de la calidad ovocitaria (dan˜o
mitocondrial y fragmentacio´n/lesio´n de ADNmt),
aumento del estre´s oxidativo y remodelacio´n
estromal (fibrosis e inflamacio´n local)
que alteran la comunicacio´n ovocito- granulosa
y la esteroidoge´nesis. Estos procesos explican
por que´ la fertilidad declina antes que la produccio´n
estroge´nica deje de ser clí´nicamente aparente
y por que´ la AMH y el recuento de folí´culos
antralesson marcadores u´tiles de reserva, mientras que FSH aumenta conforme la
inhibina B cae. (9,10)
Tabla 1. Comparacio´n
entre etapa reproductiva vs etapa perimenopa´usica

Reserva folicular
(AMH/AFC)
AMH estable;
AFC adecuado AMH ↓; AFC ↓; variabilidad marcada
Inhibina
B Normal; inhibe FSH ↓
→ FSH ↑ temprano Estradiol (E2) Picos predecibles Fluctuante, impredecible Progesterona Fase
lútea regular ↓ por anovulación
FSH / LH Patrones normales FSH ↑,
LH variable
GnRH Pulsos regulares Pulsos desorganizados Esteroidogénesis Vía
delta-4 ↑ delta-5; andrógenos relativos ↑ Endometrio Proliferativo
→ secretor Desincronizado; sangrado
irregular Síntomas Mínimos Sofocos,
insomnio, labilidad
Mecanismos celulares DDR eficiente Estrés oxidativo
↑; DDR ↓
Eje HPA Estable Influencia del cortisol variable
*Elaboracio´n propia. AMH: Hormona
antimülleriana. AFC: Conteo de folí´culos antrales. FSH: Hormona
folí´culo- estimulante. LH: Hormona luteinizante. DDR: Respuesta al dan˜o del ADN (DNA Damage Response).
HPA: Eje hipota´lamo-hipo´fisis-adrenal.
Integrando niveles:
neuroendocrino (GnRH/KNDy
→
FSH/LH), ova´rico (recuento folicular, calidad
ovocitaria, AMH/inhibina) y molecular (estre´s oxidativo, reparacio´n ADN, incompetencia mitocondrial), la perimenopausia se explica como una transicio´n heteroge´nea en la que mujeres con trayectorias
ra´pidas presentan caí´da abrupta de estradiol
y subidas marcadas de FSH, mientras otras mantienen
actividad hormonal relativamente conservada ma´s tiempo. (9,3)
Consecuencias
neuroendocrinas de la inestabilidad
del eje HHO
La
transicio´n perimenopa´usica genera una marcada inestabilidad del
eje hipota´lamo hipo´fisis ovario
(HHO), cuyo efecto principal es la caí´da progresiva
e irregular del estradiol. Esta fluctuacio´n
hormonal tiene profundas repercusiones
neuroendocrinas debido a la estrecha
relacio´n entre el estradiol y la funcio´n cerebral.
La disminucio´n estroge´nica altera el acoplamiento
entre los receptores estroge´nicos y los
sistemas bioenerge´ticos neuronales, produciendo
un estado de hipometabolismo cerebral
que afecta memoria, procesamiento cognitivo
y regulacio´n emocional, adema´s de aumentar
la vulnerabilidad a futuros procesos neurodegenerativos (3).
Los
cambios hormonales tambie´n modifican el equilibrio
de neurotransmisores como serotonina, dopamina
y noradrenalina. Las fluctuaciones del estradiol
reducen la modulacio´n normal de estos sistemas
monoamine´rgicos, lo que contribuye a sí´ntomas
afectivos, irritabilidad, ansiedad y variaciones del estado de a´nimo. Adema´s, el estre´s oxidativo y la neuroinflamacio´n, feno´menos que se incrementan por la disminucio´n
estroge´nica, exacerban la
disfuncio´n en neurotransmisores y potencian
la aparicio´n de depresio´n y trastornos del
suen˜o (5).
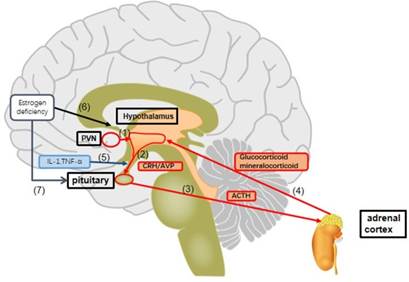
Figura 2. Alteracio´n del eje hipota´lamo–hipo´fisis– adrenal inducida
por la deficiencia estroge´nica (5)
Un
aspecto fundamental de la fisiopatologí´a neuroendocrina
de la perimenopausia es la alteracio´n
en los circuitos hipotala´micos responsables de la termorregulacio´n. La caí´da del estradiol
incrementa la actividad de las neuronas KNDy
(kisspeptina neuroquinina B dinorfina), lo que
reduce la retroalimentacio´n negativa hacia el
hipota´lamo. Este aumento en la sen˜alizacio´n de neuroquinina B desestabiliza el centro termorregulador y origina los sofocos, uno de los sí´ntomas
ma´s caracterí´sticos del climaterio (11).
La
reduccio´n estroge´nica tambie´n favorece un
ambiente neuroinflamatorio. En la perimenopausia se observa activacio´n microglial, incremento de citoquinas proinflamatorias y deterioro de
la funcio´n
mitocondrial, factores que elevan el estre´s oxidativo en el sistema nervioso central.
Este estado inflamatorio cro´nico no
solo explica sí´ntomas como fatiga,
alteraciones del suen˜o y disminucio´n
cognitiva, sino que tambie´n incrementa
el riesgo de dan˜o neurovascular y de enfermedades
neurodegenerativas en etapas posteriores (5,12).
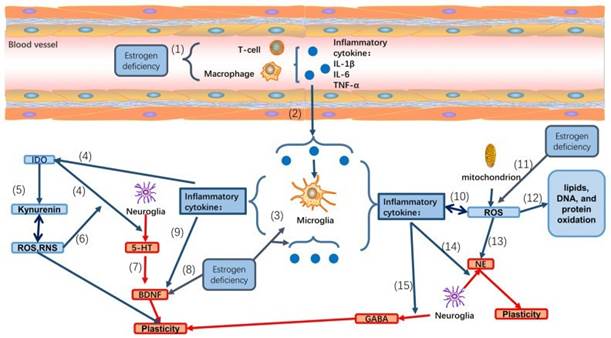
Figura 3. Ví´a neuroinflamatoria
asociada a la disminucio´n de estro´genos durante la
perimenopausia (5).
Finalmente, la suma de hipometabolismo neuronal,
neuroinflamacio´n, estre´s oxidativo, disfuncio´n en neurotransmisores y alteraciones
hipotala´micas convierte a la
perimenopausia en una “transicio´n neurolo´gica”, en la cual los cambios
endocrinos se reflejan directamente en sí´ntomas
emocionales, cognitivos, autono´micos
y metabo´licos. La evidencia indica
que esta etapa representa una ventana
de vulnerabilidad cerebral que puede influir en la salud neurolo´gica a largo plazo (3,12).
Caracterización
clínica del ciclo menstrual perimenopáusico
y sistema STRAW+10
La
perimenopausia se define como la etapa de transicio´n
alrededor de la menopausia en la que comienzan a observarse cambios
progresivos en la regularidad
de los ciclos menstruales, en el perfil hormonal
y en la aparicio´n de sí´ntomas que impactan
la calidad de vida. Abarca los an˜os previos a la u´ltima menstruacio´n y los primeros
an˜os posteriores, constituyendo el inicio del climaterio y un
periodo de “cambios fisiolo´gicos espectaculares” en el que se incrementan tambie´n riesgos
cro´nicos como la osteoporosis (14). En la pra´ctica
clí´nica se distingue una fase de perimenopausia temprana, en la que los ciclos
au´n son relativamente
frecuentes, pero empiezan a variar en
duracio´n y cantidad, con ovulacio´n intermitente,
y una perimenopausia tardí´a, caracterizada
por intervalos prolongados de amenorrea,
mayor irregularidad del sangrado y aumento
de la intensidad de los sí´ntomas vasomotores
y neuropsicolo´gicos (2,13,14).
El
sistema STRAW+10 se ha incorporado en revisiones
clí´nicas como StatPearls y en el trabajo de
Santoro como marco para clasificar el envejecimiento
reproductivo y describir la transicio´n
menopa´usica (2,13). Estas revisiones resaltan
que la perimenopausia engloba la transicio´n
menopa´usica temprana y tardí´a, definida
sobre todo por el patro´n de sangrado: primero
por una mayor variabilidad en la
longitud del ciclo y, ma´s adelante,
por episodios de amenorrea prolongada (2,13). El esquema
enfatiza que el criterio
principal para la etapa es la clí´nica del
sangrado menstrual, mientras que los marcadores
hormonales se consideran complementarios ma´s que determinantes, de modo que el diagno´stico en la pra´ctica se
basa en la historia menstrual y el
contexto sintoma´tico ma´s que en un
u´nico valor de laboratorio (2,13,14).
Desde el punto de vista del ciclo, uno de los cambios ma´s precoces es la alteracio´n de la
duracio´n y regularidad de los ciclos
menstruales. Al inicio puede observarse un ligero acortamiento de la fase folicular,
con ciclos algo ma´s cortos; conforme progresa
la transicio´n, los ciclos se vuelven irregulares,
alternando periodos de ciclos relativamente
normales con episodios de oligomenorrea
o amenorrea, y en la perimenopausia tardí´a
son tí´picos los intervalos
prolongados
sin menstruacio´n seguidos de sangrados
irregulares o abundantes, configurando un patro´n de sangrado
ano´malo perimenopa´usico (2,13,14). Estos cambios reflejan la
pe´rdida de coordinacio´n entre la
reserva folicular y el eje hipota´lamo
hipo´fisis ovario, con alternancia de ciclos
ovulatorios, oligoovulatorios y francamente anovulatorios (2,14).
La
base endocrina de estos feno´menos es el agotamiento progresivo de la reserva
folicular, con disminucio´n de la produccio´n de
estradiol e inhibinas por el ovario.
La caí´da de inhibina B y estradiol
reduce la retroalimentacio´n negativa sobre
la hipo´fisis y conduce a una elevacio´n sostenida de FSH, mientras
que los niveles de LH se modifican en menor grado (2,13). No
obstante, la reduccio´n del estradiol
no es lineal: se describen fluctuaciones
amplias y erra´ticas, con picos elevados
y fases de hipoestrogenismo marcado, lo que
contribuye tanto a la irregularidad del ciclo
como a la coexistencia de sí´ntomas de de´ficit y de “exceso relativo” de estro´genos (2,13).
En la medida en que aumentan los
ciclos anovulatorios, disminuye la
formacio´n de cuerpos lu´teos funcionales
y se instaura una insuficiencia relativa de
progesterona en la fase lu´tea; el endometrio
queda expuesto de forma intermitente a estí´mulos estroge´nicos
sin una estabilizacio´n progestacional
adecuada, favoreciendo el sangrado uterino irregular o disfuncional tí´pico de la perimenopausia (2,14).
Clí´nicamente,
la combinacio´n de alteraciones del patro´n de sangrado,
elevacio´n de FSH con estradiol fluctuante y ciclos anovulatorios se
acompan˜a de un conjunto de sí´ntomas
caracterí´sticos. Las revisiones
destacan que los sofocos y las sudoraciones
nocturnas son los sí´ntomas vasomotores
ma´s frecuentes y afectan a una elevada
proporcio´n de mujeres, con impacto relevante
sobre el suen˜o y la calidad
de vida (2,13).
Se
an˜aden sí´ntomas neuropsicolo´gicos como irritabilidad,
ansiedad, trastornos del suen˜o, labilidad
afectiva y dificultades de concentracio´n, con mayor riesgo de sí´ntomas depresivos durante la perimenopausia que en la etapa premenopa´usica
(2).
La disminucio´n estroge´nica progresiva favorece
adema´s el desarrollo de sí´ntomas genitourinarios
(sequedad vaginal, dispareunia, urgencia
y polaquiuria), junto con otros sí´ntomas como
cefaleas, fatiga, artralgias y cambios en la
composicio´n corporal, en un contexto
de aumento de riesgo de osteoporosis y enfermedad cardiovascular descrito en las
monografí´as de climaterio (2,13,14).
En conjunto, la perimenopausia se
configura como una etapa claramente
delimitada del ciclo vital femenino, cuyo
entendimiento clí´nico apoyado en la clasificacio´n
STRAW+10 es esencial para el diagno´stico oportuno y el abordaje
individualizado de las mujeres
en transicio´n menopa´usica (2,13,14).
Los
hallazgos analizados muestran que la perimenopausia
es una etapa de inestabilidad neuroendocrina
ma´s que un simple tra´nsito reproductivo.
La fluctuacio´n del estradiol desorganiza
el eje HHO y se expresa en manifestaciones
emocionales, cognitivas y autono´micas.
Hormaza et al. sen˜alan que los cambios
en la retroalimentacio´n estroge´nica alteran
la dina´mica de GnRH y FSH, generando anovulacio´n
y variabilidad extrema del estradiol que
marca el inicio de la transicio´n (1).
Desde
una perspectiva neurobiolo´gica, esta oscilacio´n
estroge´nica altera procesos que habitualmente
se mantienen finamente regulados. Casteel et al. demostraron que la caí´da intermitente del estradiol modifica la funcio´n de
sistemas monoamine´rgicos,
especialmente serotonina y noradrenalina, lo que explica
la alta prevalencia de irritabilidad, ansiedad y trastornos del
suen˜o observados durante esta etapa
(12). La evidencia de Grub y
colaboradores an˜ade que esta vulnerabilidad
emocional no es u´nicamente un feno´meno
subjetivo, sino el resultado de un desacoplamiento
entre receptores estroge´nicos, metabolismo
energe´tico neuronal y plasticidad sina´ptica, feno´meno que predispone a disfuncio´n cognitiva y disminucio´n de la resiliencia neuropsicolo´gica (6).
La
termorregulacio´n, uno de los sí´ntomas ma´s
distintivos del climaterio, tambie´n emerge como un reflejo directo de esta inestabilidad neuroendocrina. La hiperactividad de las neuronas
KNDy, inducida por la pe´rdida de retroalimentacio´n estroge´nica, ha sido descrita por Kawakita
et al. como el mecanismo clave detra´s de los
sofocos, confirmando que el climaterio es un
proceso profundamente cerebral y no meramente endocrino perife´rico (9).
Los
elementos de neuroinflamacio´n y estre´s oxidativo
se vuelven un eje explicativo central. Ferrell
et al. muestran que la disminucio´n de estradiol aumenta
la activacio´n microglial y altera la funcio´n mitocondrial, creando un microambiente inflamatorio que intensifica sí´ntomas y
eleva el riesgo neurodegenerativo
(16). Esto define a la perimenopausia
como una “ventana de vulnerabilidad cerebral”.
En
conjunto, la literatura indica que la perimenopausia es un feno´meno donde la biologí´a ova´rica,
la dina´mica hipotala´mica y la plasticidad cerebral interactu´an. Ma´s que una disminucio´n hormonal, implica una reorganizacio´n neuroendocrina que sostiene la homeostasis emocional, cognitiva y autono´mica.
Comprender esta complejidad permite explicar mejor su clí´nica
y orientar estrategias terape´uticas ma´s precisas.
CONCLUSIONES
· La evidencia disponible indica que la perimenopausia constituye una etapa de
contribuyendo a la desregulacio´n
del eje HHO y a
los cambios en el patro´n menstrual.
reorganizacio´n fisiolo´gica del eje hipota´lamo- hipo´fisis-ovario (HHO), caracterizada por una inestabilidad neuroendocrina ma´s que por una simple
deficiencia hormonal.
·
La disminucio´n progresiva
de la reserva folicular, junto con la reduccio´n de inhibina B y AMH, altera la retroalimentacio´n
negativa, generando elevaciones irregulares de FSH y, en menor
grado, de LH, lo que favorece la anovulacio´n
y la irregularidad menstrual.
·
Las fluctuaciones del estradiol
desempen˜an un papel central, al modificar la secrecio´n pulsa´til
de GnRH y la sensibilidad hipotala´mica,
·
A nivel neuroendocrino, la
variabilidad estroge´nica impacta en
neurotransmisores, metabolismo
cerebral y plasticidad sina´ptica, incrementando
la susceptibilidad a sí´ntomas emocionales,
cognitivos y autono´micos, en un contexto
de neuroinflamacio´n mediado por activacio´n
microglial y estre´s oxidativo.
·
Finalmente, la transicio´n
perimenopa´usica es heteroge´nea y
modulada por factores gene´ticos,
metabo´licos y ambientales, lo que sustenta la necesidad de un abordaje
integral y personalizado basado en los mecanismos fisiopatolo´gicos del eje HHO.
REFERENCIAS BIBLIOGRÁFICAS
1.
Hormaza A' ngel MP, Jaramillo Jaramillo LI. Endocrinología ginecológica: claves
para la práctica en la actualidad.
Medellí´n: Universidad Pontificia Bolivariana; 2024.
2.
Santoro N. Perimenopause:
from research to practice. J Womens
Health (Larchmt). 2016;25(4):332-339. doi:10.1089/jwh.2015.5556
3. Brinton RD, Yao J, Yin F, Mack WJ, Cadenas E. Perimenopause as a neurological transition
state. Nat Rev Endocrinol.
2015;11(7):393-405. doi:10.1038/nrendo.2015.82
4. Bochynska S, Garcí´a-Pe´rez MA' , Tarí´n
JJ, Szeliga A, Meczekalski
B, Cano A. The final stages of ovarian aging:
a story of divergent functional trajectories. J Clin Med. 2025;14(16):5834.
doi:10.3390/jcm14165834
5.
Liang G, Kow ASF, Yusof R, Tham CL, Ho YC, Lee MT. Depression
associated with menopause: impact of oxidative
stress and neuroinflammation in the central
nervous system—a review. Biomedicines. 2024;12(1):184.
doi:10.3390/biomedicines12010184
6.
Grub J, Süss H, Willi J, Ehlert U. Steroid
hormone secretion over the course of
the perimenopause: findings from the Swiss perimenopause study. Front Glob Womens Health. 2021;2:774308. doi:10.3389/fgwh.2021.774308
7.
Garrigo CK. Etapa de perimenopausia [Internet]. 2021. Disponible en: https://rid.unaj.edu.ar/items/5054a48c-b343- 40ef-846c-8af0975e670d
8.
Wang X, Wang L, Xiang W.
Mechanisms of ovarian aging in women:
a review. J Ovarian Res. 2023;16(1):67. doi:10.1186/s13048-023-01151-z
9. Kawakita T, Yasui T, Yoshida K, Matsui S, Iwasa
T. Associations of LH and FSH with
reproductive hormones depending on
each stage of the menopausal
transition. BMC Womens Health. 2023;23(1):286. doi:10.1186/s12905-023-02438-5
10.
Talaulikar V. Menopause
transition: physiology and symptoms.
Best Pract Res Clin Obstet
Gynaecol. 2022;81:3-7. doi:10.1016/j.bpobgyn.2022.03.003
11. Rance NE. Menopause and the human hypothalamus: evidence for the role of kisspeptin/neurokinin B neurons in the
regulation of estrogen negative
feedback. Peptides. 2009;30(1):111-122.
doi:10.1016/j.peptides.2008.05.016
12.
Casteel A, et al. Estrogen fluctuation and monoaminergic dysregulation in
perimenopause. Neuroendocrinology. 2020;110(5):350-362. doi:10.1159/000507123
13.
McCarthy M, Raval AP. The
peri-menopause in a woman’s life: a
systemic inflammatory phase that enables
later neurodegenerative disease. J Neuroinflammation. 2020;17(1):317. doi:10.1186/s12974-020-01998-9
14. Peacock K, Carlson
K, Ketvertis KM. Menopause. In: StatPearls
[Internet]. Treasure Island (FL): StatPearls
Publishing; 2025. Disponible en: https://www.ncbi.nlm.nih.gov/books/NBK507826
15.
Sa´nchez Borrego R. Perimenopausia:
el climaterio desde su inicio.
Madrid: Schering Espan˜a; 2021.
16.
Ferrell S, et al. Estrogen
deficiency, microglial activation and
neuroinflammatory cascades in perimenopause. Neuroimmunol Rep. 2023;4:100145. doi:10.1016/j.nirep.2023.100145