Inoculante constituido por Rhizobium leguminosarum, Burkholderia ubonensis y Trichoderma harzianum incrementa el número de sitios activos para la nodulación de Pisum sativum
Inoculant constituted by Rhizobium leguminosarum, Burkholderia ubonensis and Trichoderma harzianum increases the number of active sites for nodulation of Pisum sativum
David Zavaleta-Verde1,*; Bertha Soriano Bernilla1; Marco Antonio López Calvo2
1 Facultad de Ciencias Biológicas, Universidad Nacional de Trujillo, Av. Juan Pablo II s/n – Ciudad Universitaria, Trujillo, Perú.
2 Instituto de Educación Superior Tecnológica Mache, Calle Maravillas 321, Mache, Otuzco, La Libertad, Perú
*Autor corresponsal: ezverde@unitru.edu.pe (D. Zavaleta-Verde).
D.
Zavaleta-Verde: ![]() https://orcid.org/0000-0003-0382-8420
https://orcid.org/0000-0003-0382-8420
B.
Soriano: ![]() https://orcid.org/0000-0001-9216-7788
https://orcid.org/0000-0001-9216-7788
DOI: http://dx.doi.org/10.17268/manglar.2020.015
RESUMEN
Las plantas de Pisum sativum para su crecimiento requieren altas concentraciones de nitrógeno, que se obtienen principalmente de la fijación simbiótica con microorganismos. Con el objetivo de evaluar el efecto de un inoculante microbiano multicepa en la nodulación de P. sativum, se sembró el cultivar INIA-102 Usui de P. sativum, con un inoculante constituido por Rhizobium leguminosarum, Burkholderia ubonensis y Trichoderma harzianum, en soporte sólido (turba) y líquido (caldo extracto de levadura manitol - YMB), para lo cual se diseñó cuatro tratamientos. El inoculante favoreció la infectividad del rizobio y la formación de nódulos efectivos, los cuales se distribuyeron principalmente en raíces secundarias, y fue el tratamiento T4 (en soporte sólido) que reportó mayor número de nódulos (148,7 recuentos/planta) y mayor peso seco de los mismos (0,386 g/planta), que el tratamiento T3 (en soporte líquido). Por lo tanto, el inoculante microbiano multicepa en soporte sólido tiene mayor efecto significativo en la nodulación de Pisum sativum, ya que pudo haber favorecido la expansión de la longitud y masa del sistema radicular, incrementando de esa manera el número de sitios activos para la nodulación.
Palabras clave: nodulación; Rhizobium; Burkholderia; Trichoderma; Pisum sativum.
ABSTRACT
The plants of Pisum sativum for growth require high concentrations of nitrogen, which are obtained mainly from the symbiotic with microorganisms. With the objective of evaluating the effect of a microbial inoculant multicepa in nodulation of P. sativum, where he sowed the cultivar INIA-102 Usui of P. sativum, with an inoculant constituted by Rhizobium leguminosarum, Burkholderia ubonensis and Trichoderma harzianum, in solid support (peat) and liquid (Yeast Extract Mannitol Broth - YMB), for which it was designed four treatments. The favored the infectivity of inoculant rhizobia and the formation of nodules troops, which were distributed mainly in secondary roots, and was the treatment T4 (in solid support) that reported the greatest number of nodules (148.7 counts/plant) and greater dry weight of the same (0.386 g/plant), that the treatment T3 (in liquid). Therefore, the microbial inoculant multicepa in solid support has the most significant effect on nodulation of Pisum sativum, since it could have contributed to the expansion of the length and mass of the root system, thereby increasing the number of active sites for nodulation.
Keywords: nodulation; Rhizobium; Burkholderia; Trichoderma; Pisum sativum.
INTRODUCCIÓN
Las leguminosas establecen relaciones simbióticas con los Rhizobios para suplir su incapacidad de asimilar el nitrógeno atmosférico, proceso que si realizan este grupo de α y β-proteobacterias, a lo que se denomina Fijación Biológica del Nitrógeno (FBN). La FBN es usada para remplazar los fertilizantes nitrogenados en la producción de leguminosas, debido a su eficiencia económica en la provisión de servicios de agroecosistemas sostenibles (Ouma et al., 2016; Sulieman and Phan Tran, 2015).
Pisum sativum es una leguminosa considerada como guisante a nivel mundial, se consume en forma fresca, enlatada y como grano. Tiene una gran capacidad de fijación simbiótica de nitrógeno con Rhizobium leguminosarum (Chao et al., 2017). En la sierra del Perú, la arveja más cultivada es el cultivar INIA-102 Usui, liberada por el Instituto Nacional de Innovación Agraria (INIA). Tiene buena adaptación a diferentes condiciones agroecológicas, buen potencial de rendimiento, tolerancia a enfermedades. Se cultiva en los Departamentos de Cajamarca, La Libertad y Junín (Ministerio de Agricultura, 2016).
Los inoculantes comerciales son formulaciones desarrolladas para favorecer el crecimiento y la supervivencia de los microorganismos dentro del inoculante, así como también la supervivencia durante su aplicación, particularmente en la semilla (Lesueur et al., 2016). Estos inoculantes pueden ser monocepa o multicepa, de acuerdo al número de especies microbianas que lo constituyen; y generalmente se envasan en forma de polvo, granular o líquido, siendo la turba el soporte preferido para crecimiento y supervivencia de rizobios (Albareda et al., 2008).
En muchos inoculantes se ha incluido a Burkholderia ubonensis, miembro del complejo Burkholderia cepacia (Bcc), un grupo genéticamente relacionado con especies ambientales metabólicamente diversas, altamente adaptables y ampliamente dispersas (De Smet et al., 2015), ha sido aislada de la rizosfera de diversos cultivos en donde cumple el rol de Promotor del Crecimiento Vegetal (PCV) ya que produce fitohormonas, fija nitrógeno atmosférico y solubiliza fosfatos.
Otro microorganismo considerado PCV es el hongo filamentoso Trichoderma harzianum por sus mecanismos de controlador biológico como micoparasitismo, antibiosis o competencia (Carrero et al., 2018; Medeiros et al., 2017). Es también ampliamente estudiado su capacidad de inducir las defensas de los vegetales (Yedidia et al., 1999) y estimular el crecimiento y desarrollo estableciendo un diálogo molecular con las raíces (Mendoza et al., 2018). Se han informado interacciones beneficiosas mutuales entre Trichoderma spp. y P. sativum (Contreras et al., 2009; Samolski et al., 2012).
La producción de leguminosas utilizando inoculantes microbianos tiene muchos beneficios, como disminuir los costos de producción y con ello se más asequible para los pequeños agricultores de escasos recursos (Singh et al., 2016), también podría ser un factor importante cuando la planta se introduce en un nuevo agroecosistema (Klock et al., 2015; La Pierre et al., 2017). La inducción de los Rhizobios a la formación de nódulos es beneficioso para la planta ya que según Koskey et al. (2017), existe relación entre el número de nódulos y el incremento de la FBN.
Por lo mencionado anteriormente, este estudio estuvo orientado a evaluar el efecto de un inoculante microbiano multicepa en la nodulación de P. sativum cultivada en Mache, La Libertad, Perú.
MATERIAL Y MÉTODOS
Se utilizó un inoculante microbiano multicepa conformado por las bacterias Rhizobium leguminosarum, Burkholderia ubonensis y el hongo Trichoderma harzianum. Además de semillas certificadas de Pisum sativum cultivar INIA-102 Usui.
Métodos
Reactivación de los microorganismos
En la reactivación de la cepa rizobiana, se tomó como referencia la metodología sugerida por Somasegaran y Hoben, (1994). Se cultivó Rhizobium leguminosarum mediante estrías paralelas en placas de Petri con agar extracto de levadura manitol (YMA) con rojo de congo, y se incubó a 28°C por 3 días, luego una colonia aislada se conservó en medio inclinado YMA a 4°C hasta su posterior uso. Para la reactivación de Burkholderia ubonensis, se siguió la metodología sugerida en el manual de Bergey’s (Brenner, 2005), se cultivó en agar soya tripticasa (TSA) por 3 días a 30°C. Trichoderma harzianum fue reactivado en agar papa dextrosa (APD), en ausencia de luz, a temperatura ambiente por 7 días.
Preparación de inoculante microbiano multicepa
Se preparó dos tipos de soportes, uno sólido elaborado con turba fina estéril, estandarizada a pH 6,8 con carbonato de calcio al 3% (CaCO3) y otro líquido con caldo extracto de levadura manitol (YMB), según Somasegaran y Hoben, (1994). Cada microorganismo reactivado fue inoculado en los soportes asegurando una concentración final de 108 cel/g o mL, respectivamente. En el caso del inoculante sólido se dejó madurar a temperatura aproximada de 20 °C por 7 días.
Acondicionamiento de terreno de cultivo
Un terreno de cultivo de 420 m2 fue preparado teniendo en cuenta las técnicas agronómicas, considerándose también, antes de la siembra, su humedad y capacidad de campo (Somasegaran y Hoben, 1994). Se habilitó unidades experimentales de 20m2 para cada tratamiento en estudio (Tabla 1), considerando 0,75 m de distancia entre surcos y 0,5 m de separación entre tratamientos.
Tabla 1
Descripción de los tratamientos usados en la experimentación
|
Tratamientos (T) |
Descripción |
|
T1 |
Control negativo* |
|
T2 |
Control positivo** |
|
T3 |
Inoculante en soporte sólido |
|
T4 |
Inoculante en soporte líquido |
Nota: * Sin inocular; ** Recibió fertilización con N, P y K inorgánicos.
Siembra de Pisum sativum e inoculación
Se mezcló 100 g de semillas con 3 mL de una solución azucarada estéril, luego se agregó 10 g o 10 mL del inoculante sólido o líquido respectivamente, se homogenizó con movimientos suaves, hasta asegurar la distribución uniforme del inoculante. Se sembró tres semillas por golpe con una separación de 0,3 m, evitando en todo momento la contaminación cruzada, las herramientas como palanas u otros, fueron desinfestadas con alcohol de 70° en cada tratamiento. Se sembró en las primeras horas del día evitando la exposición del inoculante a la luz solar directa.
El manejo agronómico de la leguminosa se realizó según la metodología propuesta por el Instituto de Innovación Agraria INIA, con riegos en promedio de 3500 a 4000 m3/ha según las necesidades del cultivo y la disponibilidad de agua; el deshierbo fue manual, y para el control de plagas se usó control entomológico (trampas amarillas y trampas negras).
Evaluación de la nodulación
Se realizó a los 45 días de la siembra, en la etapa de prefloración, se determinó aspectos cualitativos y cuantitativos. Se extrajo al azar 3 plantas de cada unidad experimental, a las cuales se evaluó distribución, coloración, número y peso seco de los nódulos.
Análisis de datos
Todos los tratamientos fueron distribuidos en un diseño de bloques completo al azar, con cuatro repeticiones.
La diferencia de medias entre los resultados obtenidos fue analizada mediante la prueba t-student al 95% de confianza. Además, para evaluar la igualdad de varianzas entre los resultados se utilizó la prueba de Levene (p = 0,05). También se evaluó que los resultados tengan una distribución normal, mediante la prueba de Shapiro-Wilk (p = 0,05). Se utilizó el software RStudio-1.2.5033.
RESULTADOS Y DISCUSIÓN
El uso de un inoculante microbiano multicepa tuvo un efecto significativo en Pisum sativum, se observó sistemas radiculares con nódulos distribuidos principalmente en raíces secundarias, considerado un parámetro muy importante para evaluar el rendimiento de plantas (Boudjabi et al., 2017; Panasiewicz et al., 2019), estos nódulos resultaron ser infectivos y efectivos por la coloración rojiza interna, debido a la leghemoglobiana activa que protege la dinitrogenasa del rizobio (Khan et al., 2014; Farid y Navabi, 2015).
Por otro lado, la disponibilidad de fósforo (P) en suelo, contribuyó a la formación de nódulos, como lo demuestran Bello et al. (2018) quienes encontraron que la nodulación de caupí por rizobios aumentó significativamente (p < 0,05) por el uso de superfosfato simple (SSP). El inoculante microbiano multicepa estuvo constituido además por Burkholderia ubonensis, bacteria ampliamente estudiada por su capacidad de solubilizar el fósforo inorgánico en suelo y hacerlo disponible para la asimilación por las plantas, entonces también esta bacteria influyó indirectamente en la formación de nódulos.
En cuanto al número de nódulos (Figura 1), si bien es cierto no existió diferencia significativa (p = 0,059 > 0,05) entre las medias de los tratamientos T3 y T4, se observó que T4 presentó el mayor número de nódulos promedio (148,7 recuentos/planta), así mismo presentó un menor coeficiente de variación (CV% = 4,702%), indicando un comportamiento muy homogéneo. Si bien se tiene en cuenta que a mayores células bacterianas por gramo de suelo será mayor el número de nódulos en el sistema radicular, entonces este tipo de soporte favorece la viabilidad de los microorganismos.
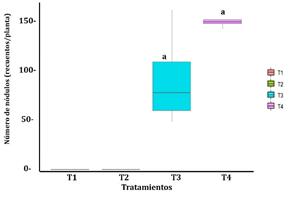
Figura 1. Número de nódulos promedio en plantas de Pisum sativum según los tratamientos experimentales. T1 control negativo, T2 control positivo, T3 inoculante en soporte sólido y T4 inoculante en soporte líquido.
Nota: Prueba t-student (p = 0,059 > 0,05); Levene (p = 0,083 > 0,05) y Shapiro-Wilk en los tratamientos T3 y T4 (p = 0,4378 y p = 0,5955, respectivamente).
El peso seco de los nódulos refleja una fijación simbiótica de nitrógeno más eficiente que podría resultar en un aumento de la biomasa de la planta (Kawaka et al., 2014; Delić et al. 2010), también Unkovich et al. (2010) informaron de una fuerte correlación positiva entre la biomasa de guisantes y el peso seco de nódulos al ser inoculados con rizobios. La Figura 2 nos muestra que el valor p de significancia de la prueba de hipótesis de la diferencia de medias t-student, es menor que 0,05 (p = 0,003 < 0,05), evidenciando que existió diferencia significativa entre los tratamientos T3 y T4, siendo el tratamiento 4, quién presentó el mayor peso de nódulos promedio (0,386 g/planta), lo que implicaría ser más eficiente en la fijación simbiótica del nitrógeno, esto debido a que hay una relación directa entre el número de nódulos y el peso seco de los mismos.
Esta experimentación ha demostrado la infectividad y efectividad de Rhizobium leguminosarum como simbionte de P. sativum, y que Burkholderia ubonensis y el hongo Trichoderma harzianum contribuyen eficazmente a la fijación biológica del nitrógeno, siendo los tres microorganismos muy importantes en la formulación de inoculantes para leguminosas.
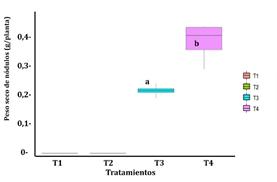
Figura 2. Peso seco de nódulos promedio en plantas de P. sativum según los tratamientos experimentales. T1 control negativo, T2 control positivo, T3 inoculante en soporte sólido y T4 inoculante en soporte líquido.
Nota: Prueba t-student (p = 0,003 < 0,05); Levene (p = 0,107 > 0,05) y Shapiro-Wilk en los tratamientos T3 y T4 (p = 0,7321 y p = 0,2456, respectivamente).
CONCLUSIONES
El inoculante microbiano multicepa en soporte sólido promovió significativamente el aumento del número y peso seco de los nódulos de P. sativum, debido a que favoreció la expansión de la longitud y masa de la raíz, por lo tanto, un mayor número de sitios activos para la nodulación.
AGRADECIMIENTOS
Al Instituto de Educación Superior Tecnológica Mache, Otuzco, La Libertad, por el apoyo en el manejo agronómico de cultivo de P. sativum. A la Estación Experimental Agraria Donoso – Huaral, Lima, por proporcionar la semilla certificada de P. sativum cultivar INIA-102 Usui. Al Laboratorio de Micología de la Universidad Nacional de Trujillo, por proporcionar el cultivo de Trichoderma harzianum. Al Laboratorio de rizobiología de la Universidad Nacional de Cajamarca por el cultivo de R. leguminosarum. Al laboratorio de suelos de la Universidad Nacional de San Martín Tarapoto por la cepa de Burkholderia ubonensis.
REFERENCIAS BIBLIOGRÁFICAS
Albareda, M.; Rodríguez-Navarro, D.; Camacho, M.; Temprano, F. 2008. Alternatives to peat as a carrier for rhizobia inoculants: solid and liquid formulations. Soil Biol Biochem 40(11): 2771–2779.
Bello, S., Yusuf, A.; Cargele, M. 2018. Performance of cowpea as influenced by native strain of rhizobia, lime and phosphorus in Samaru, Nigeria. Symbiosis 75: 167–176.
Boudjabi, S.; Kribaa, M.; Chenchouni, H. 2017. Sewage sludge fertilization alleviates drought stress and improves physiological adaptation and yield performances in durum wheat (Triticum durum): a double-edged sword. Journal King Saud Univ. Sci. 12: 1–9.
Brenner, D.; Krieg, N.; Staley, J.; Garrity, G. 2005. Bergey's Manual of Systematic Bacteriology. 2da Edition, vol. 2 (The Proteobacteria), parte C (The Alpha-, Beta-, Delta- y Epsilonproteobacteria). Editorial Springer. Nueva York. 875 pp.
Carrero-Carrón, I.; Rubio, M.; Niño‐Sánchez, J.; Navas‐Cortés, J.; Jiménez‐Díaz, R.; Monte, E.; Hermosa, R. 2018. Interactions between Trichoderma harzianum and defoliating Verticillium dahlia in resistant and susceptible wild olive clones. Plant Pathol 67: 1758–1767.
Chao, Y.; Bueckert, R.; Schoenau, J.; Diederichsen, A.; Zakeri, H.; Warkentin, T. 2017. Simbiosis de Rhizobium leguminosarum bv. cepas viciae con diversos genotipos de guisantes: efectos sobre la fijación biológica de nitrógeno. Canadian Journal of Microbiology 63: 909-919.
Contreras-Cornejo, H.; Macías-Rodríguez, A.; Cortés-Penagos, L.; López-Bucio, J. 2009. Trichoderma virens, a plant beneficial fungus, enhances bio-mass production and promotes lateral root growth through an auxin-dependent mechanism in Arabidopsis. Plant. Physiol. 149: 1579–1592.
De Smet, B.; Mayo, M.; Peeters, C.; Zlosnik, JE.; Spilker, T.; Hird, TJ.; et al. 2015. Burkholderia stagnalis sp. nov. y Burkholderia territorii sp. nov., dos nuevas especies complejas de Burkholderia cepacia de fuentes ambientales y humanas. International Journal of Systematic and Evolutionary Microbiology 65(7): 2265–2271.
Delić, D.; Stajkovi´c, O.; Rasuli´c, N.; Kuzmanovi´c, D.; Joši´c, D.; Miliˇci´c, B. 2010. Nodulation and N2 fixation effectiveness of Bradyrhizobium strains in symbiosis with adzuki bean, Vigna angularis. Brazilian Archives of Biology and Technology 53: 293–299.
Farid, M.; Navabi, A. 2015. N2 fixation ability of different dry bean genotypes. Canadian Journal of Plant Science 95: 1243–1257.
Kawaka, F.; Dida, M.; Opala, P.; Ombori, O.; Maingi, J.; Osoro, N.; Muthini, M.; Amoding, A.; Mukaminega, D.; Muoma, J. 2014. Symbiotic efficiency of native rhizobia nodulating common bean (Phaseolus vulgaris L.) in soils of Western Kenya. Int. Sch. Res. Notices 2014: 1–8.
Khan, N.; Tariq, M.; Ullah, K.; Muhammad, D.; Khan, I.; Rahatullah, K.; Ahmed, N.; Ahmed, S. 2014. The effect of molybdenum and iron on nodulation, nitrogen fixation, and yield of chickpea genotypes (Cicer arietinum L). IOSR J. Agric. Vet. Sci. 7: 63–79.
Klock, M.; Barrett, L.; Thrall, P.; Harms, K. 2015. La promiscuidad del huésped en las asociaciones de simbiontes puede influir en el establecimiento de le-guminosas exóticas y la colonización de nuevos rangos. Diversity and Distributions 21: 1193–1203.
Koskey, G.; Mburu, S.; Njeru, E.; Kimiti, J.; Ombori, O.; Maingi, J. 2017. Potential of native rhizobia in enhancing nitrogen fixation and yields of climbing beans (Phaseolus vulgaris L.) in contrasting environments of Eastern Kenya. Front. Plant Sci. 8: 1–12.
La Pierre, K.; Simms, E.; Tariq, M.; Zafar, M.; Porter, S. 2017. Las legumbres invasoras pueden asociarse con muchos mutualistas de legumbres nativas, pero generalmente no lo hacen. Ecol. Evol. 7: 8599–8611.
Lesueur, D.; Deaker, R.; Herrmann, L.; Bräu, L.; Jansa, J. 2016. The production and potential of biofertilizers to improve crop yields. In: Arora NK, Mehnaz S, Balestrini R (eds) Bioformulations: for sustainable agriculture. Editorial Springer. New Delhi. 71–92 pp.
Medeiros, H.; Vieira de Araújo, J.; Grassi de Freitas, L.; Castillo, P.; Rubio, M.; Hermosa, R.; Monte, E. 2017. Tomato progeny inherit resistance to the nematode Meloidogyne javanica linked to plant growth induced by the biocontrol fungus Trichoderma atroviride. Sci. Rep. 7: 40216.
Mendoza-Mendoza, A.; Zaid, R.; Lawry, R.; Hermosa, R.; Monte, E.; Horwitz, B.; Mukherjee, P. 2018. Molecular dialogues between Trichoderma and roots: role of the fungal secretome. Fungal Biol. Rev. 32: 62–85.
Ministerio de Agricultura y Riego. 2016. Leguminosas de grano: Semillas nutritivas para un futuro sostenible. Perú. Disponible en: https://clck.ru/N36Jn
Ouma, E.; Asango, A.; Maingi, J.; Njeru, E. 2016. Elucidating the potential of native rhizobial isolates to improve biological nitrogen fixation and growth of common bean and soybean in smallholder farming systems of Kenya. Int. J. Agron 2016: 1–7.
Panasiewicz, K.; Niewiadomska, A.; Sulewska, H.; Wolna-Maruska, A.; Borowiak, K.; Budka, A.; Ratajczak, K. 2019. The effect of sewage sludge and BAF inculant on plant condition and yield as well as biochemical and microbial activity of soil in willow (Salix viminalis L.) culture as an energy crop. J. Peer 7: 1–23.
Samolski, I.; Rincón, A.; Pinzón, L.; Viterbo, A.; Monte, E. 2012. The quid74 gene from Trichoderma harzianum has a role in root architecture and plant biofertilization. Microbiology 158: 129–138.
Somasegaran, P.; Hoben, H. 1994. Handbook for Rhizobia Methods in Legume-Rhizobium Technology. 1era Edition. Editorial Springer-Verlag New York, Inc. New York. 58-64 pp.
Singh, J.; Koushal, S.; Kumar, A.; Vimal, S.; Gupta, V. 2016. Microbial inoculants in sustainable agricultural productivity, Vol. II: functional application. Journal Frontiers in Microbiology 7: 2105.
Sulieman, S.; Tran, L. 2015. Fijación de nitrógeno en leguminosas en un entorno cambiante. 1era Edición. Editorial Springer International Publishing. Suiza. 5-33 pp.
Unkovich, M.; Baldock, J.; Peoples, M. 2010. Prospects and problems of simple linear models for estimating symbiotic N2 fixation by crop and pasture legumes. Plant Soil 329: 75–89.
Yedidia, I.; Benhamou, N.; Chet, I. 1999. Induction of defense responses in cu-cumber plants (Cucumis sativus L.) by the biocontrol agente Trichoderma harzianum. Appl. Environ. Microbiol. 65: 1061–1070.