Influencia
de bioestimulantes y aguas contaminadas en la morfología del girasol ornamental
Helianthus annuus L.
Influence of
biostimulants and contaminated water on the morphology of the ornamental
sunflower Helianthus annuus L.
Deyaneira Arévalo1, 2;
Alysson Pineda1, 2; Sayda Herrera-Reyes1, 2, *; Diego
Villaseñor-Ortiz1, 2;
Edison Jaramillo1, 2
1 Facultad de
Ciencias Agropecuarias, Universidad Técnica de Machala (UTMACH), Granja experimental
Santa Inés, Av. Panamericana, Machala, Ecuador.
2 Semillero estudiantil de
investigación en Fitotecnia (SINFIT), UTMACH, Granja experimental Santa Inés,
Machala. Ecuador.
*
Autor corresponsal: sherrera@utmachala.edu.ec (S. Herrera-Reyes).
ID
ORCID de los autores
D.
Arévalo:  https://orcid.org/0000-0001-9168-6295 A.
Pineda:
https://orcid.org/0000-0001-9168-6295 A.
Pineda:  https://orcid.org/0009-0009-6332-7143
https://orcid.org/0009-0009-6332-7143
S.
Herrera-Reyes:  https://orcid.org/0000-0002-7226-5345 D.
Villaseñor-Ortiz:
https://orcid.org/0000-0002-7226-5345 D.
Villaseñor-Ortiz:  https://orcid.org/0000-0001-5646-4451
https://orcid.org/0000-0001-5646-4451
E.
Jaramillo:  https://orcid.org/0000-0002-8241-9598
https://orcid.org/0000-0002-8241-9598
RESUMEN
Los bioestimulantes y las aguas influyen en
el desarrollo del cultivo, por esta razón se planteó el objetivo evaluar la influencia
de bioestimulantes y agua contamina en la morfología del girasol ornamental. Realizadas
las pruebas estadísticas sobre las variables morfológicas se determinó que si
existieron diferencias significativas entre las variables determinadas por el
ANOVA, donde las variables largo de planta, número de hojas, distancia entre
nudos, pedúnculo, masa de raíz, masa de planta en freso y masa de planta en
fresco presentaron diferencia significativas entre los grupos; contrario a las
variables diámetro del tallo, ancho de hojas y largo de las hojas donde no se
presentaron diferencias significativas. El tratamiento con el bioestimulante Algaser
(Algas marinas) presentaron las diferencias significativas (α = 0,05) más importantes
dentro del estudio, seguido por el tratamiento con agua destilada, Rady max
(Aminoácidos + Fertilizante inorgánico) y Flizz (Aminoácidos) el agua de canal
en todas las variables morfológicas presento las medias más bajas entre los
tratamientos. Se demostró que los bioestimulantes y la calidad del agua tienen
un impacto significativo en el desarrollo morfológico del girasol ornamental.
Palabras
clave:
fitorreguladores;
estimulantes de crecimiento; morfología; raíces.
ABSTRACT
Bio-stimulants and water quality influence crop
development. Therefore, the objective was to assess the influence of
bio-stimulants and contaminated water on the morphology of ornamental
sunflowers. Statistical tests revealed significant differences among variables,
such as plant height, leaf number, internode distance, peduncle length, root
mass, fresh plant mass, and stem diameter. The Algaser bio-stimulant (seaweed)
exhibited the most significant differences (α = 0.05), followed by
distilled water, Rady max (amino acids + inorganic fertilizer), and Flizz
(amino acids). Canal water consistently resulted in the lowest means for all
morphological variables. This study demonstrates that bio-stimulants and water
quality play a significant role in the morphological development of ornamental
sunflowers.
Keywords: phyto-regulators; growth
stimulants; morphology; roots.
Recibido: 24-02-2023.
 Aceptado: 28-05-2023.
Aceptado: 28-05-2023.
El girasol también conocido con el nombre científico Helianthus
annuus L, es una planta oleaginosa nativa de América del Norte, que posee
múltiples propiedades antioxidantes que benefician al ser humano, así mismo
tiene la capacidad de absorber cationes del suelo e inclusive metales como el
plomo y cadmio, que ayudan a la biorremediación de los suelos (Bravo Delgado
& Días López, 2021; Rodríguez Guzmán et al., 2021). En la actualidad existe
un incremento del cultivo del girasol a nivel mundial, dado que de su semilla
se elaboran varios productos necesarios para la sociedad, tales como aceites,
cosméticos, perfumes, jabones, medicinas, etc. (de
Lima Franzen et al., 2019).
Ecuador ocupa menos del 1% de la superficie terrestre,
a pesar de ello, este pequeño país cuenta con una de las mayores
biodiversidades del mundo. Ecuador alberga la mitad de las 3.000 especies de
aves de Sudamérica, el 10% de las especies vegetales del mundo y es el mayor
productor y exportador mundial de banano (Sawers,
2005). Este país alberga más de 100 especies de flores tropicales de una
amplia gama de colores y más de 4.000 especies de orquídeas. Miles de flores
crecen silvestres en el país, pero la flor no autóctona más conocida es la
rosa. Las rosas ecuatorianas son conocidas por ser las mejores del mundo en
todas las categorías, incluidos el tamaño de la flor, la longitud del tallo, la
duración en el jarrón y el color (Castro et al.,
2020).
La industria ecuatoriana de la rosa es una cadena de
producción gestionada por varias entidades que aportan recursos materiales e
inmateriales. Sin embargo, pocas empresas de cultivo pueden centrarse también
en proporcionar variedades de plantas con mutaciones culturalmente controladas,
basadas en los conocimientos tradicionales de la comunidad de cultivadores y de
las personas que trabajan en las plantaciones de flores del país (Arcos &
Carrera, 2023).
En la Provincia de El Oro, el cultivo del girasol se
realiza tradicionalmente con productos químicos como fertilizantes y
herbicidas, mismos que con el pasar del tiempo dañan los suelos y calidad del
producto (Vásquez López et al., 2021). Es así,
que existe una limitada utilización de métodos orgánicos como los
fitorreguladores, para controlar el rendimiento, crecimiento y desarrollo del girasol;
puesto que generalmente se utiliza esta herramienta orgánica en cultivos de
banano, maracuyá, hortalizas, entre otros. Al utilizar fitorreguladores en el
girasol, se mejora los procesos fisiológicos de la planta, se reduce el daño al
suelo y puede reducir las pérdidas de la cosecha al garantizar un desarrollo
adecuado de las semillas.
En todo caso hay que tomar en cuenta que, para el
cultivo del girasol, el uso de fertilizantes minerales es uno de los
principales factores del aumento del rendimiento. Es importante alimentar al
girasol de acuerdo con sus necesidades, de modo que se pueda conseguir una alta
calidad y rendimiento si se presta mucha atención a la cantidad y duración de
las aplicaciones de fertilizantes minerales (Mahmood
et al., 2022).
Las cambiantes condiciones climáticas, combina-das con
la contaminación, han provocado diversos estreses abióticos en los cultivos,
incluido el girasol, que afectan a su calidad y rendimiento, la sinergia que
producen los bioestimulantes favorecen la nutrición de los cultivos (Antón‐Herrero et al., 2022). Entre los
estreses abióticos, la salinidad ha afectado a la producción de girasol en
varios países. Los estudios han descubierto que el girasol tiene una tolerancia
media a la sal, tolerando un nivel umbral de CE (2,5 dS/m), pero cuando se
supera este nivel, las pérdidas de rendimiento alcanzan el 30% o más. Los
principales efectos de la toxicidad del NaCl se producen en el contenido de
aceite del cultivo, la biomasa vegetal, la salud de las hojas, la longitud de
las raíces y los brotes y la actividad fotosintética (Fatima & Arora, 2021).
En cuanto a los bioestimulantes existen algunas
formulaciones de diferentes ingredientes, dividido en tres categorías,
dependiendo del tipo de fuente incluidas en este caso las sustancias húmicas
(HS), compuesto con hormonas (HCP) y otros que contienen aminoácidos (ACP). Las
sustancias húmicas, y otros como los extractos vegetales de algas marinas,
tiene varias sustancias como auxinas, citoquininas o derivados de estas (du Jardin, 2015), otras alternativas son los hongos
endófitos las cuales actúan bajo una sinergia positiva que pueden ser
utilizadas por la agroindustria (Hung et al., 2023).
Los reguladores del crecimiento de las plantas no
sustituyen a los fertilizantes minerales, sino que los complementan en el
sistema de nutrientes de las plantas y aumentan la utilización del suelo y los
fertilizantes. Para conseguir altos rendimientos de girasol y generar altos
rendimientos y beneficios, es necesario utilizar los últimos avances
científicos y las tecnologías innovadoras de las explotaciones experimentales
avanzadas (Spring et al., 2020). Los efectos
de los fitorreguladores pueden potenciar la eficacia de los plaguicidas
aplicados a las semillas y durante el periodo vegetativo.
Una nueva dirección para mejorar la tecnología de
producción del girasol es el desarrollo de sistemas que utilicen eficazmente
los modernos reguladores del crecimiento vegetal que controlan todas las fases
del crecimiento y desarrollo de la planta, activan la inmunidad de la planta y,
en consecuencia, controlan todas las fases de la producción para mejorar el
rendimiento y la calidad de las semillas de girasol. Por lo tanto, el
desarrollo de tecnologías para aplicar bioestimulantes al girasol con el fin de
regular su crecimiento y mejorar su inmunidad es de suma importancia (Kovaliova et al., 2020).
Por tal motivo, se planteó el objetivo de analizar los
fitorreguladores orgánicos mediante investigación experimental y búsqueda en
fuentes bibliográficas para la determinación de su influencia en el crecimiento
y desarrollo en el cultivo de girasol ornamental.
Área de estudio
El
estudio se realizó en la Granja
Experimental Santa Inés de la Facultad de Ciencias Agropecuarias, perteneciente
a la Universidad Técnica de Machala. La zona de estudio se encuentra ubicada
geográficamente en las coordenadas 3°15’52.29 S, 79°57’4.3 W en el cantón
Machala, dentro de la provincia de El Oro, Ecuador. En cuanto al régimen de
precipitación o de lluvias esta se divide dentro de dos periodos; con un
periodo lluvioso de diciembre a mayo, una precipitación media anual de 1250 mm
y una temperatura media anual que oscila entre 24 y 26 °C (Luna-Romero et al., 2018).
Material vegetal
El material vegetal fue un hibrido F1 de Girasol de la
empresa SAKATA SEED AMERICA, INC. De semillas certificadas con una pureza del
99,94%.
Manejo del Ensayo
Fase 1: germinación de las semillas (se evaluó in
vitro en cajas de Petri, hasta que las semillas tuvieran dos hojas de los
cotiledones iniciales).
Fase 2: se llevaron a semillero por 15 días para luego
ser llevado a maceteros plásticos en forma convencional de rizotrones para la
observación periódica del desarrollo de raíces.
Diseño del experimento
Se utilizó
un diseño experimental completamente aleatorizado (Festing, 2020), con 5 tratamientos y 6 repeticiones (30 unidades
experimentales (Figura 1). El experimento midió 10 m de ancho y 5 m de largo,
cuyo producto equivale al área bruta (50 m2). La aplicación de los
bioestimulantes se realizó todas con agua bidestilada y los valores de
disolución fueron calculado de acuerdo con las especiaciones de los productos.
Variables respuesta
Las variables evaluadas en el estudio fueron: Altura de
planta la cual fue medida en cada parcela con ayuda de una cinta métrica,
tomada desde la corona radical hasta la yema apical en el vástago principal de
la planta. El número de hojas se cuantificó manualmente dentro de cada unidad
experimental. El diámetro del tallo, se registró sus unidades en mm con ayuda
de un calibrador Vernier. El largo y ancho de la hoja la cual fue medida con
ayuda de una cinta métrica en 5 hojas de la parte media de la planta. La
longitud de raíces fue medida con una cinta métrica en unidades de cm, desde el
cuello hasta la cofia.
La masa fresca se tomó con ayuda de una balanza
analítica, como la masa de la raíz y la masa seca de la planta se obtuvo por
diferencia de peso, para ello se llevaron las muestras al laboratorio se suelos
de la Facultad de Ciencias Agropecuarias (Universidad Técnica de Machala) donde
se colocaron en una estufa a 70 °C por 24 horas y luego se procedió a pesar.
Las muestras fueron extraídas de la estufa y colocadas en un desecador, luego
se volvieron a pesar, obteniendo la masa seca por diferencia de peso.
Análisis estadístico
Se realizó para el estudio un análisis de varianza de
una sola vía para todas las variables de estudio y la comparación múltiple de
medias utilizando la prueba de Tukey con un nivel de significancia del 95%
(α = 0.05). Los datos estadísticos fueron procesados dentro del programa
estadístico IBM SPPS Statistics versión 25.
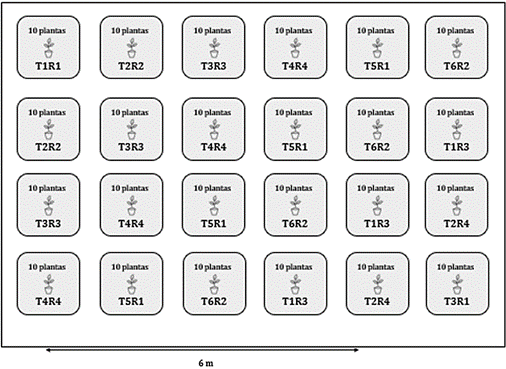
Figura 1. Bosquejo del diseño experimental del
estudio.
Los resultados del estudio
indican que hubo diferencias significativas en varias variables morfológicas
evaluadas mediante pruebas estadísticas ANOVA. Las variables como el largo de
planta, número de hojas, distancia entre nudos, pedúnculo, masa de raíz, masa
de planta en freso y masa de planta en fresco mostraron diferencias
significativas entre los grupos.
En contraste, las variables
diámetro del tallo, ancho de hojas y largo de las hojas no presentaron
diferencias significativas. El diámetro del tallo se mantuvo en un rango de 6 a
7 cm, mientras que el largo y ancho de las hojas oscilaron alrededor de 10 cm y
6 cm, respectivamente.
En cuanto al largo de la
planta, se observaron diferencias significativas entre los diferentes
tratamientos (Figura 2). El tratamiento con Algaser (Algas marinas) mostró la
media más alta, con 41,5 cm, seguido por el agua destilada con 40,5 cm, Rady
max (Aminoácidos + Fertilizante inorgánico) con una media de 39,38 cm, Flizz
(Aminoácidos) con medias de 36,2 cm y, por último, el agua de canal con la
media más baja de altura, 32,88 cm. Estos resultados indican que el uso de
Algaser como bioestimulante tuvo un impacto significativo en el crecimiento y
desarrollo de las plantas de girasol, ya que se obtuvo la mayor altura
promedio. Además, el agua de canal mostró un efecto negativo en el crecimiento
de las plantas, ya que presentó la media más baja.
Estos hallazgos resaltan la
importancia de seleccionar adecuadamente los bioestimulantes y el tipo de agua
utilizados en la producción de girasoles ornamentales, ya que pueden tener un
impacto significativo en su morfología y crecimiento (Yuldasheva
& Karabayeva, 2023).
Los resultados
revelan que hubo diferencias significativas en el número de hojas entre los
diferentes tratamientos evaluados (Figura 3). Tanto el agua destilada como el
bioestimulante Algaser (Algas marinas) mostraron las medias más altas, con un
promedio de 17 hojas completas. El tratamiento con Rady max (Aminoácidos +
Fertilizante inorgánico) también tuvo un promedio relativamente alto, con 16
hojas. Por otro lado, los tratamientos con Flizz (Aminoácidos) y agua de canal
tuvieron medias más bajas, con 14 y 13 hojas respectivamente.
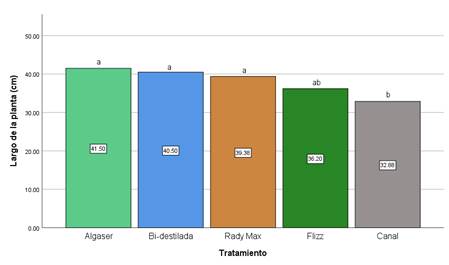
Figura 2. Media para la
variable largo de la planta.
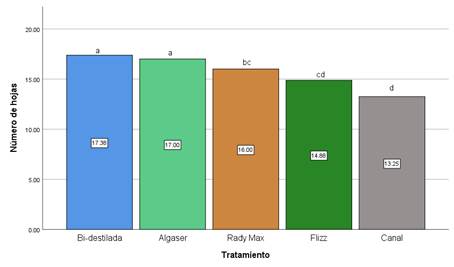
Figura 3. Media para la variable número de hojas.
Estos resultados
sugieren que el uso de agua destilada y el bioestimulante Algaser pueden
favorecer el crecimiento y desarrollo de un mayor número de hojas en las
plantas de girasol. Por otro lado, el uso de Flizz y agua de canal puede tener
un impacto menos favorable en la producción de hojas.
Es importante
destacar que el número de hojas es un indicador importante del vigor y la salud
de las plantas (Mystkowska & Dmitrowicz, 2023). Un
mayor número de hojas generalmente se asocia con un mejor crecimiento y una
mayor capacidad fotosintética. Por lo tanto, estos resultados resaltan la
importancia de seleccionar cuidadosamente los tratamientos adecuados para
promover un desarrollo óptimo de las plantas de girasol.
Los resultados
indicaron diferencias significativas en la distancia entre nudos de los
tratamientos evaluados (Figura 4). El tratamiento con agua bidestilada presentó
la menor elongación entre nudos, con un promedio de 5,60 cm. Por otro lado, el
tratamiento con Flizz (Aminoácidos) mostró la mayor distancia entre nudos, con
un promedio de 7,12 cm. Los tratamientos con Algaser (Algas marinas), Rady max
(Aminoácidos + Fertilizante inorgánico) y agua de canal tuvieron valores
intermedios de 6,30 cm, 5,88 cm y 5,63 cm, respectivamente. Estos resultados
destacan que los tratamientos utilizados influyeron en la elongación entre
nudos de las plantas de girasol (Santos et al., 2019).
Los resultados
revelaron que el largo del pedúnculo varió significativamente entre los
diferentes tratamientos evaluados (Figura 5). El tratamiento con Algaser (Algas
marinas) mostró la media más alta, con un promedio de 7,38 cm. El agua
bidestilada presentó un promedio de 6,73 cm, seguido por Flizz (Aminoácidos)
con 6,26 cm y Rady max (Aminoácidos + Fertilizante inorgánico) con 5,56 cm. Por
último, el agua de canal tuvo la media más baja de largo de pedúnculo, con 3,63
cm.
Estos resultados
indican que los diferentes tratamientos tuvieron un impacto significativo en la
longitud del pedúnculo de las plantas de girasol. El uso de Algaser (Algas
marinas) y agua bidestilada promovió un mayor desarrollo en esta variable,
mientras que el agua de canal mostró los valores más bajos.
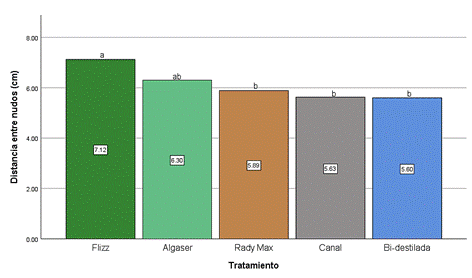
Figura 4. Medias para el
diámetro del tallo.
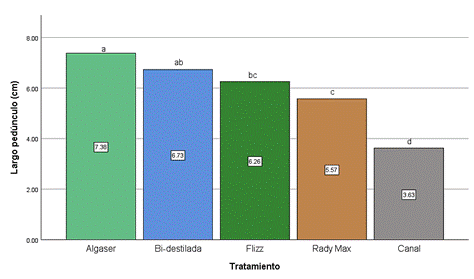
Figura 5. Media para la
variable largo del pedúnculo.
El largo del
pedúnculo es un factor importante en la calidad y apariencia de las flores, ya
que determina la altura de la flor en relación con el tallo. Estos hallazgos
destacan la importancia de seleccionar adecuadamente los tratamientos para
lograr un desarrollo óptimo del pedúnculo en el cultivo de girasoles
ornamentales (Parađiković et al., 2019).
Los resultados
revelaron diferencias significativas en la masa de la planta en seco entre los
tratamientos evaluados (Figura 6). El tratamiento con Algaser (Algas marinas)
mostró la media más alta, con un promedio de 4,48 g. Flizz (Aminoácidos) tuvo
una media de 3,38 g, mientras que el tratamiento con agua bidestilada presentó
una media de 3,03 g. Rady max (Aminoácidos + Fertilizante inorgánico) mostró
una media de 2,98 g y el agua de canal tuvo las medias más bajas en todas las
variables, con 2,8 g. Estos resultados indican que los tratamientos tuvieron un
impacto significativo en la masa de la planta en seco de las plantas de
girasol. El uso de Algaser (Algas marinas) promovió un mayor crecimiento en
esta variable, seguido por Flizz y el agua destilada. Por otro lado, el agua de
canal mostró los valores más bajos de masa de planta en seco. La masa de la
planta en seco es un indicador importante de la producción de biomasa y puede
reflejar el desarrollo y la salud general de las plantas. Estos hallazgos
resaltan la importancia de seleccionar los tratamientos adecuados para promover
un crecimiento óptimo y una mayor masa de la planta en el cultivo de girasoles
ornamentales.
Los resultados
muestran diferencias significativas en la masa de la raíz entre los
tratamientos evaluados (Figura 7). El tratamiento con Algaser (Algas marinas)
obtuvo la media más alta, con un promedio de 6,25 g. El agua bidestilada
presentó una media de 4,6 g, seguida de Flizz (Aminoácidos) con 4,24 g. Por
último, el agua del canal mostró la media más baja en todas las variables, con
2,8 g. Estos hallazgos indican que el tratamiento con Algaser favoreció un
mayor desarrollo y crecimiento de las raíces en comparación con los demás
tratamientos. El agua bidestilada también mostró un efecto positivo en la masa
de la raíz, seguida de cerca por el tratamiento con Flizz. En contraste, el
agua del canal tuvo un impacto menos favorable en el crecimiento de las raíces,
reflejado en su menor masa promedio. La masa de la raíz es un indicador clave
del sistema radicular de las plantas y puede tener implicaciones importantes en
su absorción de nutrientes y estabilidad. Estos resultados resaltan la
importancia de seleccionar adecuadamente los tratamientos que promuevan un
desarrollo saludable de las raíces, lo cual puede tener un impacto
significativo en el crecimiento y rendimiento general de los girasoles ornamentales
(Montoneri et al., 2022).
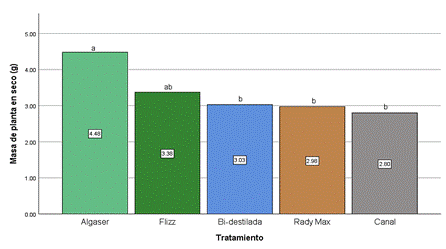
Figura 6. Media para masa
planta en seco.
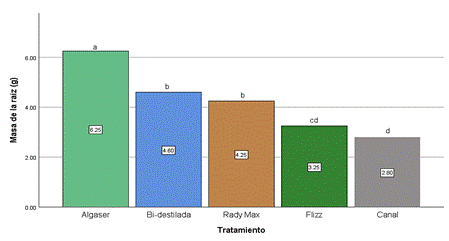
Figura 7. Media para la
variable masa de raíz.
Los resultados
mostraron diferencias significativas en la masa de la planta en fresco entre
los tratamientos (Figura 8). El tratamiento con Algaser (Algas marinas) obtuvo
la media más alta, con un promedio de 43,15 g. El agua bidestilada presentó una
media de 35,2 g, seguido de Flizz (Aminoácidos) con 33,05 g, y Rady max
(Aminoácidos + Fertilizante inorgánico) con 31,64 g. El agua del canal mostró
la media más baja en todas las variables, con 23,75 g.
Estos hallazgos
indican que los tratamientos tuvieron un impacto significativo en la masa de la
planta en fresco de los girasoles ornamentales. El uso de Algaser (Algas
marinas) resultó en una mayor masa de planta, seguido del agua bidestilada. Los
tratamientos con Flizz y Rady max también mostraron una masa de planta
considerable, mientras que el agua del canal presentó los valores más bajos (Funes-Pinter et al., 2023; Loconsole et al., 2023) .
La masa de la planta en fresco es un parámetro importante que refleja el
crecimiento y desarrollo general de las plantas. Estos resultados destacan la importancia
de seleccionar tratamientos adecuados para promover una mayor masa de planta en
fresco en el cultivo de girasoles ornamentales (Kisvarga
et al., 2022).
Los resultados
revelaron que los valores de pH y CE (conductividad eléctrica) en el cultivo
variaron entre los diferentes tratamientos. El tratamiento con agua bidestilada
mostró un pH de 6,91 y una CE de 1,30. El agua del canal presentó un pH de 6,75
y una CE de 1,71. Rady max (Aminoácidos + Fertilizante inorgánico) tuvo un pH
de 6,72 y una CE de 1,51. Algaser (Algas marinas) mostró un pH de 6,61 y una CE
de 1,62. Finalmente, Flizz (Aminoácidos) tuvo un pH de 6,59 y una CE de 1,65.
Estos resultados
indican que los diferentes tratamientos afectaron los valores de pH y CE en el
cultivo de girasoles ornamentales. El agua bidestilada presentó un pH
ligeramente más alto, seguida por el agua del canal, Rady max, Algaser y Flizz.
En términos de CE, el agua del canal mostró el valor más alto, seguida por
Algaser, Flizz, Rady max y agua bidestilada.
El pH y la CE
son factores importantes que pueden influir en la disponibilidad de nutrientes
y en la salud de las plantas. Estos hallazgos resaltan la importancia de
monitorear y ajustar adecuada-mente los niveles de pH y CE en el cultivo de
girasoles ornamentales para favorecer un ambiente óptimo para el crecimiento y
desarrollo de las plantas.
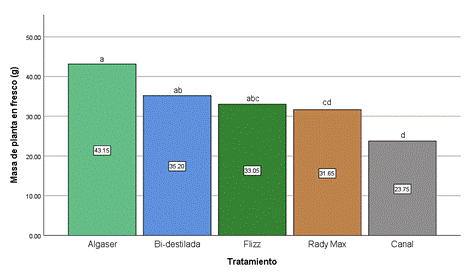
Figura 8. Media masa de la
planta fresca.
El tratamiento con el
bioestimulante Algaser (Algas marinas) presentaron las diferencia
significativas (α = 0,05) más importantes dentro del
estudio, seguido por el tratamiento con agua destilada, Rady max (Aminoacidos +
Fertilizante inorganico) y Flizz (Aminoacidos), el agua de canal en todas las
variables morfológicas presento las medias más bajas entre los tratamientos en
este sentido se corrobora la influencia positiva de los bioestimulantes sobre
el cultivo los valores de pH en el suelo y Ce demostraron que los tratamiento
con el bioestimulante se mantuvieron dentro de los mismos rangos aunque Flizz
(Aminoacidos) presento el pH más acido con relación al agua bidestilada que
presento los valores más neutros. Se recomienda realizar estudios
futuros para investigar más a fondo los efectos de diferentes bioestimulantes y
tratamientos de agua en el cultivo de girasoles ornamentales. Estos estudios
podrían enfocarse en analizar parámetros adicionales, como el contenido de
nutrientes en las plantas, la resistencia a enfermedades y la producción de
flores. Además, sería beneficioso explorar el uso de otros bioestimulantes
naturales y evaluar su efectividad en comparación con Algaser. Estas
investigaciones proporcionarán una mayor comprensión de las mejores prácticas
agrícolas para el cultivo exitoso de girasoles ornamentales.
REFERENCIAS
BIBLIOGRÁFICAS
Antón‐Herrero, R., Vega‐Jara, L.,
García‐Delgado, C., Mayans, B., Camacho‐Arévalo, R.,
Moreno‐Jiménez, E., Plaza, C., & Eymar, E. (2022). Synergistic effects of
biochar and biostimulants on nutrient and toxic element uptake by pepper in
contaminated soils. Journal of the Science of Food and Agriculture, 102(1),
167–174. https://doi.org/10.1002/jsfa.11343
Arcos,
C., & Carrera, A. (2023). Obstacles to Innovative Activities: Case of
the Floriculture Sector in Ecuador (pp. 67–94).
https://doi.org/10.1007/978-3-031-17960-0_4
Bravo Delgado, H. R., & Días López, E. (2021).
Variabilidad genética en raíz de girasol mediante gamma de 60Co. Revista
Mexicana de Ciencias Agrícolas, 12(3), 461–472.
https://doi.org/10.29312/remexca.v12i3.2597
Castro, C., Castañeda, Z., Ruiz, K. R., González, G., &
Poveda, G. (2020). El sector florícola ecuatoriano y su afectación en el
mercado internacional producto de la pandemia causada por el Covid-19. In
CONGRESO INTERNACIONAL VIRTUAL SOBRE COVID-19.
de Lima Franzen, F., Rodrigues de Oliveira, M. S., Lidório, H.
F., Farias Menegaes, J., & Martins Fries, L. L. (2019). Composición química
de pétalos de flores de rosa, girasol y caléndula para su uso en la
alimentación humana. Ciencia y Tecnología Agropecuaria, 20(1).
https://doi.org/10.21930/rcta.vol20_num1_art:1252
du
Jardin, P. (2015). Plant biostimulants: Definition, concept, main categories
and regulation. Scientia Horticulturae, 196, 3–14.
https://doi.org/10.1016/j.scienta.2015.09.021
Fatima, T., & Arora, N. K. (2021). Pseudomonas entomophila PE3
and its exopolysaccharides as biostimulants for enhancing growth, yield and
tolerance responses of sunflower under saline conditions. Microbiological
Research, 244, 126671. https://doi.org/10.1016/j.micres.2020.126671
Festing,
M. F. W. (2020). The “completely randomised” and the “randomised block” are the
only experimental designs suitable for widespread use in pre-clinical research.
Scientific Reports, 10(1), 17577. https://doi.org/10.1038/s41598-020-74538-3
Funes-Pinter,
I., Pisi, G., Aroca, M., & Uliarte, E. M. (2023). Compost tea and bioslurry
as plant biostimulants. Part 2: biofertilizer test in ornamental flowers. Journal
of Plant Nutrition, 1–12. https://doi.org/10.1080/01904167.2023.2171883
Hung,
S.-H. W., Huang, T.-C., Lai, Y.-C., Wu, I.-C., Liu, C.-H., Huarng, Y.-F.,
Hwang, H.-H., Chiang, E.-P. I., Kuo, C.-H., & Huang, C.-C. (2023).
Endophytic Biostimulants for Smart Agriculture: Burkholderia seminalis 869T2
Benefits Heading Leafy Vegetables In-Field Management in Taiwan. Agronomy,
13(4), 967. https://doi.org/10.3390/agronomy13040967
Kisvarga,
S., Farkas, D., Boronkay, G., Neményi, A., & Orlóci, L. (2022). Effects of
Biostimulants in Horticulture, with Emphasis on Ornamental Plant Production. Agronomy,
12(5), 1043. https://doi.org/10.3390/agronomy12051043
Kovaliova,
O., Tchoursinov, Y., Kalyna, V., Koshulko, V., Kunitsia, E., Chernukha, A.,
Bezuglov, O., Bogatov, O., Polkovnychenko, D., & Grigorenko, N. (2020).
Identification of patterns in the production of a biologically-active component
for food products. Eastern-European Journal of Enterprise Technologies, 2(11
(104)), 61–68. https://doi.org/10.15587/1729-4061.2020.200026
Loconsole, D., Cristiano, G., & De Lucia, B. (2023). Biostimulant Application,
under Reduced Nutrient Supply, Enhances Quality and Sustainability of
Ornamental Containerized Transplants. Agronomy, 13(3), 765.
https://doi.org/10.3390/agronomy13030765
Luna-Romero, A., Ramírez, I., Sánchez, C., Conde, J., Agurto,
L., & Villaseñor, D. (2018). Spatio-temporal distribution of precipitation in
the Jubones river basin, Ecuador: 1975-2013. Scientia Agropecuaria, 9(1),
63–70. https://doi.org/10.17268/sci.agropecu.2018.01.07
Mahmood,
A., Awan, M. I., Sadaf, S., Mukhtar, A., Wang, X., Fiaz, S., Khan, S. A., Ali,
H., Muhammad, F., Hayat, Z., Gul, F., & Fahad, S. (2022). Bio-diesel
production of sunflower through sulphur management in a semi-arid subtropical
environment. Environmental Science and Pollution Research, 29(9),
13268–13278. https://doi.org/10.1007/s11356-021-16688-z
Montoneri,
E., Baglieri, A., & Fascella, G. (2022). Biostimulant Effects of Waste
Derived Biobased Products in the Cultivation of Ornamental and Food Plants. Agriculture,
12(7), 994. https://doi.org/10.3390/agriculture12070994
Mystkowska,
I., & Dmitrowicz, A. (2023). Evaluation of the Effect of Biostimulants on
Palatability and Flesh Darkening of Raw and Cooked Tubers of
<i>Helianthus tuberosus</i> Journal of
Ecological Engineering, 24(6), 119–128.
https://doi.org/10.12911/22998993/162783
Parađiković,
N., Teklić, T., Zeljković, S., Lisjak, M., & Špoljarević, M.
(2019). Biostimulants research in some horticultural plant species—A review. Food
and Energy Security, 8(2), e00162. https://doi.org/10.1002/fes3.162
Rodríguez Guzmán, E., Espino, A. A., Barrios, E. P., García,
J. M. P., & Rodríguez, L. J. A. (2021). Evaluación del vigor híbrido en
cruzas de girasol (Helianthus annuusL.) con líneas tempranas s1 de bajo
contenido de aceite. Acta Universitaria, 31, 1–16.
https://doi.org/10.15174/au.2021.2905
Santos, P. L. F. dos, Zabotto, A. R., Jordão, H. W. C., Boas,
R. L. V., Broetto, F., & Tavares, A. R. (2019). Use of seaweed-based
biostimulant (Ascophyllum nodosum) on ornamental sunflower seed germination and
seedling growth. Ornamental Horticulture, 25(3), 231–237.
https://doi.org/10.1590/2447-536x.v25i3.2044
Sawers,
L. (2005). Nontraditional or New Traditional Exports: Ecuador’s Flower Boom. Latin
American Research Review, 40(3), 40–67.
http://www.jstor.org/stable/3662821
Spring,
O., Schmauder, K., Lackus, N. D., Schreiner, J., Meier, C., Wellhausen, J.,
Smith, L. v., & Frey, M. (2020). Spatial and developmental synthesis of
endogenous sesquiterpene lactones supports function in growth regulation of
sunflower. Planta, 252(1), 2.
https://doi.org/10.1007/s00425-020-03409-y
Vásquez López, B. E., Quevedo Guerrero, J. N., & García
Batista, R. M. (2021). Análisis de la proyección de las exportaciones de
camarón del Ecuador. Revista
Científica Agroecosistemas, 9(3), 74–83.
Yuldasheva,
Z. F., & Karabayeva, D. J. (2023). The effect of different doses of
different biostimulants on the yield of oily sunflower. IOP Conference
Series: Earth and Environmental Science, 1142(1), 012097.
https://doi.org/10.1088/1755-1315/1142/1/012097
![]() https://orcid.org/0000-0001-9168-6295 A.
Pineda:
https://orcid.org/0000-0001-9168-6295 A.
Pineda: ![]() https://orcid.org/0009-0009-6332-7143
https://orcid.org/0009-0009-6332-7143![]() https://orcid.org/0000-0002-7226-5345 D.
Villaseñor-Ortiz:
https://orcid.org/0000-0002-7226-5345 D.
Villaseñor-Ortiz: ![]() https://orcid.org/0000-0001-5646-4451
https://orcid.org/0000-0001-5646-4451![]() https://orcid.org/0000-0002-8241-9598
https://orcid.org/0000-0002-8241-9598