![]()
Esta obra está publicada bajo la licencia CC BY 4.0
INTRODUCCIÓN
Biodiversidad de árboles de mangle en el manglar de Puerto Pizarro, Tumbes, Perú
Biodiversity of mangrove trees in the Puerto Pizarro mangrove forest, Tumbes, Peru
Marco A. Zapata-Cruz1, 4; Ramón García Seminario 2; Auberto Hidalgo Mogollón3;
Enedia G. Vieyra-Peña3; Héctor Sánchez Suárez2; Alberto Ordinola-Zapata3, 4, *
1 Escuela de Posgrado, Universidad Nacional de Tumbes. Ciudad Universitaria, Av. Universitaria S/N, Tumbes, Perú.
2 Facultad de Ciencias Agrarias, Universidad Nacional de Tumbes. Fundo La Cruz S/N, La Cruz, Perú.
3 Facultad de Ingeniería Pesquera y Ciencias del Mar, Universidad Nacional de Tumbes. Calle Los Ceibos S/N, Puerto Pizarro, Perú.
4 Grupo de Investigación en Biodiversidad en Ecosistemas Acuáticos Tropicales (BioTrop), Universidad Nacional de Tumbes. Calle Los Ceibos S/N, Puerto Pizarro, Perú.
* Autor corresponsal: aordinolaz@untumbes.edu.pe (A. Ordinola-Zapata).
ID ORCID de los autores:
M. Zapata: https://orcid.org/0000-0002-9018-280X
R. García: https://orcid.org/0000-0003-0756-0935
A. Hidalgo: https://orcid.org/0000-0003-2921-4523
E. Vieyra-Peña: https://orcid.org/0000-0001-6541-7075
H. Sánchez-Suárez: https://orcid.org/0000-0003-2395-5056
A. Ordinola-Zapata: https://orcid.org/0000-0002-9644-0531
RESUMEN
El objetivo de la investigación fue determinar la diversidad alfa y beta de los árboles de mangle en el manglar de Tumbes. El área del manglar se dividió en tres zonas: A, B y C, en ellas se tomaron 41 puntos de muestreo (PM). Se contaron y midieron los árboles de mangle y se determinaron los índices de diversidad alfa: Shannon-Wiener (H’), Simpson (DS) y Pielou (J’), así como la similitud de los PM. La diversidad beta se determinó con los índices: de Jackard (IJ) y cuantitativo de Sorensen (S). Se determinó que la diversidad alfa del manglar fue baja (H’=1,0260, DS=0,6158 y J’=0,9339), siendo la zona A la de menor diversidad (H’=0,3048, DS=0,8531 y J’=0,2774), por su menor impacto antrópico y por el dominio de Rhizophora mangle sobre las otras especies, se observó que los PM fueron muy similares dentro de cada zona, con menor diversidad en la zona A. La diversidad beta evaluada mediante IJ fue de 1, indicando que la diversidad de especies no cambia entre las zonas, en tanto que el índice S mostró que hay un mayor cambio en diversidad entre la zona A y las restantes zonas. Estos resultados pueden permitir a las autoridades locales y regionales tomar decisiones a fin de poder proteger a dicho manglar. Por otro lado, también sería conveniente realizar investigación para determinar el impacto que la alteración de la biodiversidad de las especies de mangles pueda tener en los organismos que habitan en este manglar.
Palabras clave: Avicenia germinans; Laguncularia racemosa; mangle rojo; riqueza de especies; similitud.
ABSTRACT
The aim of this research was to determine the alpha and beta diversity of mangrove trees in the Tumbes mangrove forest. The mangrove forest area was divided into three zones: A, B and C, in which 41 sampling points (PM) were taken. Mangrove trees were counted and measured, and the alpha diversity indices were determined: Shannon-Wiener (H'), Simpson (DS) and Pielou (J’), as well as the similarity of the PM. Beta diversity is determined with the indices: Jackard (IJ) and quantitative Sorensen (S). It is considered that the alpha diversity of the mangrove forest was low (H'=1.0260, SD =0.6158 and J’=0.9339), with zone A being the one with the lowest diversity (H'=0.3048, SD=0.8531 and J’=0.2774), due to its less anthropic impact and due to the dominance of Rhizophora mangle over the other species, it was observed that the PM were very similar within each zone, with lower diversity in zone A. The beta diversity evaluated using IJ was 1, indicating that the diversity of species does not change between the zones, while the S index showed that there is a greater change in diversity between zone A and the remaining zones. These results can allow local and regional authorities to make decisions to protect said mangrove forest. On the other hand, it would also be advisable to carry out research to determine the impact that alterations in mangrove species biodiversity may have on the organisms that inhabit this mangrove forest.
Keywords: Avicenia germinans; Laguncularia racemosa; red mangrove; species richness; similarity.
Recibido: 30-11-2023.
Aceptado: 10-03-2024.
Los manglares son ecosistemas marinos muy importantes que proveen diversos recursos y servicios esenciales como produciendo alimentos, así como funciones ecológicas clave tales como estabilizar la costa (de la erosión y la inundación), limitar el ingreso del agua de mar, aminorar el impacto de olas y tormentas, Particularmente los manglares son importantes pues ayudan a mitigar el cambio climático al ser grandes sumideros de carbono(Arnaud et al., 2023; Bunting et al., 2022; Rull, 2023; Zhila et al., 2014); a pesar de todos sus servicios e importancia, este ecosistema está amenazado por las actividades humanas, tal es así que a nivel mundial se ha dado una fuerte reducción de su área, la que en 1996 era de 152 604 km2, pasó en 2020 a solo 147 359 km2, con una pérdida de más de 5000 km2, esto representa una tasa de deforestación de 3,4% (Bunting et al., 2022; Jia et al., 2023; Malik et al., 2023).
El ecosistema del manglar recibe su nombre por los árboles de mangle que lo pueblan, éstos son vegetación adaptada a la anoxia, alta salinidad e inundación; los mangles a nivel mundial, comprenden 240 especies, 48 de las cuales se consideran mangles verdaderos y 192 asociados; dentro de las cuales se hallan entre 50 a 74 especies arbóreas; siendo los manglares de Asia los que tienen mayor cantidad de especies y los de América la menor cantidad (Bezerra et al., 2022; Mitra et al., 2021; Rahman et al., 2024; Segaran et al., 2023; Thattai et al., 2023).
La mayor parte de los manglares se hallan en países en vías de desarrollo en los cuales muchos de ellos están en peligro crítico por la degradación de su hábitat, la deforestación y en especial por el cambio de uso del terreno, los que se han empleado para la agricultura y acuicultura (Ashton & Macintosh, 2024; Zhila et al., 2014).
Ciertas investigaciones han mostrado que manglares expuestos al impacto antrópico pueden tener índices de biodiversidad distintos a los de manglares conservados (Zhila et al., 2014); por lo que para poder conocer mejor el estado de un manglar, una buena opción es evaluar su diversidad.
En el Perú, los manglares se hallan al norte, en los departamentos de Tumbes y Piura, siendo el primero el que tiene la mayor área de manglar (Martinez, 2022; Seminario-Córdova et al., 2022).
En los manglares peruanos se hallan presentes árboles de mangle de varias especies como: mangle rojo (Rhizophora mangle), mangle negro (Avicennia germinans), mangle blanco (Laguncularia racemosa), mangle colorado (Rhizophora harrisonii) y mangle botón (Conocarpus erectus) (Dioses-Puelles et al., 2023); sin embargo, según diversos autores C. erectus, no es un mangle verdadero pues no posee adaptaciones típicas de un mangle (raíces especializadas de tipo zancudas o con neumatóforos así como viviparidad) (Hamilton, 2020).
Asimismo, R. harrisonii no sería una especie distinta, pues la clasificación de Rhizophora en América no está bien definida y varios autores indican que R. harrisonii podría ser un híbrido de R. mangle y R. racemosa o que las tres especies (R. harrisonii, R. racemosa y R. mangle) serían la misma especie (Mori et al., 2021; Takayama et al., 2021).
Debido a lo antes indicado, en esta investigación se ha registrado a los árboles del género Rhizophora del manglar de Puerto Pizarro como una única especie: R. mangle, y no se ha considerado a C. erectus como una especie de mangle.
El manglar de Puerto Pizarro es el que soporta mayor actividad antrópica en el manglar de Tumbes (Morán & Hidalgo, 2018; Ordinola-Zapata et al., 2019); esto posiblemente podría afectar a su desarrollo, adicionalmente ciertas zonas del mismo presentan mayor impacto antrópico, por lo que podrían existir diferencias entre dichas áreas respecto a su diversidad (Zhila et al., 2014).
MATERIAL Y MÉTODOS
Lugar de investigación
La investigación se llevó a cabo en el manglar de Puerto Pizarro, ubicado en Tumbes, Perú. Este manglar constituye el ecosistema más extenso de Perú, según lo señala (Aguirre-Sanchez et al., 2022; Martinez, 2022). La región Tumbes, donde se encuentra este manglar, presenta un clima semiárido con influencia oceánica, caracterizado por suelos compuestos de arcilla y arena. El período de lluvias ocurre generalmente en enero, febrero y marzo. Las temperaturas en la zona varían entre 22 y 29 °C (Pérez et al., 2016). Enclavado en este manglar se encuentra el pueblo de Puerto Pizarro, con una población aproximada de 7500 habitantes al año 2022. En este manglar, se realizan diversas actividades antrópicas entre ellas la pesca, el turismo, la agricultura y la acuicultura (Morán & Hidalgo, 2018; Ramírez, 2022).
Tamaño de la muestra
El ecosistema del manglar de Puerto Pizarro se extiende en un área de 830,14 hectáreas. El área del manglar se subdividió en tres zonas que fueron designadas como A, B y C. En cada zona se seleccionaron 41 puntos de muestreo consistentes en parcelas de 1 hectárea; en cada una de ellas se tomó una sub-área de 0,25 hectáreas (50 m x 50 m) para realizar el muestreo de los árboles del manglar (Figura 1).
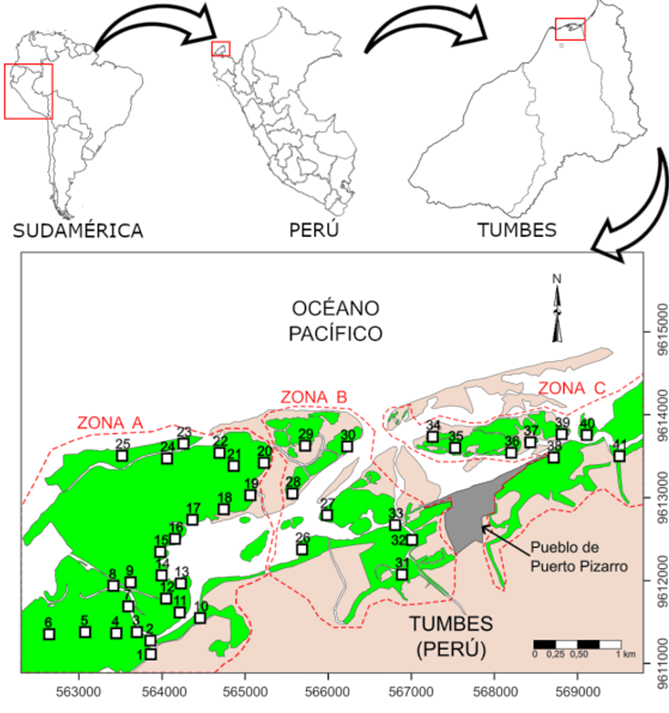
Figura 1. Zonas y parcelas de muestreo en el manglar de Puerto Pizarro (Sistema de coordenadas UTM, huso 17 banda M, datum WGS84).
Abundancia de árboles de mangle
En cada parcela de muestreo de 0,25 ha se identificaron los árboles de mangle según su especie; se contaron y midieron únicamente los mangles con un diámetro a la altura del pecho (DAP) ≥ 2,5 cm, siguiendo la recomendación de Villeda et al. (2018) para mangles de tipo arbustivo.
Se estableció el número de árboles por parcela y zona evaluada, así como se calculó su porcentaje.
Diámetro y altura de árboles de mangle
El DAP de los árboles de mangle se midió indirectamente tomando el perímetro del árbol con una cinta métrica a 1,30 m de la base de los árboles de mangle negro (A. germinans) y mangle blanco (L. racemosa); pero en el caso de R. mangle, se tomó 30 cm sobre las raíces zancudas más altas (Villeda et al., 2018). La altura (h) de los árboles de mangle se midió con un clinómetro.
Diversidad alfa de especies de mangle
La diversidad alfa de las especies de mangle se evaluó para cada parcela con tres índices: Shannon–Wiener; Simpson y equidad de Pielou (Pototan et al., 2020; Zhila et al., 2014).
El índice de Shannon–Wiener (H’)(Rodríguez & Medianero, 2022), se calculó mediante la ecuación 1:
|
|
(1) |
Donde:
i es la i-ésima especie.
pi es la proporción de la especie i.
R es el número de especies.
El índice de Simpson (Ds)(Rodríguez & Medianero, 2022) se calculó mediante la ecuación 2:
|
|
(2) |
Donde:
N es el número de individuos de todas las especies.
ni es el número de individuos de la especie i.
R es el número de especies.
El índice de equidad de Pielou (J’) se calculó mediante la ecuación 3:
|
|
(3) |
Donde:
H’ es el índice de Shannon-Wiener.
H’max es el máximo índice de Shannon-Wiener para la zona evaluada.
S es la riqueza de especies (número de especies) en la zona evaluada.
Se evaluó la similitud de los puntos de muestreo respecto a su diversidad, de dos maneras: un gráfico de agrupamiento jerárquico usando el software Past 4.14, con el algoritmo Unweighted pair group method with arithmetic mean (UPGMA) utilizando el índice de similitud de Bray-Curtis con restricción estratigráfica; y un gráfico de diversidad alfa (índice de Shannon-Wiener) de cada punto de muestreo.
El índice de similitud de Bray-Curtis se calculó con la ecuación 3, que se dedujo en base al índice de disimilitud que aparece en Nepali et al. (2022):
|
|
(3) |
Donde:
BCij es el valor calculado para el índice de similitud de Bray-Curtis entre los puntos i y j.
Cij es la suma de las abundancias menores de las especies comunes en los puntos i y j.
Si y Sj son el número de especies en los puntos i y j respectivamente.
Se evaluó la existencia de diferencias estadísti-camente significativas en la diversidad de las zonas en estudio con la prueba t de Hutcheson (Mohammad et al., 2021), según la ecuación 3:
|
|
(3) |
Donde:
t es el valor calculado para el estadígrafo evaluado.
H’1 y H’2 son los índices de Shannon-Wiener de las zonas que fueron comparadas.
H’1 y H’2 son los índices de Shannon-Wiener de las zonas que fueron comparadas.
Var H’1 y Var H’2 son las varianzas de los índices de Shannon-Wiener.
Las varianzas del estimador H’ (Var H’) se obtuvieron según la ecuación 4:
|
|
(4) |
Donde:
pi es la proporción de la especie i.
N es el número de árboles en la zona evaluada
S es la riqueza de especies (cantidad de especies) en la zona evaluada.
Para comparar el valor t se calculó los grados de libertad (df) para la prueba de hipótesis, según la ecuación 5:
|
|
(5) |
Donde:
df son los grados de libertad
H’1 y H’2 son los índices de Shannon-Wiener de las zonas en comparación.
Var H’1 y Var H’2 son las varianzas correspondientes de los índices H’ de las zonas en comparación.
N1 y N2 son las cantidades de árboles en las respectivas zonas evaluadas.
Diversidad beta de especies de mangle
Se evaluó la biodiversidad beta entre cada zona en estudio, con tres índices, el índice cualitativo de Jackard (IJ), y el cuantitativo de Sorensen (S) que fueron calculados para cada pareja de zonas mediante las ecuaciones 6 y 7:
Índice de Jackard (IJ):
|
|
(6) |
Donde:
C es el número de especies comunes a ambas zonas en comparación.
A es el número de especies presentes en la primera zona.
B es el número de especies presentes en la segunda zona.
Índice cuantitativo de Sorensen (S):
|
|
(7) |
Donde:
nJ es la suma de los mínimos de individuos de las especies comunes a ambas zonas.
nA es el total de individuos de las especies en la primera zona.
nB es el total de individuos de las especies en la segunda zona.
RESULTADOS Y DISCUSIÓN
Abundancia de árboles de mangle
En las sub-áreas de muestreo se registraron 7731 árboles de mangles, de los cuales la mayoría (51,5%) fueron árboles de R. mangle seguidos de A. germinans y L. racemosa con 26,8% y 21,7% respectivamente (tabla 1). El área B fue la que mayor cantidad de árboles presentó, con cantidades de árboles de especie similares para las tres especies, en tanto que en la zona A, se observó una cantidad mucho más alta de árboles de R. mangle que de las otras dos especies.
La predominancia de R. mangle en este manglar es coherente con lo reportado por otros autores en el caso del manglar de Tumbes, del cual forma parte el manglar de Puerto Pizarro como lo han reportado Cabrera (2022), Dioses-Puelles et al. (2023) y Martinez (2022).
Tabla 1
Abundancia de árboles de mangle en zonas del manglar de Puerto Pizarro
|
Especie |
Zona |
|
Total |
|||
|
A |
B |
C |
|
n |
% |
|
|
R. mangle |
2458 |
911 |
615 |
|
3984 |
51,5 |
|
A. germinans |
24 |
1025 |
1020 |
|
2069 |
26,8 |
|
L. racemosa |
187 |
1178 |
313 |
|
1678 |
21,7 |
|
Total |
2669 |
3114 |
1948 |
|
7731 |
100,0 |
La mayor abundancia de R. mangle sobre otras especies que se observa en la zona A, se puede deber a que en condiciones óptimas, estas plantas tienden a ocupar grandes áreas del manglar de manera casi exclusiva limitando el desarrollo de otras especies de mangle junto a ellas (Antepara, 2023), por lo que esto justificaría la mayor abundancia de R. mangle en la zona A, zona con poco impacto antrópico y menor grado de contaminación que las zonas B y C.
Diámetro de los árboles de mangle
De manera consistente y para las tres especies de mangle, los árboles de la zona A tuvieron un mayor DAP que en las otras dos zonas (Tabla 2), asimismo, los árboles de R. mangle tuvieron DAP más altos que los de las otras dos especies, lo cual indica que los árboles de mangle presentan un mayor nivel de desarrollo en la zona A.
Al respecto, se observa que los árboles de mangle en las zonas B y C, que son las zonas más cercanas al pueblo de Puerto Pizarro (el mayor centro poblado dentro del manglar tumbesino) muestran un menor grado de desarrollo, esto probable-mente debido a que en estas zonas hay muchas actividades antrópicas (pesca, acuicultura, turismo) y de contaminantes (efluentes, residuos sólidos, entre otros).
Tabla 2
Diámetro a la altura del pecho (Promedio ± Desviación estándar en cm) de árboles de mangle en zonas del manglar de Puerto Pizarro
|
Especie |
Zona |
Total |
||
|
A |
B |
C |
||
|
R. mangle |
19,32±6,11 |
10,20±2,83 |
8,31±1,73 |
15,53±6,98 |
|
A. germinans |
12,66±4,18 |
7,60±1,35 |
8,37±1,68 |
8,04±1,70 |
|
L. racemosa |
13,15±4,52 |
5,97±2,39 |
8,09±1,54 |
7,17±3,45 |
|
Todas |
18,83±6,23 |
7,74±2,84 |
8,31±1,67 |
11,71±6,64 |
Montero (2019), reportó que existe contaminación por metales pesados (Cd, Pb, Mn y Fe) en dichas zonas de Puerto Pizarro. Nguyen et al. (2020) y Prihatiningrum et al. (2018) han señalado que la los metales pesados pueden reducir la tasa de crecimiento del mangle; así también, Ramos et al. (2023), indican que los árboles de mangle tienen un menor grado de desarrollo en aquellos lugares que presenten un mayor impacto antrópico; lo expresado por estos autores, por tanto, permiten suponer que posiblemente el menor DAP (indicador de árboles menos desarrollados), se den en las zonas B y C por problemas de contaminación e impacto antrópico.
Altura de los árboles de mangle
Los árboles de mangle fueron consistentemente más altos en la zona A y menores en las zonas B y C (Tabla 3), esto posiblemente por el hecho que las zonas B y C son zonas con mayor perturbación ambiental; este hecho ya ha sido reportado por autores como De Santana et al. (2020) y Ramos et al. (2023), quienes precisan que las actividades antrópicas pueden producir alteraciones ambientales que afectan a las características estructurales de los mangles (una de ellas es su altura), llegando incluso a incrementar su mortalidad, esto debido a que varias actividades antrópicas pueden alterar el suelo en el que se asientan estos manglares.
Tabla 3
Altura de árboles de mangle (Promedio ± Desviación estándar en cm) en zonas del manglar de Puerto Pizarro
|
Especie |
Zona |
Total |
||
|
A |
B |
C |
||
|
R. mangle |
12,64±2,82 |
7,85±1,74 |
7,24±1,64 |
10,71±3,47 |
|
A. germinans |
7,73±1,66 |
5,44±1,53 |
5,70±1,66 |
5,60±1,62 |
|
L. racemosa |
10,61±2,30 |
6,07±1,88 |
7,08±1,82 |
6,76±2,39 |
|
Todas |
12,45±2,86 |
6,38±1,99 |
6,41±1,84 |
8,49±3,68 |
Diversidad alfa de especies de mangle
La biodiversidad alfa de los árboles de mangle del manglar de Puerto Pizarro fue baja según el índice de Shannon-Wiener (H’ = 1,0260), pues fue menor de 2 (García, 2017; Mohammad et al., 2021), lo cual puede deberse al reducido número de especies de mangle, que es una característica propia de mangles americanos(Bezerra et al., 2022); mientras que en el caso del índice de Simpson (DS = 0,6158) se consideraría media. Si bien no hay reportes de estudios previos de diversidad de árboles de mangle en el manglar de Puerto Pizarro; si los hay referidos al manglar del Santuario Nacional Los Manglares de Tumbes (SNLMT)(Tumbes, Perú), ubicado a 13 km al noreste de Puerto Pizarro; así, tomando como base los datos de Idrogo (2016), se ha calculado que los índices de diversidad alfa fueron bastante similares al de este estudio, con la excepción del índice J’, con valores de: H’ = 1,169, DS = 0,6367 y J’ = 0,7263; así mismo, en base a los datos de Dioses (2020), se ha calculado que para la zona de manglar bajo y alto del SNLMT, los índices fueron también similares (salvo J’) con valores de: H’ = 1,262, DS = 0,6859 y J’ = 0,7841. La diferencia entre los valores de J’, se deben a que la riqueza de especies fue distinta, entre esta investigación (S = 3) y los estudios de Idrogo (2016) y de Dioses (2020) (S = 5), esto porque dichos autores han asumido a C. erectus y a R. harrisonii como especies de mangle, de manera contraria al criterio tomado en esta investigación.
Los valores de diversidad observados posiblemente sean similares con los del SNLMT por la corta distancia entre ambos lugares; sin embargo, al comparar con datos de los siguientes manglares más cercanos, que son los del Ecuador, no se mantienen los mismos valores de diversidad; así por ejemplo, con los datos de Guerrero (2022), se calculó para el manglar de El Guabo (El Oro) ubicado a 60 km al noreste de Puerto Pizarro que H’ = 0,7806, DS = 0,4707 y J’=0,7105; de igual manera en base a la información de Freire (2021), se calculó para Puerto El Morro (Guayas): H’ = 0,5915; DS = 0,3111 y J’ = 0,5384; y con los datos reportados por Patiño (2018) para el Manglar del río Muisne (Esmeraldas): H’ = 0,5915; DS = 0,3111 y J’ = 0,5384. Estos valores son más bajos que los hallados en esta investigación y denotan una diversidad más baja, cabe mencionar que en estos estudios sólo se tuvo una riqueza de especies de 3.
Asimismo, se debe señalar que en todas las investigaciones que se han mencionado, las especies más abundantes fueron correspondientes al género Rhizophora, tal como ha ocurrido en este estudio.
Respecto a la diversidad de especies de mangle en las zonas en que se subdividió el manglar de Puerto Pizarro, se observó que fue diferente para la zona A, en comparación las zonas B y C, las cuales fueron algo más similares entre ellas. El índice de Shannon-Wiener y el de Pielou (J’) fue más bajo en la zona A (0,3048 y 0,2774) en comparación con las zonas B (1,0930 y 0,9949) y C (0,9971 y 0,9076) (Tabla 4).
Tabla 4
Índices de diversidad alfa de árboles de mangle en las zonas del manglar de Puerto Pizarro
|
Zona |
Índice |
||
|
Shannon-Wiener (H’) |
Simpson (DS) |
Pielou (J’) |
|
|
A |
0,3048 |
0,8531 |
0,2774 |
|
B |
1,0930 |
0,3368 |
0,9949 |
|
C |
0,9971 |
0,3994 |
0,9076 |
|
Total |
1,0260 |
0,6158 |
0,9339 |
Los valores de H’ de las zonas en estudio, indican que la diversidad alfa fue baja pues todos ellos fueron menores a 2 (García, 2017; Mohammad et al., 2021).
Sin embargo al evaluar el índice de Simpson (DS), se observa que en la zona A, hay un mayor valor del mismo, lo cual se debe a la clara dominancia que tiene R. mangle sobre las otras especies (Tabla 1) , lo cual es común, puesto que R. mangle cuando se desarrolla en un ambiente con buenas condiciones para su desarrollo tiende a desplazar a las otras especies de mangle (Bezerra et al., 2022). Los valores de DS en las zonas B y C fueron menores pues en ellas hubo una mayor equitatividad del número de ejemplares de cada especie.
El DS de la zona A indica una diversidad menor (DS = 0,8531) comparado con las otras dos zonas (DS de 0,3368 y 0,3994) (Tabla 4); puesto que el índice de Simpson toma valores entre 0 y 1, siendo mayor la diversidad en valores bajos de este rango y menor en valores altos. La baja diversidad en mangles americanos es bien conocida, lo cual se debe a su menor cantidad de especies comparado con los de otros ecosistemas forestales y también a que especies de la familia Rhizophoraceae, tienden a dominar y formar agrupaciones que impiden el desarrollo de otras especies de mangle en áreas aledañas (Abino et al., 2014).
Respecto a la diversidad observada en cada punto de muestreo, esta fue en su mayoría bastante uniforme dentro de las zonas A y C, con una mayor variación en la zona B, como se puede apreciar en la Figura 2, en la que se muestra los valores del índice de Shannon-Wiener (H’) para cada punto de muestreo.
En la zona A se observó que la mayoría de los 25 puntos tienen un índice H’ entre 0,2 y 0,4; que refleja el hecho que en dichos puntos R. mangle fue la especie dominante con pocos ejemplares de L. racemosa (entre 2 a 11 ejemplares por punto) y aún menos de A. germinans (entre 0 y 5); en tanto que, en las zonas B y C, los puntos de muestreo tuvieron mayor valor de H’, pues tuvo una menor población de R. mangle y una proporción mayor de árboles de A. germinans y L. racemosa.
Sin embargo, en el punto de muestreo 10 de la zona A, se observó mayor diversidad, pues A. germinans y L. racemosa fueron más abundantes (14 y 9 ejemplares respectivamente); pero en el punto 38, (zona C), la diversidad fue cero, debido a que en él se halló un rodal de árboles de R. mangle sin presencia de otras especies.
El gráfico de similitud de los puntos de muestreo basados en el índice de Bray-Curtis (Figura 3), mostró que los puntos de la zona A, formaron un conglomerado bastante homogéneo.
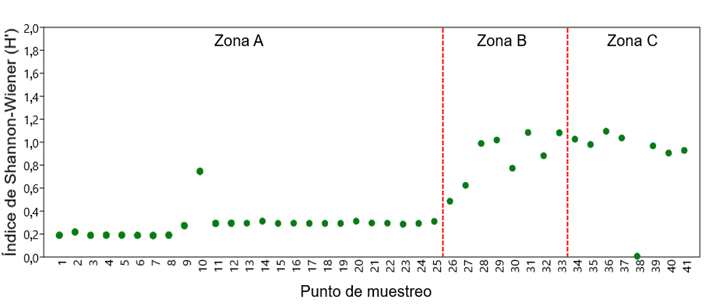
Figura 2. Índice de diversidad de Shannon-Wiener (H’) según punto de muestreo.
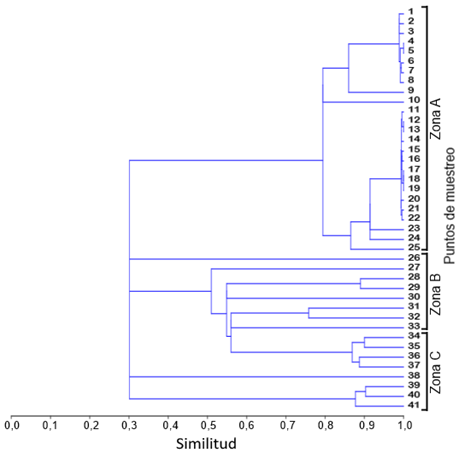
Figura 3. Gráfico de similitud de los puntos de muestreo basado en la distancia de Bray-Curtis.
Entre los puntos de la zona A, el que tuvo menor similitud fue el punto 10, por las consideraciones antes expuestas.
Los puntos de las zonas B y C tuvieron menor similitud. En particular, los puntos 26 y 38, mostraron la mínima similitud con el resto de puntos de muestreo, debido a que en el caso del punto 26, hubo una cantidad muy alta de árboles de L. racemosa (624 ejemplares) en comparación con los de R. mangle y de A. germinans (68 y 31 ejemplares); mientras que en el caso del punto 38 se halló solo una sola especie, R. mangle, por lo que la dominancia de ésta fue máxima
Las diversidades de los árboles de mangle de las zonas evaluadas (medidas como H’) fueron estadísticamente diferentes (p<0,001), tal como se aprecia en los resultados de la prueba t de Hutchenson (tabla 5), de lo cual se deduce que las diversidades alfa fueron diferentes entre todas las zonas evaluadas, siendo menor la diversidad en la zona A y mayor en la zona B y C.
Tabla 5
Resultados de la prueba t de Hutchenson para la comparación del índice de Shannon-Wiener entre zonas
|
Zonas comparadas |
Parámetro de la prueba t |
|||
|
|t| |
Grados de libertad (df) |
t crítico |
p |
|
|
AB |
51,81 |
2755 |
1,96 |
<0,001 |
|
AC |
38,56 |
4319 |
1,96 |
<0,001 |
|
BC |
9,76 |
2100 |
1,96 |
<0,001 |
Diversidad beta de especies de mangle
La diversidad beta evaluada entre las zonas del manglar de Puerto Pizarro, tuvo diferentes valores de acuerdo con el tipo de índice utilizado. El que menos información aportó fue el de Jackard (IJ)(tabla 6), que obtuvo valores iguales a 1,00; que indicó que no hubo ningún tipo de cambio en la diversidad al pasar de una zona a otra; sin embargo, este valor al ser cualitativo solo evaluó el cambio en el número de especies pero no el cambio de su abundancia (García, 2017); por ello, al estar presentes las mismas tres especies (R. mangle, A. germinans y L. racemosa) en las tres zonas, no se evidenció un cambio en su riqueza de especies y por tanto en el índice de Jackard.
Tabla 6
Índices de Jackard y Sorensen cuantitativo de árboles de mangle en las zonas del manglar de Puerto Pizarro
|
Zonas comparadas |
Índice |
|
|
Jackard (IJ) |
Sorensen (S) |
|
|
AB |
1 |
0,388 |
|
AC |
1 |
0,357 |
|
BC |
1 |
0,770 |
El índice cuantitativo de Sorensen (tabla 6), incluyó la abundancia como un parámetro para evaluar la diversidad beta, es por ello que se observó que existieron diferentes valores entre los pares de zonas comparadas; en general, se observó que la zona A mostró menor porcentaje de similitud con las otras dos áreas (similitud con la zona B de 38,8% y con la zona C de 35,7%); en tanto, que las zonas B y C presentaron mayor similitud (77,0%) entre ellas; esto es consistente con lo observado respecto a las diferencias en diversidad alfa entre las tres zonas del manglar de Puerto Pizarro, en que se evidenció que la zona A tiene una diversidad mucho menor que las de las zonas B y C.
A su vez, esta diferenciación entre las zonas evaluadas se justifica por el impacto antrópico que es menor en la zona A y mayor en la B y C, al respecto, varios autores como De Santana et al. (2020) y Ramos et al. (2023)señalan que el impacto antrópico es capaz de cambiar la diversidad alfa y por tanto su razón de cambio es decir la diversidad beta.
CONCLUSIONES
La diversidad alfa del manglar de Puerto Pizarro fue baja al ser evaluada por los índices de Shannon-Wiener y de Pielou; pero fue media respecto al índice de Simpson. Estos valores de diversidad se deben a una mayor dominancia de R. mangle en la zona, así como posiblemente al impacto de las actividades antrópicas en dicho lugar. La zona A mostró menor diversidad alfa que las zonas B y C, por la mayor dominancia en la misma de R. mangle que desplazó a las otras especies. El análisis de diversidad de los puntos de muestreo mostró que estos fueron bastante homogéneos en la zona A, teniendo una menor diversidad que los de las zonas B y C. El análisis de la diversidad beta, confirmó que las tres zonas presentan distinta diversidad, siendo mayor el cambio de ésta, cuando se pasa de la zona A a las otras dos zonas. La zona A, que es una zona con menor impacto antrópico, mostró un mayor grado de desarrollo de la población de árboles de R. mangle, evidenciada por sus mayores DAP y alturas, esto porque en condiciones óptimas, R. mangle predomina sobre las otras especies, desarrollándose más y desplazando a las otras especies. Los hallazgos realizados permiten confirmar que las zonas B y C, ubicadas al centro y este del manglar de Puerto Pizarro, presentan una menor abundancia de R. mangle, que posiblemente esté relacionada con un mayor impacto antrópico. Estos resultados pueden ayudar a las autoridades locales y regionales a tomar decisiones adecuadas para proteger a dicho manglar. Por otro lado, también sería conveniente realizar investigaciones para determinar el impacto que la alteración de la biodiversidad de las especies de mangles pueda tener en los organismos que habitan en este manglar.
REFERENCIAS BIBLIOGRÁFICAS
Abino, A. C., Castillo, J. A. A., & Lee, Y. J. (2014). Species diversity, biomass, and carbon stock assessments of a natural mangrove forest in Palawan, Philippines. Pak. J. Bot, 46(6), 1955-1962.
Aguirre-Sanchez, A., Purca, S., & Indacochea, A. G. (2022). Microplastic presence in the mangrove crab Ucides occidentalis (Brachyura: Ocypodidae) (Ortmann, 1897) derived from local markets in Tumbes, Peru. Air, Soil and Water Research, 15, 117862212211245. https://doi.org/10.1177/11786221221124549
Antepara Peñafiel, L. A. (2023). Composición y estructura del manglar de la Reserva Ecológica Manglares Churute, Provincia del Guayas, Ecuador [Tesis de Biólogo, Universidad de Guayaquil]. http://repositorio.ug.edu.ec/handle/redug/67638
Arnaud, M., Krause, S., Norby, R. J., Dang, T. H., Acil, N., Kettridge, N., Gauci, V., & Ullah, S. (2023). Global mangrove root production, its controls and roles in the blue carbon budget of mangroves. Global Change Biology, 29(12), 3256-3270. https://doi.org/10.1111/gcb.16701
Ashton, E. C., & Macintosh, D. J. (2024). Mangrove Rehabilitation and Brachyuran Crab Biodiversity in Ranong, Thailand. Diversity, 16(2), 92. https://doi.org/10.3390/d16020092
Bezerra, W. M., Tavares, T. C. L., Nogueira, V. L. R., Normando, L. R. O., Bomfim, T. A., Angelim, A. L., & Melo, V. M. M. (2022). Bacteriome associated with Rhizophora mangle sediments within Brazil semi-arid mangroves. Arquivos de Ciências Do Mar, 55, 34-51.
Bunting, P., Rosenqvist, A., Hilarides, L., Lucas, R. M., Thomas, N., Tadono, T., Worthington, T. A., Spalding, M., Murray, N. J., & Rebelo, L.-M. (2022). Global mangrove extent change 1996–2020: Global mangrove watch version 3.0. Remote Sensing, 14(15), 3657. https://doi.org/10.3390/rs14153657
Cabrera Dioses, V. V. (2022). Análisis multitemporal del comportamiento forestal en el ecosistema manglar mediante percepción remota, período 1986 a 2021, Tumbes. [Tesis de Ingeniero Forestal y del Medio Ambiente, Universidad Nacional de Tumbes]. https://repositorio.untumbes.edu.pe/handle/20.500.12874/63842
De Santana Lopes, D. M., De Oliveira Chaves, F., & Pereira Tognella, M. M. (2020). Mangrove mortality: Analyses of natural and anthropic causes and their effects on forest dynamics. Journal of Coastal Research, 95(sp1), 102. https://doi.org/10.2112/SI95-020.1
Dioses Puelles, J. E. (2020). Determinación y evaluación de la cobertura vegetal a través de parcelas de monitoreo permanente en el Santuario Nacional los Manglares de Tumbes—Perú [Tesis de Ingeniero Forestal y del Medio Ambiente, Universidad Nacional de Tumbes]. https://repositorio.untumbes.edu.pe/handle/20.500.12874/2328
Dioses-Puelles, J., García-García, R., & Bermejo-Requena, L. A. (2023). Tipos de cobertura vegetal del Área Natural Protegida “Santuario Nacional Los Manglares de Tumbes”, Tumbes, Perú. Manglar, 20(2), 177-183. https://doi.org/10.57188/manglar.2023.020
Freire Carpio, J. S. (2021). Composición y estructura de los manglares de borde, Puerto El Morro, provincia del Guayas, Ecuador. [Tesis de Bióloga, Universidad de Guayaquil]. http://repositorio.ug.edu.ec/handle/redug/52772
García Velandia, H. A. (2017). Estudio preliminar de la fenología de fructificación en la vegetación con frutos carnosos en un relicto de bosque suptropical premontano en la Vereda Marroquín, Corregimiento El Morro, Casanare [Tesis de Biólogo, Universidad Distrital Francisco José de Caldas]. https://repository.udistrital.edu.co/bitstream/handle/11349/7095/GarciaVelandiaHugoArmando2017.pdf?sequence=1&isAllowed=y
Guerrero Calderón, J. M. (2022). Composición, distribución y estructura de los manglares de borde de las comunas Bajo Alto y La Puntilla—El Guabo, provincia de El Oro, Ecuador 2021. [Tesis de Biólogo Marino, Universidad Estatal Península de Santa Elena]. https://repositorio.upse.edu.ec/handle/46000/8861
Hamilton, S. E. (2020). Botany of mangroves. En S. E. Hamilton, Mangroves and aquaculture (Vol. 33, pp. 1-40). Springer International Publishing. https://doi.org/10.1007/978-3-030-22240-6_1
Idrogo Harvey, I. K. (2016). Estructura de las especies de mangle en el Santuario Nacional Los Manglares de Tumbes [Tesis de Bióloga, Universidad Nacional de Piura]. http://repositorio.unp.edu.pe/handle/UNP/1335
Jia, M., Wang, Z., Mao, D., Ren, C., Song, K., Zhao, C., Wang, C., Xiao, X., & Wang, Y. (2023). Mapping global distribution of mangrove forests at 10-m resolution. Science Bulletin, 68(12), 1306-1316. https://doi.org/10.1016/j.scib.2023.05.004
Malik, A., Rahim, Abd., Jalil, Abd. R., Amir, M. F., Arif, D. S., Rizal, M., Husain, J., William, D., & Jihad, N. (2023). Mangrove blue carbon stocks estimation in South Sulawesi Indonesia. Continental Shelf Research, 269, 105139. https://doi.org/10.1016/j.csr.2023.105139
Martinez Cabrera, R. (2022). Presión antrópica y su relación con la susceptibilidad del Santuario Nacional los Manglares de Tumbes, 2000 – 2020. Revista Cátedra Villarreal Posgrado, 1(2), Article 2.
Mitra, S., Naskar, N., & Chaudhuri, P. (2021). A review on potential bioactive phytochemicals for novel therapeutic applications with special emphasis on mangrove species. Phytomedicine Plus, 1(4), 100107. https://doi.org/10.1016/j.phyplu.2021.100107
Mohammad, K., Suratman, Nismah, N., & Siti, A. (2021). Impact of 2-years practice of organic coffee farming on soil arthropod diversity. World Journal of Advanced Research and Reviews, 10(1), 168-173. https://doi.org/10.30574/wjarr.2021.10.1.0144
Montero, P. (2019). Calidad ambiental de la bahía de Puerto Pizarro y del ecosistema de manglar, Tumbes, Perú. Junio 2009. Boletín. Instituto del Mar del Perú, 46(4), 636-660.
Morán Ávila, B., & Hidalgo Mogollón, A. (2018). Impactos ambientales en la Bahía Puerto Pizarro. Manglar, 13(2), 43-51.
Mori, G. M., Madeira, A. G., Cruz, M. V., Tsuda, Y., Takayama, K., Matsuki, Y., Suyama, Y., Iwasaki, T., De Souza, A. P., Zucchi, M. I., & Kajita, T. (2021). Testing species hypotheses in the mangrove genus Rhizophora from the Western hemisphere and South Pacific islands. Estuarine, Coastal and Shelf Science, 248, 106948. https://doi.org/10.1016/j.ecss.2020.106948
Nepali, B., Skartveit, J., & Baniya, C. B. (2022). Diversity patterns of vascular plants at varied elevations in Arghakhanchi, West Nepal. Journal of Plant Resources, 20(2), 29-39. https://doi.org/10.3126/bdpr.v20i2.56955
Nguyen, A., Richter, O., Le, B. V. Q., Phuong, N. T. K., & Dinh, K. C. (2020). Long-term heavy metal retention by mangroves and effect on its growth: A field inventory and scenario simulation. International Journal of Environmental Research and Public Health, 17(23), 9131. https://doi.org/10.3390/ijerph17239131
Ordinola-Zapata, A., Siccha, Z., Castillo-Carrillo, P., & Luque, C. (2019). Identificación mediante ADN barcode de peces invasores en el manglar de Tumbes (Perú). Manglar, 16(2), 91-97. https://doi.org/10.17268/manglar.2019.013
Patiño Márquez, L. D. (2018). Inventario de especies arbóreas estuarinas que interactúan en el ecosistema de manglar del refugio de vida silvestre manglares estuario río Muisne. [Tesis de Ingeniero en Recursos Naturales y Ambientales]. https://repositorio.uleam.edu.ec/handle/123456789/3111
Pérez, A., Velazco, F., Carhuapoma, W., & Guitiérrez, D. (2016). Efecto del régimen hídrico sobre las condiciones geoquímicas de los sedimentos submareales de los manglares de Tumbes. Memoria Tercer Encuentro de Investigadores Ambientales, 1-17.
Pototan, B., Capin, N., Delima, A. G., & Novero, A. (2020). Assessment of mangrove species diversity in Banaybanay, Davao Oriental, Philippines. Biodiversitas Journal of Biological Diversity, 22(1). https://doi.org/10.13057/biodiv/d220120
Prihatiningrum, A., Arifin, S., Sutarman, & Abror, M. (2018). The response of seedling growth of Rhizophora apiculuta to various concentrations of Sidoarjo mud. Journal of Physics: Conference Series, 1114, 012001. https://doi.org/10.1088/1742-6596/1114/1/012001
Rahman, Lokollo, F. F., Manuputty, G. D., Hukubun, R. D., Krisye, Maryono, Wawo, M., & Wardiatno, Y. (2024). A review on the biodiversity and conservation of mangrove ecosystems in Indonesia. Biodiversity and Conservation. https://doi.org/10.1007/s10531-023-02767-9
Ramírez Astudillo, J. C. (2022). Sistema de gestión ambiental para el manejo de residuos sólidos en el Centro Poblado villa Puerto Pizarro [Tesis de Maestro en Acuicultura y Gestión Ambiental, Universidad Nacional de Tumbes]. https://repositorio.untumbes.edu.pe/handle/20.500.12874/63754
Ramos, J. G., Gracia-Sánchez, J., & Marrufo-Vázquez, L. (2023). Loss of mangroves as a consequence of the anthropic interactions downstream a river basin. Journal of Ecohydraulics, 8(1), 71-80. https://doi.org/10.1080/24705357.2020.1820913
Rodríguez, L. A., & Medianero, E. (2022). The composition of braconid wasp communities in three forest fragments in a tropical lowland forest of Panama. BMC Ecology and Evolution, 22(1), 98. https://doi.org/10.1186/s12862-022-02051-4
Rull, V. (2023). Rise and fall of Caribbean mangroves. Science of The Total Environment, 885, 163851. https://doi.org/10.1016/j.scitotenv.2023.163851
Segaran, T. C., Azra, M. N., Lananan, F., Burlakovs, J., Vincevica-Gaile, Z., Rudovica, V., Grinfelde, I., Rahim, N. H. A., & Satyanarayana, B. (2023). Mapping the link between climate change and mangrove forest: A global overview of the literature. Forests, 14(2), 421. https://doi.org/10.3390/f14020421
Seminario-Córdova, R. A., Barreto, I. B., & Tuesta, Z. E. E. (2022). Coastal wetlands of the north of Peru: Preservation progress. Acta Scientiarum. Biological Sciences, 44, e62571. https://doi.org/10.4025/actascibiolsci.v44i1.62571
Takayama, K., Tateishi, Y., & Kajita, T. (2021). Global phylogeography of a pantropical mangrove genus Rhizophora. Scientific Reports, 11(1), 7228. https://doi.org/10.1038/s41598-021-85844-9
Thattai, D., Rangarajan, S., Rajan, R. J., & Rajan, L. J. (2023). Mangrove literature from 2000 to 2019 – A Scientometric analysis of Scopus records. Journal of Scientometric Research, 11(3), 458-468. https://doi.org/10.5530/jscires.11.3.49
Villeda Chávez, E., Lara Domínguez, A. L., González Zamorano, P., Rubio, E. A., Valderrama Landeros, L. H., Ramírez García, P., García Calva, L., Argüello Velázquez, J., & Cruz López, M. I. (2018). Muestreo de variables estructurales. En M. T. Rodríguez Zúñiga, E. Villeda Chávez, A. D. Vázquez-Lule, M. Bejarano, M. I. Cruz López, M. Olguin, S. A. Villela Gaytán, & R. Flores (Eds.), Métodos para la caracterización de los manglares mexicanos: Un enfoque espacial multiescala (1ra edición, pp. 70-129). Comisión Nacional para el Conocimiento y Uso de la Biodiversidad. https://bioteca.biodiversidad.gob.mx/janium/Documentos/14078.pdf
Zhila, H., Mahmood, H., & Rozainah, M. Z. (2014). Biodiversity and biomass of a natural and degraded mangrove forest of Peninsular Malaysia. Environmental Earth Sciences, 71(11), 4629-4635. https://doi.org/10.1007/s12665-013-2853-6