 |
INTRODUCCIÓN
Un recubrimiento a base de mucílago de tuna y extracto de llantén mejora la vida útil de mandarinas
A coating made from prickly pear mucilage and plantain extract improves the shelf life of mandarins
Walter Cubas-Irigoin1,*; Haley Figueroa-Avalos2; Julio Chico-Ruíz3
1 Escuela de Posgrado, Universidad Nacional de Trujillo. Trujillo, Perú.
2 Escuela de Ingeniería Agroindustrial, Facultad de Ciencias Agropecuarias, Universidad Nacional de Trujillo, Av. Juan Pablo II s/n, Trujillo, Perú.
3 Laboratorio de Cultivos Celulares. Facultad de Ciencias Biológicas. Universidad Nacional de Trujillo. Trujillo, Perú.
* Autor corresponsal: wacuir02@gmail.com (W. Cubas-Irigoin).
ORCID de los autores:
W. Cubas-Irigoin: https://orcid.org/0009-0003-8185-1404 H. Figueroa-Avalos: https://orcid.org/0000-0002-3658-7005
J. Chico-Ruíz: https://orcid.org/0000-0002-7287-321X
RESUMEN
La mandarina (Citrus reticulata Blanco) es una fruta cítrica susceptible a procesos de senescencia y descomposición, principalmente de origen fúngico. Por ello, el objetivo de esta investigación fue evaluar el efecto de un recubrimiento a base de mucílago de tuna (Opuntia ficus-indica) y extracto de llantén (Plantago major) en la preservación de mandarinas contra Penicillium digitatum. Los cítricos fueron tratados por inmersión en la solución de mucílago de tuna (1% y 3%) y extracto de llantén (1% y 5%) correspondiente. Posteriormente, a cada fruto se le inoculó el hongo por aspersión y se almacenaron a 25 °C y humedad relativa de 85% durante 30 días. Se realizaron los análisis de sólidos solubles, pH, firmeza y pérdida de peso a los 10, 20 y 30 días de almacenamiento. Se identificó que el tratamiento con extracto de llantén al 5%, y la combinación de extracto de llantén al 5% con mucílago de tuna al 3%, mostraron los menores porcentajes de pérdida de peso, con valores de 5,67 % y 6,03 %, respectivamente. Además, fueron los tratamientos que presentaron los mejores valores de firmeza y sólidos solubles al cabo de los 30 días. Se concluyó que un recubrimiento a base de mucílago de tuna y extracto de llantén permite conservar las características fisicoquímicas de los frutos de mandarinas.
Palabras clave: Penicillium; llantén; mucílago; Plantago major.
ABSTRACT
Mandarin (Citrus reticulata Blanco) is a citrus fruit susceptible to senescence and decay processes, mainly of fungal origin. Therefore, the objective of this research was to evaluate the effect of a coating based on prickly pear (Opuntia ficus-indica) mucilage and plantain (Plantago major) extract on the preservation of mandarins against Penicillium digitatum. Citrus fruits were treated by immersion in the corresponding solution of prickly pear mucilage (1% and 3%) and plantain extract (1% and 5%). Subsequently, each fruit was inoculated with the fungus by spraying and stored at 25 °C and 85% relative humidity for 30 days. Analyses of soluble solids, pH, firmness, and weight loss were performed after 10, 20, and 30 days of storage. Treatment with 5% plantain extract and the combination of 5% plantain extract and 3% prickly pear mucilage showed the lowest percentages of weight loss, with values of 5.67% and 6.03%, respectively. Furthermore, these treatments showed the highest firmness and soluble solids values after 30 days. It was concluded that a coating based on prickly pear mucilage and plantain extract helps preserve the physicochemical characteristics of mandarin fruits.
Keywords: Penicillium; plantain; mucilage; Plantago major.
Recibido: 23-09-2025.
Aceptado: 31-01-2026
Los cítricos, reconocidos a nivel mundial por sus múltiples aplicaciones, poseen numerosos fitoquímicos y componentes bioactivos con variadas propiedades beneficiosas para la salud, además son una importante fuente de compuestos fenólicos y fibra dietética (Rafiq et al., 2018). La mandarina (Citrus reticulata Blanco) es una fruta cítrica reconocida por su valor nutricional y compuestos bioactivos. Sin embargo, es susceptible a procesos de senescencia y descomposición, principalmente de origen fúngico (Devi et al., 2025). Entre los principales causantes del deterioro poscosecha, destacan Penicillium digitatum y Penicillium italicum causantes de las pudriciones verdes y azules, respectivamente (Devi et al., 2023). Ante esta problemática, diversos estudios han evaluado el uso de recubrimientos comestibles, empleando goma laca y cera de carnaúba, con el objetivo de conservar la calidad del fruto y prolongar su vida útil (Devi et al., 2023, Devi et al., 2025). En este sentido, los recubri-mientos comestibles consisten en capas delgadas y consumibles que se aplican directamente a la superficie de los alimentos, preservando la calidad y prolongando su vida útil (Abu-Shama et al., 2020). Además, los recubrimientos comestibles facilitan el control de la pérdida de peso al reducir los proce-sos de respiración y transpiración, preservando así la textura y las propiedades nutricionales de la fruta (Sortino et al., 2022). Asimismo, estos recu-brimientos pueden incorporar aditivos naturales como antimicrobianos y antioxidantes, mejorando su funcionalidad y estabilidad. Las formulaciones varían, desde hidrocoloides (polisacáridos y proteínas) hasta lípidos y mezclas compuestas, cada una adaptada a las necesidades específicas de conservación de alimentos (Karnwal et al., 2025).
Una de las fuentes naturales más investigadas para la formulación de recubrimientos es el mucílago extraído de la tuna (Opuntia ficus-indica). Esta especie no solo posee una notable resistencia a condiciones climáticas adversas, sino también un alto valor nutricional y propiedades terapeúticas (Prisa, 2021). Por ejemplo, se ha reportado que un recubrimiento comestible de mucílago de tuna más un 5% de ácido ascórbico permite mantener la calidad de las fresas y extender su vida poscosecha (Liguori, Gaglio, Settanni, et al., 2021). Asimismo, diversos estudios indican que el mucílago de la tuna mejora los parámetros de comerciabilidad y comestibilidad de frutos mínimamente procesados como higos, tunas y rodajas de kiwi frescas (Liguori et al., 2021; Sortino et al., 2022; Sortino et al., 2024).
Por otra parte, los extractos vegetales como los de llantén (Plantago major) han cobrado interés en el desarrollo de alimentos funcionales por sus propiedades antioxidantes, antiinflamatorias y antimicrobianas, lo que sugiere su potencial uso como agente bioactivo complementario al mucílago de la tuna en matrices comestibles (Albahri et al., 2023). Por ello, surge la necesidad de explorar formulaciones sinérgicas que integren polisacári-dos naturales con extractos vegetales para crear recubrimientos multifuncionales.
No se ha reportado estudios que evalúen la sinergia del mucílago de tuna y extracto de llantén en la elaboración de recubrimientos comestibles. Por ello, el objetivo del presente estudio fue evaluar el efecto de un recubrimiento comestible a base de mucílago de tuna (Opuntia ficus-indica) y extracto de llantén (Plantago major) en la preservación de mandarinas frente al ataque de Penicillium digitatum.
Además, se propuso diseñar una recubierta de doble acción: que no solo atenúe el proceso de maduración, sino que también actúe como barrera protectora frente a patógenos fúngicos, contribu-yendo así a la extensión de la vida de anaquel del fruto.
METODOLOGÍA
Obtención del mucílago de tuna
Se lavaron las hojas de tuna con agua e hipoclorito sódico (100 ppm) durante 5 min. A continuación, se realizó la separación de la piel y la pulpa. Para ello se cortaron las hojas longitudinalmente y se retiró suavemente el mucílago hasta quedar completa-mente separado del parénquima cortical o piel. Posteriormente los geles se congelaron a -20 oC para su posterior uso.
Obtención de extracto de llantén
Las hojas de llantén se lavaron y se molieron en un mortero. Posteriormente, se filtró con una malla para separar los sólidos de la fase líquida. El extracto se almacenó en refrigeración a 10 °C (Núñez et al., 1997).
Cultivo de Penicillium digitatum
El patógeno Penicillium digitatum se aisló de cítricos infectados. Luego se cultivó en agar de papa dextrosa (PDA). Se extrajeron esporas de cultivos de PDA de 7 días de antigüedad a 28 °C y se suspendieron en agua destilada estéril. La suspensión se filtró a través de dos capas de gasa estéril para eliminar el micelio adherido (Liu et al., 2017). Se obtuvo una suspensión homogénea de esporas en agua destilada estéril.
Experimento ex vitro
Se emplearon mandarinas de la variedad Río de Oro, provenientes de Huaral. Se seleccionaron 390 frutos homogéneos en color, tamaño y exentos de defectos visuales, y se dividieron aleatoriamente en 36 lotes de 15 frutos. Se desinfectó la superficie de los frutos mediante inmersión en hipoclorito de sodio al 2% (v/v) durante 2 minutos, se enjuagaron con agua corriente y se secaron al aire (Liu et al., 2017). Posteriormente, un lote se utilizó para analizar las características fisicoquímicas de la fruta en el momento de la recolección. Poste-riormente, los cítricos restantes fueron tratados por inmersión en la solución del mucílago correspondiente durante 10 minutos. Transcurrido este tiempo se sacaron y se dejaron secar a temperatura ambiente durante 24 horas. Finalmente, a cada fruto se le inoculó los hongos por aspersión de acuerdo con los tratamientos planteados (Tabla 1).
Almacenamiento
Los frutos se almacenaron en condiciones controladas en una cámara a 25 °C y una humedad relativa de 85% durante 30 días. De manera paralela se realizaron las mediciones de los parámetros de incidencia, pérdida de peso (%), firmeza (kg-f), sólidos solubles (°Brix), pH y color a los 10, 20 y 30 días
Incidencia
Para la determinación de la incidencia, se evaluaron 30 mandarinas al azar y se identificaron los síntomas y signos característicos del hongo. Se consideró mandarina enferma, cuando se presenta pudriciones verdes en la superficie de la mandarina. Luego, con las evaluaciones registradas se determinó la Incidencia, haciendo uso de la fórmula matemática.
![]()
Pérdida de peso
Para calcular la pérdida de peso (%) se empleó una balanza analítica (OHAUS, modelo PR - 224) con dos cifras decimales de precisión ± 0,01 g. La pérdida de peso se calculó en % con respecto al peso inicial de los frutos antes de la conservación (100%).
![]()
Firmeza
Se midió la firmeza de los frutos empleando un Texturómetro TA. HD Plus (Stable Microsystems, UK) equipado con un disco plano de 75mm. Para la realización de la prueba se empleó una deforma-ción de 35% respecto a su diámetro ecuatorial y una velocidad de descenso del disco de 18 mm.min-1.
Sólidos solubles totales (SST)
La medida del contenido de SST se realizó empleando el zumo filtrado de los frutos. Para ello se empleó un refractómetro (KRÜSS DR301–95, Alemania) a 20 °C y los resultados se expresaron en °Brix.
Potencial de hidrógeno (pH)
Se utilizó un pHmetro LR44 digital automático de sensibilidad 0,01 para medir el pH de los frutos.
Espectroscopía Infrarroja por Transformada de Fourier (FTIR)
La muestra de mucílago de nopal se secó a 45 °C durante 24 h en una estufa (Memmert UF55, Alemania), las hojas de llantén frescas se lavaron; ambas muestras se analizaron en un espectrómetro FTIR Nicolet iS50 (Thermo Scientific, Alemania) equipado con el accesorio ATRMiracle diamante de 3 rebotes, en un intervalo de 600 a 4000 cm-1 con una resolución de 4 cm-1 y empleando 16 barridos.
|
Tratamientos |
Concentraciones |
|
TC1 |
Mandarina sin extracto y sin hongo. |
|
TC2 |
Mandarina solo con hongo. |
|
T1 |
Mandarina con extracto de llantén al 1%. |
|
T2 |
Mandarina con extracto de llantén al 5%. |
|
T3 |
Mandarina con mucílago de tuna al 1%. |
|
T4 |
Mandarina con mucílago de tuna al 3%. |
|
T5 |
Mandarina con extracto de llantén al 1% y de mucílago de tuna al 1%. |
|
T6 |
Mandarina con extracto de llantén al 1% y de mucílago de tuna al 3%. |
|
T7 |
Mandarina con extracto de llantén al 5% y de mucílago de tuna al 1%. |
|
T8 |
Mandarina con extracto de llantén al 5% y de mucílago de tuna al 3%. |
RESULTADOS Y DISCUSIÓN
El espectro FTIR del extracto seco de hojas de Plantago major presentó bandas espectrales correspondientes a diversos a grupos funcionales bioactivos. El número de onda de 2900 - 3000 cm⁻¹, se correlaciona con los modos de estiramiento de los enlaces C-H de los grupos metilo, que consisten en CH, CH₂ y CH₃. El espectro que presenta una extensa banda entre 3000 y 3600 cm⁻¹, se atribuye a la vibración de estiramiento de los grupos O-H en ácidos carboxílicos y alcoholes, individualmente (Niknam et al., 2020). El área entre 800 y 1200 cm⁻¹ se denomina área de "huella dactilar" para los carbohidratos. Además, el pico observado alrededor de 1590 cm−1 (estiramiento asimétrico COO−) y 1410 cm−1 (estiramiento simétrico COO−) indica la presencia de ácido urónico (Figura 1A) (Guo et al., 2011).
El espectro FTIR del mucílago extraído de cladodios Opuntia ficus-indica (Figura 1B), muestra una banda ancha alrededor de 3290 cm⁻¹ (estiramiento O–H), y bandas a 2920 cm⁻¹ (estiramiento CH₂). Se observan vibraciones características del grupo carboxilato (COO-) alrededor de 1600 cm⁻¹. También aparecen señales visibles en ~1420 cm⁻¹ y en ~875 cm⁻¹, que indican posible presencia de carbonatos (CO₃²⁻) (Quintero-García et al., 2021).
Los tratamientos que presentaron menor incidencia fueron aquellos que contenían mínimo 3% de mucílago de tuna y/o extracto de llantén. Los cuales fueron T2 (extracto de llantén al 5%), T4 (mucílago de tuna al 3%) y T7 (llantén al 5% y mucílago de tuna al 1%) que presentaron 13,33 % de incidencia. Seguidos por los tratamientos T6 (llantén al 1% y mucílago de tuna al 3%) y T8 (llantén al 5% y mucílago de tuna al 3%) que presentaron un 16.67 % de incidencia (Tabla 2). Ello indica que los recubrimientos evitaron que el Penicillium comience a degradar los tejidos vegetales. Por otro lado, los tratamientos en los cuales la incidencia es el 100%, indican que el patógeno se estableció, desarrolló y desintegró completamente al fruto.
La actividad antimicrobiana del llantén se debió a su componente activo aucubigenina, que se genera a partir de la aucubina, el cual durante el catabolismo crea un dialdehído que actúa como bactericida al desnaturalizar las proteínas de las bacterias orales y los colonizadores de la placa. También contiene varios flavonoides, entre los que se encuentran el acteósido y el plantamajosido, que tienen propiedades antibacterianas (Zhakipbekov et al., 2023). Asimismo, concuerda con estudios en los que se evidencia que los recubrimientos que emplean mucílago de llantén suprimen el crecimiento de bacterias y hongos (Behbahani et al., 2017; Noshad et al., 2021).
Por otra parte, el mucílago de tuna contribuyó a disminuir el porcentaje de incidencia, debido sus compuestos fenólicos que contribuyen a sus actividades antioxidantes y antimicrobianas (Iftikhar et al., 2023).
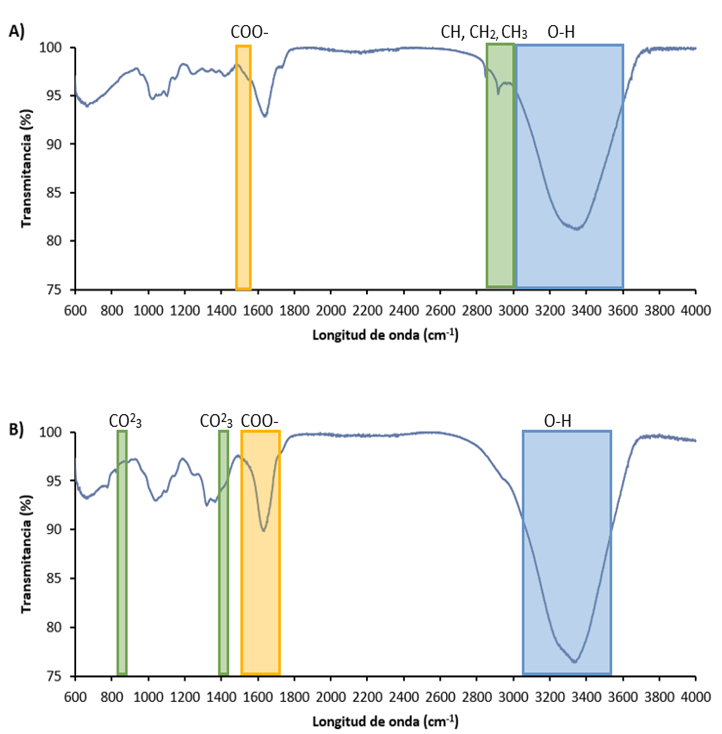
Figura 1. Espectro FTIR. A) Hoja de llantén, B) Mucílago de tuna.
Tabla 2
Incidencia de mandarinas infestadas por Penicillium según tratamientos
|
Tratamientos |
Incidencia (%) |
|
TC1 |
13,33 |
|
TC2 |
100 |
|
T1 |
100 |
|
T2 |
13,33 |
|
T3 |
100 |
|
T4 |
13,33 |
|
T5 |
100 |
|
T6 |
16,67 |
|
T7 |
13,33 |
|
T8 |
16,67 |
La Figura 2 muestra la respuesta visual de las mandarinas tras 30 días de almacenamiento: el control negativo (TC1, A) permanece íntegro sin síntomas, mientras que el control positivo (TC2, B) presenta la máxima colonización fúngica con micelio verde abundante y desintegración de la epidermis. Los tratamientos con recubrimientos vegetales reducen notablemente la incidencia comparados con TC2; así, T1 (llantén al 1 %) exhibe una reducción moderada de lesiones, T2 (llantén 5 %) muestra un efecto más marcado dependiente de la concentración, y T3 (mucílago de tuna al 1%) también disminuye la aparición de moho probablemente por la formación de una película semipermeable que limita la pérdida de agua y la respiración del fruto. La combinación de ambos extractos (T5, llantén 1% y mucílago 1%) pero en menores concentraciones presenta una ligera inhibición del hongo en comparación con el control positivo (TC2). En general, los tratamientos empleando recubrimientos presentaron una menor extensión visible de pudrición, sugiriendo un efecto sinérgico entre la barrera física del mucílago y los compuestos bioactivos del llantén que pueden añadir actividad antifúngica o moduladora de defensas. Estos resultados concuerdan con estudios previos que muestran que recubrimientos a base de mucílagos (por ejemplo, Opuntia ficus-indica) prolongan la vida útil de cítricos mediante mecanismos físicos y bioquímicos (Allegra et al., 2016; Papoutsis et al., 2019).
En la Figura 3A se presenta la pérdida fisiológica de peso (%) que aumentó con el almacenamiento en todos los tratamientos debido a la pérdida continua de humedad causada por la transpiración y la respiración (Barsha et al., 2021). Además, se observa que los tratamientos T2 (llantén al 5%) y T8 (llantén al 5% y mucílago de tuna al 3%) presentaron los valores más bajos de pérdida de peso de 5,67% y 6,03% después de los 30 días de almacenamiento, respectivamente. Lo que concuerda con estudios sobre recubrimientos comestibles a base de cera y nanoemulsiones con aceites esenciales, los cuales reducen significativamente la pérdida de agua, por debajo del 20%, manteniendo la calidad en mandarinas durante 30 días de almacenamiento (Devi et al., 2025).
En la Figura 3B, se observó que el T8 mantienen firmeza estable cerca de 6,000 kg-f, mientras que T3 (mucílago de tuna al 1%), T5 (llantén al 1% y mucílago de tuna al 1%) y control positivo (TC2) se desmoronan rápidamente. Esto corrobora estudios que muestran que los recubrimientos comestibles limitan la biosíntesis de etileno y reducen la tasa de respiración y la pérdida de agua, salvaguardando la turgencia celular y la firmeza del fruto (Kumar et al., 2024). Por ejemplo, En otro estudio, recubrimientos de quitosano nanométrico con cera mantenían mejor firmeza y menor pérdida de peso en mandarinas comparados con controles, preservando textura y calidad sensorial (Al et al., 2024).

Figura 2. Incidencia de mandarinas infestadas por Penicillium digitatium según tratamientos a los 30 días. A) TC1: Mandarina sin extracto y sin hongos. B) TC2: Mandarina solo con hongos. C) T1: Mandarina con extracto de llantén al 1%. D) T2: Mandarina con extracto de llantén al 5%. E) T3: Mandarina con extracto de mucílago de tuna al 1%. F) T5: Mandarina con extracto de llantén al 1% y de mucílago de tuna al 1%.
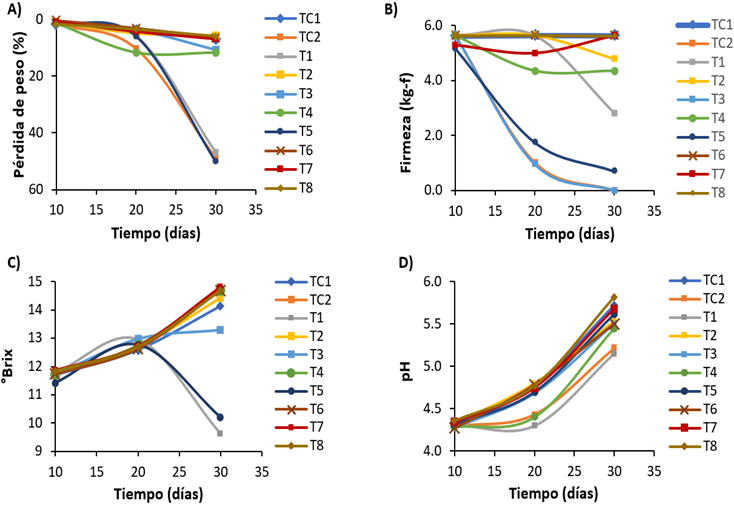
Figura 3. Promedio de determinaciones analíticas de los frutos durante su almacenamiento. A) pérdida de peso (%). B) Firmeza (Kg-f). C) °Brix, D) pH.
En la Figura 3C se observa que a medida que aumentan los días de almacenamiento aumentan los SST de los frutos en todos los tratamientos, excepto T1 (llantén al 1%) y T5 (llantén al 1% y mucílago de tuna al 1%), en los cuales se presenta una disminución a los 30 días. El aumento de los SST, se atribuye a la conversión de almidón y otros carbohidratos insolubles en sólidos solubles (Barsha et al., 2021). Por otro lado, en el caso de los tratamientos T1 (llantén al 1%) y T5(llantén al 1% y mucílago de tuna al 1%) en los cuales se presenta una disminución de SST después de los 20 días. Siendo que estos dos tratamientos presentaron los valores más altos de incidencia (100%) y pérdida de peso (T1 (46,95%) y T5 (50,13%)). Se podría atribuir a que el efecto del recubrimiento fue menos eficiente lo cual permitió un consumo continuo mayor de azúcares como sustratos durante la respiración, lo que disminuyó el contenido de sólidos solubles (Wei et al., 2021).
En la Figura 3D se aprecia que el pH de los frutos tiende a aumentar a lo largo de los días de almacenamiento, lo que refleja una reducción progresiva de la acidez titulable, mientras que los grados Brix (indicadores de contenido de azúcares solubles como sacarosa) aumentan. Este comportamiento, común en frutas durante la conservación, se explica por la degradación de ácidos orgánicos y su potencial conversión en azúcares u otros metabolitos, lo que en conjunto eleva el pH al disminuir la acidez. Este patrón ha sido reportado en pitahaya (Hylocereus spp.), donde se observó un incremento del pH de aproximadamente 4,42 a 5,09, mientras los sólidos solubles totales (°Brix) se mantuvieron o aumentaron levemente durante el almacena-miento bajo temperatura ambiente, demostrando la relación inversa entre acidez y contenido de azúcares (Chen et al., 2024).
En la Tabla 3 se comparan los principales resultados obtenidos en el presente estudio con otros estudios realizados en frutos empleando recubrimientos. Se observa que la aplicación de recubrimientos comestible en frutos permite prolongar su vida útil, debido a que reducen significativamente la pérdida de peso durante el almacenamiento, relacionada directamente con la firmeza. Además, mejoran las propiedades de barrera lo cual se evidencia en una menor incidencia de infestación por hongos. Por otra parte, los parámetros fisicoquímicos (pH, SST y acidez) presentan mayor estabilidad lo que indica una mejor conservación de los frutos.
Tabla 3
Estudios comparativos de aplicación de recubrimientos en frutos
|
Fuente |
Aplicación/ concentración |
Fruta |
Condiciones de almacena-miento |
Parámetros evaluados |
Resultados clave |
Refe-rencia |
|
Opuntia ficus-indica mucílago y extracto de llantén |
Inmersión/ solución de mucílago de tuna (1% y 3%) y extracto de llantén (1% y 5%) |
Mandarinas (Citrus reticulata Blanco) |
Temperatura ambiente a 25 °C y 85 % de humedad relativa |
Firmeza pH SST Pérdida de peso |
Menor incidencia (%) Valores de firmeza mayores pH y SST estables Menor pérdida de peso |
Presente estudio |
|
glucomanano de konjac + aceite esencial de Ocimum gratissimum |
Inmersión/ konjac glucomannan y aceite esencial en distintas concentraciones (0,5–1,5%) |
Naranja |
25 ± 1 °C y humedad relativa del 90 ± 1 % |
Pérdida de peso, firmeza, respiración, vitamina C, parámetros antioxidantes
|
Menor pérdida de peso Mayor firmeza Mejores valores de vitamina C Mejores parámetros antioxidantes |
(Yu et al., 2025) |
|
Suero de leche, agar, almidón de yuca y glicerol |
Inmersión/ Solución combinada de proteínas + polisacáridos |
Banano (Musa paradisiaca) |
13 °C, 95% humedad relativa |
Pérdida de peso, firmeza, color, pH, SST, acidez titulable |
Menor pérdida de peso Mayor firmeza Mejor retención de color
|
(Ruiz Medina et al., 2025) |
|
Opuntia ficus-indica mucílago + gel de Aloe |
Inmersión/ mucílago + Aloe gel + glicerol |
Higos frescos (Ficus carica L.) |
Almacenamiento en frío (4 °C) |
Pérdida de peso, firmeza, carga microbiana, apariencia visual |
Mayor firmeza Menor pérdida de peso Menor carga microbiana. |
(Sortino et al., 2024) |
|
Opuntia ficus-indica mucílago (polvo) |
Inmersión/ 1%, 2%, 3% (w/v) con glicerol |
Banana (Musa spp.) |
Temperatura ambiente (~23 °C) y 85% de humedad relativa |
Peso, firmeza, etileno, respiración, enzimas pectinas |
Menor degradación de la pared celular Mayor firmeza Menor tasa respiratoria |
(Shinga & Fawole, 2023) |
|
Opuntia ficus-indica mucílago + lisozima |
Inmersión/ Fórmulas con 0-1 % lisozima |
Papaya (Carica papaya L.) |
Almacenamiento a temperatura ambiente |
Pérdida de peso, SST, pH, acidez, carga microbiana (S. aureus) |
Menor pérdida de peso Restricción significativa de S. aureus. |
(Yadav et al., 2023) |
|
Opuntia ficus-indica mucílago |
Pulverización / atomización/ Solución acuosa de mucílago |
Níspero (Eriobotrya japonica Lindl.) |
Almacenamiento en frío (5 °C) |
Firmeza, SST, acidez, color, microbiología, parámetros nutracéuticos |
Mayor firmeza SST, acidez y fenoles estables Menor recuento microbiano. |
(Liguori et al., 2022) |
*SST: sólidos solubles totales.
CONCLUSIONES
El uso de recubrimientos comestibles elaborados con mucílago de tuna y extracto de llantén permitió reducir significativamente la pérdida de peso y preservar la calidad de mandarinas inoculadas con Penicillium digitatum durante 30 días de almace-namiento a temperatura ambiente (25 °C y 85% de humedad relativa).
Se identificó que el tratamiento con extracto de llantén al 5%, y la combinación de extracto de llantén al 5% con mucílago de tuna al 3%, mostraron los menores porcentajes de pérdida de peso, con valores de 5,67% y 6,03%, respec-tivamente, evidenciando un efecto protector frente a la deshidratación y el deterioro poscosecha. Además, presentaron los mejores valores de firmeza y sólidos solubles al cabo de los 30 días.
Se concluyó que un recubrimiento a base de mucílago de tuna y extracto de llantén permite conservar las características fisicoquímicas de los frutos de mandarinas. Estos resultados confirman el potencial de los recubrimientos naturales como estrategia sostenible para prolongar la vida útil de frutas cítricas y reducir las pérdidas durante su comercialización, y sugiere la posibilidad de evaluar su efectividad en otros frutos perecibles y bajo condiciones reales de transporte, almace-namiento y distribución comercial.
REFERENCIAS BIBLIOGRÁFICAS
Abu-Shama, H. S., Abou-Zaid, F. O. F., & El-Sayed, E. Z. (2020). Effect of using edible coatings on fruit quality of Barhi date cultivar. Scientia Horticulturae, 265, 109262.
Al, N. A., Gad, M. M., Fikry, A. M., Ezzat, A., El-tarabily, A., Elakkad, H. A., & Eid, I. (2024). Saudi Journal of Biological Sciences Efficacy of chitosan nanoparticles and wax coatings on maintaining post-harvest quality of “ Murcott ” mandarins. Saudi Journal of Biological Sciences, 31(2), 103894. https://doi.org/10.1016/j.sjbs.2023.103894
Albahri, G., Badran, A., Hijazi, A., Daou, A., Baydoun, E., Nasser, M., & Merah, O. (2023). The Therapeutic Wound Healing Bioactivities of Various Medicinal Plants. Life, 13(2). https://doi.org/10.3390/life13020317
Allegra, A., Inglese, P., Sortino, G., Settanni, L., Todaro, A., & Liguori, G. (2016). The influence of Opuntia ficus-indica mucilage edible coating on the quality of “Hayward” kiwifruit slices. Postharvest Biology and Technology, 120, 45–51. https://doi.org/10.1016/j.postharvbio.2016.05.011
Barsha, D. C., Singh, M., Khanal, P., Pandey, M., & Pathak, R. (2021). Effect of Different Edible Coatings on Postharvest Quality of Mandarin Orange (Citrus reticulata Blanco). Agro Bali : Agricultural Journal, 4(2), 136–144. https://doi.org/10.37637/ab.v4i2.695
Behbahani, B. A., Shahidi, F., Yazdi, F. T., Mortazavi, S. A., & Mohebbi, M. (2017). Use of Plantago major seed mucilage as a novel edible coating incorporated with Anethum graveolens essential oil on shelf life extension of beef in refrigerated storage. International Journal of Biological Macromolecules, 94, 515–526. https://doi.org/10.1016/j.ijbiomac.2016.10.055
Chen, S. Y., Islam, M. A., Johnson, J. B., Xu, C. Y., Mazhar, M. S., & Naiker, M. (2024). Comparative Analysis of Shelf-Life, Antioxidant Activity, and Phytochemical Contents of Australian-Grown and Imported Dragon Fruit under Ambient Conditions. Horticulturae, 10(10). https://doi.org/10.3390/horticulturae10101048
Devi, L. S., Mukherjee, A., Dutta, D., & Kumar, S. (2023). Carnauba wax-based sustainable coatings for prolonging postharvest shelf-life of citrus fruits†. Sustainable Food Technology, 1(3), 415–425. https://doi.org/10.1039/d2fb00049k
Devi, L. S., Mukherjee, A., Sharma, S., Katiyar, V., Dutta, J., & Kumar, S. (2025). Natural wax-based edible coatings for preserving postharvest quality of mandarin orange. Food Chemistry: X, 26(January), 102302. https://doi.org/10.1016/j.fochx.2025.102302
Guo, Q., Cui, S. W., Wang, Q. I., Hu, X., Guo, Q., Kang, J. I., & Yada, R. (2011). Extraction, fractionation and physicochemical characterization of water-soluble polysaccharides from Artemisia sphaerocephala Krasch seed. Carbohydrate Polymers, 86(2), 831–836.
Iftikhar, K., Siddique, F., Ameer, K., Arshad, M., Kharal, S., Mohamed Ahmed, I. A., Yasmin, Z., & Aziz, N. (2023). Phytochemical profiling, antimicrobial, and antioxidant activities of hydroethanolic extracts of prickly pear (Opuntia ficus indica) fruit and pulp. Food Science and Nutrition, 11(4), 1916–1930. https://doi.org/10.1002/fsn3.3226
Karnwal, A., Kumar, G., Singh, R., Selvaraj, M., Malik, T., & Al Tawaha, A. R. M. (2025). Natural biopolymers in edible coatings: Applications in food preservation. Food Chemistry: X, 25(November 2024), 102171. https://doi.org/10.1016/j.fochx.2025.102171
Kharchoufi, S., Parafati, L., Licciardello, F., Muratore, G., Hamdi, M., Cirvilleri, G., & Restuccia, C. (2018). Edible coatings incorporating pomegranate peel extract and biocontrol yeast to reduce Penicillium digitatum postharvest decay of oranges. Food Microbiology, 74, 107–112. https://doi.org/10.1016/j.fm.2018.03.011
Kumar, N., Upadhyay, A., Shukla, S., Bajpai, V. K., Kieliszek, M., Yadav, A., & Kumaravel, V. (2024). Next generation edible nanoformulations for improving post-harvest shelf-life of citrus fruits. Journal of Food Measurement and Characterization, 18(3). https://doi.org/10.1007/s11694-023-02287-8
Liguori, G., Gaglio, R., Greco, G., Gentile, C., Settanni, L., & Inglese, P. (2021). Effect of Opuntia ficus-indica Mucilage Edible Coating on Processed Cactus Pear Fruits. Agronomy, 11(1963), 1–16. https://www.mdpi.com/journal/agronomy
Liguori, G., Gaglio, R., Settanni, L., Inglese, P., D’Anna, F., & Miceli, A. (2021). Effect of Opuntia ficus-indica Mucilage Edible Coating in Combination with Ascorbic Acid, on Strawberry Fruit Quality during Cold Storage. Journal of Food Quality, 2021. https://doi.org/10.1155/2021/9976052
Liguori, G., Greco, G., Gaglio, R., Settanni, L., Inglese, P., & Allegra, A. (2022). Influence of Cactus Pear Mucilage-Based Edible Coating on Marketability and Edibility Parameters of Minimally Processed Loquat Fruits. Agronomy, 12(9). https://doi.org/10.3390/agronomy12092120
Liu, K., Zhou, X., & Fu, M. (2017). Inhibiting effects of epsilon-poly-lysine (ε-PL) on Pencillium digitatum and its involved mechanism. Postharvest Biology and Technology, 123, 94–101. https://doi.org/10.1016/j.postharvbio.2016.08.015
Niknam, R., Ghanbarzadeh, B., Ayaseh, A., & Rezagholi, F. (2020). Barhang (Plantago major L.) seed gum: Ultrasound-assisted extraction optimization, characterization, and biological activities. Journal of Food Processing and Preservation, 44(10), 1–15. https://doi.org/10.1111/jfpp.14750
Noshad, M., Alizadeh Behbahani, B., Jooyandeh, H., Rahmati-Joneidabad, M., Hemmati Kaykha, M. E., & Ghodsi Sheikhjan, M. (2021). Utilization of Plantago major seed mucilage containing Citrus limon essential oil as an edible coating to improve shelf-life of buffalo meat under refrigeration conditions. Food Science and Nutrition, 9(3), 1625–1639. https://doi.org/10.1002/fsn3.2137
Papoutsis, K., Mathioudakis, M. M., Hasperué, J. H., & Ziogas, V. (2019). Non-chemical treatments for preventing the postharvest fungal rotting of citrus caused by Penicillium digitatum (green mold) and Penicillium italicum (blue mold). Trends in Food Science and Technology, 86(March), 479–491. https://doi.org/10.1016/j.tifs.2019.02.053
Prisa, D. (2021). Opuntia ficus-indica the key plant in climate change: characteristics, cultivation and uses. GSC Biological and Pharmaceutical Sciences, 17(2), 094–105. https://doi.org/10.30574/gscbps.2021.17.2.0333
Quintero-García, M., Gutiérrez-Cortez, E., Bah, M., Rojas-Molina, A., Cornejo-Villegas, M. de los A., Real, A. Del, & Rojas-Molina, I. (2021). Comparative analysis of the chemical composition and physicochemical properties of the mucilage extracted from fresh and dehydrated opuntia ficus indica cladodes. Foods, 10(9), 1–18. https://doi.org/10.3390/foods10092137
Rafiq, S., Kaul, R., Sofi, S. A., Bashir, N., Nazir, F., & Ahmad Nayik, G. (2018). Citrus peel as a source of functional ingredient: A review. Journal of the Saudi Society of Agricultural Sciences, 17(4), 351–358. https://doi.org/10.1016/j.jssas.2016.07.006
Ruiz Medina, M. D., Quimbita Yupangui, Y., & Ruales, J. (2025). Effect of a Protein–Polysaccharide Coating on the Physicochemical Properties of Banana (Musa paradisiaca) During Storage. Coatings, 15(7). https://doi.org/10.3390/coatings15070812
Shinga, M. H., & Fawole, O. A. (2023). International Journal of Biological Macromolecules Opuntia ficus indica mucilage coatings regulate cell wall softening enzymes and delay the ripening of banana fruit stored at retail conditions. International Journal of Biological Macromolecules, 245(April), 125550. https://doi.org/10.1016/j.ijbiomac.2023.125550
Sortino, G., Guccione, E., Casales, F. G., de Chiara, M. L. V., Passafiume, R., Gallotta, A., & Allegra, A. (2024). Application of Opuntia ficus-indica Mucilage and Aloe Gel-Based Edible Coating to Enhance Postharvest Quality and Microbiological Aspects of Fresh Figs (Ficus carica L.). Horticulturae, 10(5). https://doi.org/10.3390/horticulturae10050482
Sortino, G., Inglese, P., Farina, V., Passafiume, R., & Allegra, A. (2022). The Use of Opuntia ficus-indica Mucilage and Aloe arborescens as Edible Coatings to Improve the Physical, Chemical, and Microbiological Properties of ‘Hayward’ Kiwifruit Slices. Horticulturae, 8(3). https://doi.org/10.3390/horticulturae8030219
Wei, S., Mei, J., & Xie, J. (2021). Effects of edible coating and modified atmosphere technology on the physiology and quality of mangoes after low-temperature transportation at 13 °C in vibration mitigation packaging. Plants, 10(11). https://doi.org/10.3390/plants10112432
Yadav, D., Dagadkhair, A., Shere, P., & Patil, V. (2023). Effect of lysozyme based Opuntia ficus-indica mucilage edible coating on shelf life of papaya (Carica papaya L.) fruits. Journal of Postharvest Technology, 11(3), 110–118.
Yu, X., Zhu, J., Wu, J., Cheng, Y., Gao, Y., Liu, Y., & Jiang, F. (2025). Edible Coating Based on Konjac glucomannan Loading Ocimum gratissimum Essential Oil for Postharvest Preservation of Orange. Polymers, 17(9). https://doi.org/10.3390/polym17091217
Zhakipbekov, K., Turgumbayeva, A., Issayeva, R., Kipchakbayeva, A., Kadyrbayeva, G., Tleubayeva, M., Akhayeva, T., Tastambek, K., Sainova, G., Serikbayeva, E., Tolenova, K., Makhatova, B., Anarbayeva, R., Shimirova, Z., & Tileuberdi, Y. (2023). Antimicrobial and Other Biomedical Properties of Extracts from Plantago major, Plantaginaceae. Pharmaceuticals, 16(8), 1–21. https://doi.org/10.3390/ph16081092