 |
INTRODUCCIÓN
Registro de Parasaissetia nigra, Pulvinaria psidii y Dysmicoccus brevipes (Hemiptera: Coccidae, Pseudococcidae) infestando mangle blanco Laguncularia racemosa
Record of Parasaissetia nigra, Pulvinaria psidii and Dysmicoccus brevipes (Hemiptera: Coccidae, Pseudococcidae) infesting white mangrove Laguncularia racemosa
Pedro S. Castillo-Carrillo1*; Walter Díaz Burga2; Fiorela Cano Carrillo1; Edgar A. Coveñas Rumiche1; Jorge L. Purizaga Preciado1
1 Museo Entomológico, Facultad de Ciencias Agrarias, Universidad Nacional de Tumbes. Campus La Cruz Corrales, Tumbes, Perú.
2 Consultor privado. Lima, Perú.
* Autor corresponsal: pcastilloc@untumbes.edu.pe (P. S. Castillo-Carrillo).
ORCID de los autores:
P. S. Castillo-Carrillo: http://orcid.org/0000-0002-0255-1047 W. Diaz Burga: http://orcid.org/0009-0005-3611-9075
F. Cano Carrillo: http://orcid.org/0009-0008-3928-4975 E.A. Coveñas Rumiche: http://orcid.org/0009-0007-3629-1777
J. L. Purizaga Preciado: http://orcid.org/0000-0003-1160-3715
RESUMEN
Se reporta el registro de tres especies de insectos escama (Hemiptera) infestando el mangle blanco (Laguncularia racemosa) en el ecosistema de manglar de Tumbes, Perú. Las especies identificadas son: Dysmicoccus brevipes (Familia Pseudococcidae - cochinilla harinosa de la piña), plaga polífaga conocida por dañar cultivos tropicales, ahora observada en mangle blanco. Pulvinaria psidii (Familia Coccidae - cochinilla algodonosa de la guayaba), especie invasora grave que afecta a numerosas plantas leñosas, incluyendo frutales y Parasaissetia nigra (Familia Coccidae - cochinilla negra), plaga común en diversas plantas ornamentales y frutales. Este hallazgo es significativo porque amplía el rango de plantas hospedantes conocidas para estas plagas, especialmente D. brevipes y P. psidii, cuya asociación con L. racemosa no estaba documentada previamente en Perú. Constituye el primer reporte de estas tres especies co-infestando L. racemosa en la región de Tumbes. Destaca una potencial nueva presión fitosanitaria para los manglares de Tumbes, un ecosistema crítico y ya vulnerable. La infestación por cochinillas puede debilitar los árboles, reducir su crecimiento y fotosíntesis, haciéndolos más susceptibles a otros factores ambientales o patógenos. El estudio subraya la necesidad de monitorear estas plagas para evaluar su impacto real en la salud del manglar y la importancia de la identificación temprana para posibles medidas de manejo en este frágil ecosistema costero peruano.
Palabras clave: Coccidae; cochinillas; infestación mangle; Laguncularia racemosa, Sternorhyncha.
ABSTRACT
Three species of scale insect (Hemiptera) are reported to be infesting white mangrove (Laguncularia racemosa) in the mangrove ecosystem of Tumbes, Peru: Dysmicoccus brevipes (Pseudococcidae family – pineapple mealybug), a polyphagous pest known for damaging tropical crops, now observed on mangroves; Pulvinaria psidii (Coccidae family – guava mealybug), a serious invasive species affecting numerous woody plants including fruit trees; and Parasaissetia nigra (Coccidae family – nigra scale), a common pest on diverse ornamental and fruit plants. This finding significantly expands the known host plant range for these pests, particularly D. brevipes and P. psidii, whose association with L. racemosa was previously undocumented in Peru. It also represents the first report of these three species co-infesting L. racemosa in the Tumbes region, highlighting a potential new phytosanitary threat for these critical and already vulnerable mangroves. Scale infestation can weaken trees by reducing growth and photosynthesis, thereby increasing susceptibility to other environmental stressors or pathogens. The study emphasizes the need to monitor these pests to assess their actual impact on mangrove health and underscores the importance of early detection for potential management measures in this fragile Peruvian coastal ecosystem.
Keywords: Coccidae ; Laguncularia racemosa; mangrove infestation; scale insects; Sternorrhyncha
Recibido: 09-12-2025.
Aceptado: 28-03-2026.
Los manglares del noroeste peruano, particu-larmente los de la región de Tumbes, representan la mayor extensión de este ecosistema en el país (Martínez, 2022; Seminario-Córdova et al., 2022). Estos constituyen ecosistemas críticos que brindan servicios ecosistémicos esenciales, tales como la protección costera, el mantenimiento de criaderos para especies marinas y la mitigación del cambio climático, al actuar como importantes sumideros de carbono azul (Alongi, 2008; Barbier, 2012; Zhila et al., 2014; Bunting et al., 2022; Arnaud et al., 2023; Rull, 2023).
En los manglares de Tumbes se encuentran presentes diversas especies de mangle: mangle rojo (Rhizophora mangle), mangle negro (Avicennia germinans), mangle blanco (Laguncularia racemosa), mangle colorado (Rhizophora harrisonii) y mangle botón o piña (Conocarpus erectus) (Takahashi y Grimaldo, 2015). L. racemosa (L.) C.F. Gaertn., denominada comúnmente como mangle blanco, es una especie que se encuentra en menor proporción en estos ecosistemas (Dioses-Puelles et al., 2023). Actualmente, esta especie enfrenta amenazas crecientes debido al cambio climático y a diversas actividades antropogénicas (Spalding, 2010). A estas presiones ambientales se suma ahora el reporte de plagas que afectan su fitosanidad.
Los insectos escama (Hemiptera: Coccomorpha, superfamilia Coccoidea) representan plagas agrícolas globales con un alto potencial invasor en ecosistemas naturales (García Morales et al., 2016). El suborden Sternorrhyncha agrupa, además, a otras cuatro superfamilias que incluyen a los principales artrópodos fitófagos: Aphidoidea (pulgones), Phylloxeroidea (adélgidos y filoxeras), Aleyrodoidea (moscas blancas) y Psylloidea (psílidos o "algodones") (Pérez et al., 2015).
Especies como Pulvinaria psidii han demostrado una alta adaptabilidad a nuevos hospederos, llegando a causar la mortalidad de plantas leñosas (Tanaka & Kondo, 2015). P. psidii fue descrita originalmente en Hawái sobre Psidium sp. y, actualmente, se encuentra establecida en numerosos países de las regiones tropicales y subtropicales del mundo (Bragard et al., 2022). En Perú, Diaz Villa (2017) registra a P. psidii en Schinus terebinthifolius (“molle brasileño”) y Schinus molle (“molle serrano”). Del mismo modo, Huamán Tunante (2022) también la reportó afectando a S. molle L., pero su incidencia en manglares permanecía inexplorada. Aunque existen registros de Coccidae en manglares del Atlántico (e.g., sobre Avicennia germinans en Brasil; Reis et al., 2020), la interacción específica con L. racemosa en el Pacífico sudeste carecía de evidencia científica previa.
Dysmicoccus es un género de cochinillas de la familia Pseudococcidae, la cual ocupa el segundo lugar en número de especies dentro de la superfamilia Coccoidea, después de Diaspididae (García Morales et al., 2016). La mayoría de sus integrantes son polífagos y poseen el potencial de causar daños económicos en diversos hospederos, ya que pueden residir y reproducirse en todos los órganos de la planta, incluidas las raíces (Sartiami, 2006). Una de las especies más relevantes de este género es la cochinilla harinosa de la piña, conocida científicamente como Dysmicoccus brevipes (Cockerell). Esta especie puede asociarse con todos los órganos de la planta y desempeña un rol crucial como vector de fitopatógenos, lo que incrementa su importancia económica y sanitaria (Sudiarta et al., 2025).
Por su parte, Parasaissetia nigra ha sido reportada en diversos cultivos y plantas ornamentales, incluyendo el caucho, la caoba, la higuera y el romero. Actualmente, se continúan registrando nuevas asociaciones con plantas hospederas en distintas regiones del mundo, como Italia, Brasil, Irak y Colombia (Abdul-Rassoul & Al-Mallo, 2016; Junior et al., 2019; Mazzeo et al., 2020).
La presencia simultánea de insectos escama y cochinillas harinosas productoras de melaza favorece el desarrollo de fumagina, un hongo epífito que reduce la capacidad fotosintética y el vigor general de las plantas. Este efecto se ha documentado ampliamente para las familias Coccidae y Pseudococcidae, incluyendo especies como P. psidii, P. nigra y D. brevipes (Malumphy, 2002; Sudiarta et al., 2025). El presente estudio provee el primer registro de esta triada en manglares peruanos, alertando sobre un posible riesgo fitosanitario para la conservación de L. racemosa y la estabilidad de este ecosistema altamente vulnerable (UICN, 2023).
METODOLOGÍA
Durante una visita realizada en julio de 2025 a las áreas de manglar en el sector El Bendito (cerca al Santuario Nacional Los Manglares, Distrito y Provincia de Zarumilla, Región de Tumbes; coordenadas: 03º 27’ 2.064” S, 80º 19’ 1.626” W) con fines de otros estudios, se detectaron ramas de Laguncularia racemosa (Combretaceae) (Figura 1), infestadas con tres especies de cochinillas (queresas), siendo la más abundante la del género Parasaissetia (Coccidae).

Figura 1. Árbol de mangle blanco (Laguncularia racemosa).
Se recolectaron varias ramitas del hospedero que contenían ejemplares de Parasaissetia sp. (Figuras 2a, b), Pulvinaria sp. (Figura 3a-d) y algunos pseudocóccidos del género Dysmicoccus (Figura 3e). Estas se depositaron en un recipiente plástico con tapa de tul para su aireación. Del material recolectado se seleccionaron para preservación aproximadamente 20 hembras de Parasaissetia sp., cinco ejemplares de Pulvinaria sp. (ambos Coccidae) y tres de Pseudococcidae. Todas las muestras se conservaron en frascos de vidrio con alcohol al 70%.
Para las preparaciones microscópicas, se siguieron las técnicas convencionales de clarificación, tinción, deshidratación y montaje permanente en bálsamo de Canadá, adaptadas de Williams & Watson (1988) y Miller & Davidson (2005). Para el montaje, se utilizó un estereoscopio binocular marca Euromex (modelo ED-1302-P). Una vez procesada, la muestra fue observada a diferentes aumentos en un microscopio compuesto binocular marca Eurolab (modelo DN-117M) con cámara fotográfica incorporada. Igualmente se pudo observar que varios ejemplares de las queresas de Parasaissetia habían sido parasitadas por varias especies de himenópteros de las familias Eulophidae y Encyrtidae.

Figura 2. Parasaissetia nigra: (a) en ramas del árbol de mangle blanco (Laguncularia racemosa), (b) vista ampliada de queresas.
Métodos
La identificación de cóccidos se realizó siguiendo las claves de Hamon & Williams (1984); Gill (1988); Hodgson (1994); Kondo & Gullan (2010).

Figura 3. Pulvinaria psidii: (a) ninfa, (b)ninfa secretando cera, (c) hembras con ovisaco. (d) huevos en ovisaco. (e) hembra adulta de Dysmicoccus.
RESULTADOS Y DISCUSIÓN
Parasaissettia nigra (Nietner)
Material examinado. Perú: Tumbes, Zarumilla, El Bendito, 28. VI. 2025, recolector. P. S. Castillo, Laguncularia racemosa, 10 (♀) adultas. Basado en las llaves de Hodgson (1994), Ben-Dov & Hodgson (1997) y Williams & Watson (1990) se llegó a determinar que la especie pertenecía a la familia Coccidae y a la especie Parasaissetia nigra (Nietner). En la Figura 5 se presentan algunos detalles de las observaciones realizadas en el microscopio.
Distribución y hospederos
En la zona tropical del Pacífico Sur, esta especie es probablemente una de las cochinillas más comunes en plantas leñosas. Cohic (1955) y Reboul (1976) mencionaron que era una plaga específica de la yuca (Manihot esculenta) en la Polinesia Francesa. En Fiji, se reportó en guayaba (Lever, 1946) y, en Nueva Caledonia, Cohic (1956) analizó su importancia en Coffea spp. y Ficus spp. También se ha registrado como plaga del café en Papúa Nueva Guinea (Barrie, 1956) y como causante de la muerte regresiva de los brotes de Hevea brasiliensis (Anon, 1969). En Tonga, O'Connor (1949) indicó su presencia en cantidades considerables sobre M. esculenta.
Ben-Dov & Hodgson (1997) y Lin et al. (2015) reportan que es un insecto polífago que se alimenta de plantas de más de 80 familias. Se cree que la especie se originó en África (Malumphy, 2002), aunque actualmente se encuentra distribuida por todo el mundo. Es una plaga importante de plantas ornamentales y de invernadero (Ben-Dov & Hodgson, 1997), así como de frutales y otras plantaciones en países tropicales y subtropicales (Hamon, 1984; Shree & Manjunatha, 2000). Asimismo, se considera una plaga moderada de varios cultivos en regiones templadas (Malumphy, 2002). P. nigra también ha sido identificada como una especie potencialmente invasora en áreas de vulnerabilidad ambiental, como las Islas Galápagos (Causton et al., 2006). La infestación puede reducir el vigor de los hospederos al agotar sus reservas de savia; además, la mielada producida constituye un sustrato ideal para el crecimiento de fumagina, la cual puede reducir el valor comercial de los productos (Malumphy, 2002).
Diagnosis de la especie
Granara de Willink (1999), proporciona una descripción bastante detallada de la especie en el micro montaje e indica que la forma del cuerpo es oval redondeado, convexo, dermis en mosaico, muy esclerosada en los adultos y de coloración castaño oscuro. (Figura 5). Del mismo modo proporciona información para las superficies dorsal y ventral.
Superficie dorsal: Setas marginales largas y fimbriadas; presencia de tubérculos submarginales en cabeza, tórax y abdomen. Setas de la superficie cilíndricas, con ápice redondeado y de longitud variable. Poros discoidales grandes y preoperculares, escasos; poros biloculares de contorno ovalado, dispersos en la superficie. Placas anales con cuatro setas apicales, tres subapicales y tres en el borde del pliegue anal, estas últimas muy largas; anillo anal con seis setas.
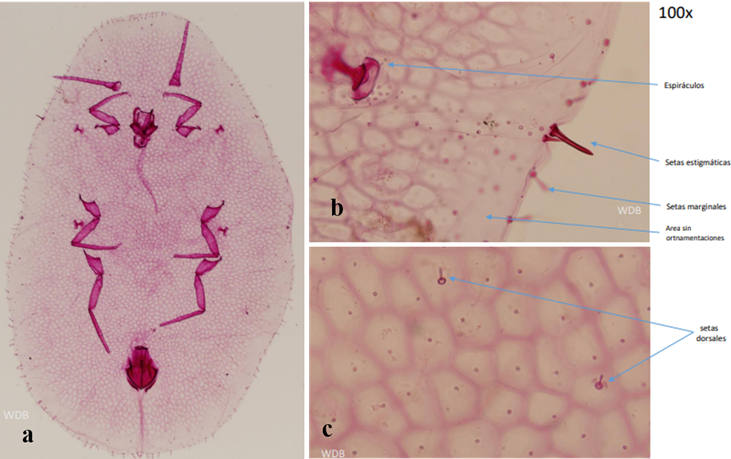
Figura 5. Parasaissetia nigra: (a)hembra a 40x, (b) espiráculos, setas estigmáticas, setas marginales, área sin ornamentación. 100x, (c) setas dorsales. 100x.
Superficie ventral: Patas sin esclerotización tibio-tarsal y con articulación; antenas largas, de ocho segmentos. Setas de la superficie dispersas, delgadas y dispuestas en banda submarginal; setas interantenales (2) y prevulvares (3). Canal estigmático con poros quinqueloculares y tres setas estigmáticas (la media de mayor longitud que las laterales), todas con ápice puntiagudo. Poros multiloculares (con 10 lóculos) presentes en la zona de la vulva y en los segmentos abdominales, aunque no son abundantes. Conductos tubulares con filamento terminal en forma de flor, restringidos a la banda submarginal en cabeza, tórax y abdomen. Microconductos de contorno circular dispersos por toda la superficie. La misma autora reporta que esta especie es cosmopolita y que afecta a numerosos hospederos, y que en su país (Argentina) podría ser confundida con espe-cies del género Saissetia pero la presencia de una seta discal que caracteriza a ese género y del que carece Parasaissetia, las diferencia rápidamente.
Pulvinaria psidii (Maskell)
Material examinado. Perú: Tumbes, Zarumilla, El Bendito, 28. VI. 2025, recolector. J. L. Purizaga, Laguncularia racemosa, 10 (♀) adultas. Basado en las llaves taxonómicas de Tanaka & Kondo (2015), se determinó que los ejemplares pertenecen a la familia Coccidae y a la especie Pulvinaria psidii (Maskell). En la Figura 6a-c se presentan algunos detalles de las observaciones microscópicas realizadas.
Diagnosis de la especie
Tanaka & Kondo (2015) indican que la hembra presenta conductos tubulares ventrales frecuentes y ampliamente distribuidos en el área submarginal de la cabeza. Los poros multiloculares poseen, principalmente, entre 9 y 11 lóculos cada uno. Las setas marginales suelen estar fuertemente fimbriadas, con el collar basal de la mayoría de ellas más estrecho que el ápice setal. En especímenes maduros, los espiráculos generalmente están rodeados por una placa en forma de media luna fuertemente esclerotizada.
Distribución y hospederos
Según el EFSA Panel on Plant Health (2022), P. psidii fue descrita originalmente en Hawái sobre Psidium sp. y, actualmente, se encuentra establecida en numerosos países de regiones tropicales y subtropicales. En la Unión Europea, se ha reportado en España continental y en las Islas Canarias. El informe destaca su alta polifagia, con registros en 230 especies de plantas pertenecientes a más de 70 familias botánicas (EFSA, 2022). Presenta preferencia por cultivos como aguacate (Persea americana), cítricos (Citrus spp.), café (Coffea sp.), guayaba (Psidium guajava), lichi (Litchi chinensis), mango (Mangifera indica), morera (Morus sp.) y granada (Punica granatum). También se ha registrado en solanáceas como tomate (Solanum lycopersicum) y pimiento (Capsicum annuum), además de ornamentales como Melia azedarach.
Por su parte, la base de datos ScaleNet (2014) complementa esta información listando hospe-deros en al menos 60 familias vegetales, incluyendo géneros como Anthurium, Gardenia y los ya mencionados anteriormente. Tanaka & Kondo (2015) reportaron que una especie de Pulvinaria causa daños considerables en el arbolado urbano de Bogotá. Los brotes de este insecto han sido documentados durante largo tiempo en la capital colombiana, donde se le considera, sin duda, una plaga urbana de importancia
Dysmicoccus brevipes (Cockerell)
Material examinado. Perú: Tumbes, Zarumilla, El Bendito, 28. VI. 2025, recolector. F. Cano, Laguncularia racemosa, 10 (♀) adultas. Basado en las llaves de Williams & Granara de Willink (1992), se determinó que los ejemplares pertenecen a la familia Pseudococcidae y a la especie Dysmicoccus brevipes (Cockerell). En la Figura 7a-d se presentan los detalles de las observaciones microscópicas realizadas.
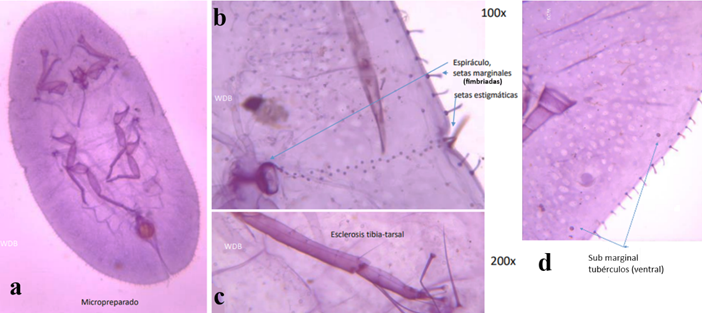
Figura 6. Pulvinaria psidii. (a) hembra a 40x, (b) Espiráculo, setas marginales(fimbriadas), setas estigmáticas. 100x, (c) esclerosis tibial tarsal, 200x (d) parte ventral mostrando tubérculos submarginales.
Diagnosis de la especie
Según Williams & Granara de Willink (1992), la hembra adulta presenta un cuerpo ovalado y moderadamente convexo; carece de anillo caudal y filamentos caudales largos, lo que permite dife-renciarla de las especies del género Planococcus. Posee 17 pares de cerarios: el anal con dos setas cónicas y setas auxiliares, mientras que los restantes presentan de dos a cuatro setas cónicas. Las antenas constan de ocho segmentos y posee dos pares de ostíolos. Los poros triloculares se encuentran dispersos; los discoidales son granu-lados, con un diámetro mayor al de los triloculares, y se distribuyen de forma dispersa o en grupos en la zona media de los últimos segmentos abdominales. Las setas dorsales son normalmente flageladas y fuertes, alcanzando su mayor longitud en la zona media de los segmentos VII y VIII. El anillo anal presenta seis setas y dos vueltas de poros. En la superficie ventral, se observan poros triloculares y discoidales granulados dispersos; estos últimos se localizan próximos a los ojos. Las patas presentan poros translúcidos en el fémur y la tibia posteriores. Los conductos tubulares, de un solo tamaño, se distribuyen en el abdomen (desde el segmento IV hasta el último) y en la zona frontal entre las antenas. Los poros multiloculares se disponen alrededor de la vulva y se extienden hasta el segmento VI. Finalmente, presenta un circulus subcuadrado con la línea intersegmental situada entre los segmentos III y IV.
Distribución y hospederos
D. brevipes es una especie altamente polífaga, conocida principalmente por infestar la piña (Ananas comosus), aunque también se asocia al plátano, caña de azúcar, café y cítricos. Este insecto coloniza diversos órganos de la planta, incluyendo las raíces, donde cumple un rol crítico como vector de virus vegetales. Su distribución es amplia en regiones tropicales y subtropicales de América, Asia y Oceanía (CABI, 2021; Williams & Granara de Willink, 1992; Cox, 1989).
Al respecto, De Araujo et al. (2021) reportan que D. brevipes es una plaga clave en diversos cultivos, capaz de transmitir fitopatógenos, reducir el crecimiento y comprometer la producción. Un caso crítico es el de la palma macaúba (Acrocomia aculeata), donde este pseudocóccido posee una gran capacidad para causar la muerte de ejemplares jóvenes, afectando seriamente la longevidad y productividad de las plantaciones.
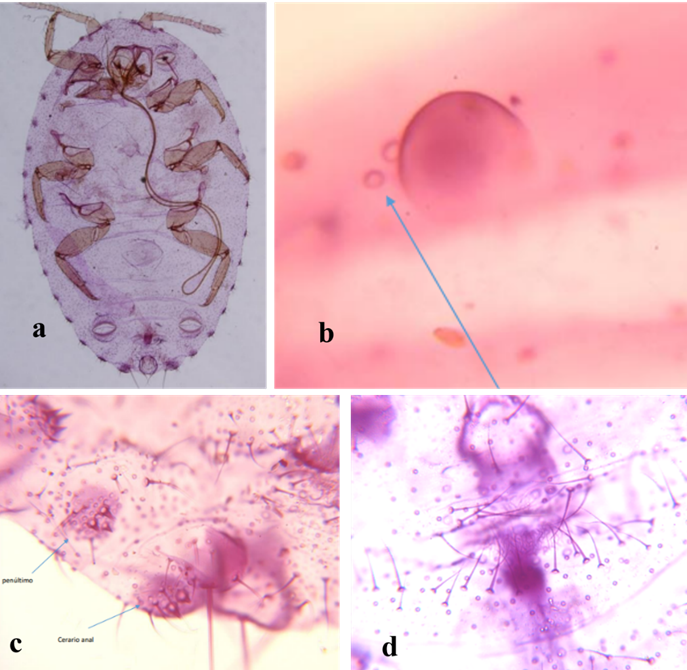
Figura 7. Dysmicoccus brevipes: (a) Hembra. 40x, (b) ojo con poro discoidales adjuntos 200x, (c)tres últimos cerarios. 200x. (d)pelos ubicados en la parte dorsal entre el séptimo y octavo segmento abdominal. 200x.
CONCLUSIONES
Este estudio constituye el primer registro de Parasaissetia nigra, Pulvinaria psidii y Dysmicoccus brevipes infestando Laguncularia racemosa en los manglares de Tumbes, lo que amplía el rango de hospederos conocidos y representa un avance en el conocimiento fitosanitario de este ecosistema costero. Los resultados evidencian un potencial riesgo para la salud del manglar, dado que la infestación por cochinillas puede reducir la fotosíntesis, debilitar los árboles y aumentar su vulnerabilidad frente a factores ambientales y patógenos. En este contexto, se resalta la importancia del monitoreo y la detección temprana como medidas clave para la conservación, y se sugiere que futuras investigaciones evalúen cuantitativamente los efectos fisiológicos y ecológicos de estas plagas, así como posibles estrategias de manejo integrado que mitiguen su impacto en un ecosistema catalogado globalmente como vulnerable.
AGRADECIMIENTOS
A la Agencia Española de Cooperación -Programa de Triangulación para América Latina y el Caribe como parte del proyecto “Apicultura climáticamente inteligente en ecosistemas de manglar. Al IDIAP-Panamá, Universidad Nacional de Tumbes, Consorcio Manglares Noroeste del Perú, Universidad de Santiago Compostela, CREO Ramsar.
REFERENCIAS BIBLIOGRÁFICAS
Abdul-Rassoul, & Al-Mallo, I. (2016). First record of Nigra scale, Parasaissetia nigra (Nietner, 1861) (Hemiptera; Coccidae) as a pest of fig trees in Iraq. Bulletin of the Iraq Natural History Museum, 14(2), 171–178.
Alongi, D. M. (2008). Mangrove forests: Resilience, protection from tsunamis, and responses to global climate change. Estuarine, Coastal and Shelf Science, 76(1), 1–13. https://doi.org/10.1016/j.ecss.2007.08.024
Anon. (1969). Insect pest survey fort the year ending 30th june 1967. Phytophagous insect pests in Papua and New Guinea. Papua and New Guinea Agricultural Journal 21, 49-75
Arnaud, M., Krause, S., Norby, R. J., Dang, T. H., Acil, N., Kettridge, N., Gauci, V., & Ullah, S. (2023). Global mangrove root production, its controls and roles in the blue carbon budget of mangroves. Global Change Biology, 29(12), 3256-3270. https://doi.org/10.1111/gcb.16701
Barbier, E. B. (2012). A spatial model of coastal ecosystem services. Ecological Economics, 78, 70–79. https://doi.org/10.1016/j.ecolecon.2012.03.015
Barrie, J. W. (1956). Coffee in the highlands. Papua and New Guinea Agricultural Journal 11, 1-29
Ben-Dov, Y., & Hodgson, C. (1997). Soft Scale Insects: Their Biology, Natural Enemies and Control. World Crop Pests Vol. 7. Elsevier.
Bragard, C., Baptista, P., Chatzivassiliou, E., Di Serio, F., Gonthier, P., Jaques Miret, J. A., Justesen, A.F., Magnusson, C. S., Milonas, P., Navas-Cortes, J. A., Parnell, S., Potting, R., Reignault, P. L., Stefani, E., Thulke, H. -H., Van der Werf, W., Vicent Civera, A., Yuen, J., Zappala, L., Gregoire, J. -C., Malumphy, C., Akrivou, A., Kertesz, V., Maiorano, A., Papachristos, D., & MacLeod A. (2022). Scientific Opinion on the pest categorisation of Pulvinaria psidii. EFSA Journal, 20(8), 7526. https://doi.org/10.2903/j.efsa.2022.7526
Bunting, P., Rosenqvist, A., Hilarides, L., Lucas, R. M., Thomas, N., Tadono, T., Worthington, T. A., Spalding, M., Murray, N. J., & Rebelo, L. -M. (2022). Global mangrove extent change 1996– 2020: Global mangrove watch version 3.0. Remote Sensing, 14(15), 3657. https://doi.org/10.3390/rs14153657
CABI. (2021). Dysmicoccus brevipes datasheet. In Invasive Species Compendium. CAB International.
Camacho, E. R., & Chong, J. -H. (2015). General Biology and Current Management Approaches of Soft Scale Pests (Hemiptera: Coccidae). Journal of Integrated Pest Management, 6(1), 17.
Causton, C. E., Peckb, S. B., Sinclair, J, Roque-Albelo, L., Hodgson, C. J., & Landry, B. (2006) Alien Insects: Threats and Implications for Conservation of Galápagos Islands, Annals of the Entomological Society of America, 99(1), 121–143. https://doi.org/10.1603/0013-8746(2006)099[0121:AITAIF]2.0.CO;2
Cohic, F. (1955). Rappoort d^une misión aux ètablissements francasis de l^Oceanic. Fascicle III.
Cohic, F. (1956). Parasite animaux des plantes cultivèes en Nouvelles- Calèdonie et dèpendances. Pp 1-91 Institute Francais dÒceanic . O.R.S.T.O.M. , Noumèa.
Cox, J. M. (1989). The mealybug genus Dysmicoccus Ferris (Homoptera: Pseudococcidae). CAB International.
de Araújo, V. C. R., Silva, G. A., Ramos, R. S., Júnior, P. A. S., Pereira, R. R., Motoike, S. Y., & Picanço, M. C. (2021). Distribution and attack of pineapple mealybug to macauba palm Acrocomia aculeata. International Journal of Tropical Insect Science, 41(4), 2765–2773. https://doi.org/10.1007/s42690-021-00456-0
Dioses Puelles, J. E. (2020). Determinación y evaluación de la cobertura vegetal a través de parcelas de monitoreo permanente en el Santuario Nacional los Manglares de Tumbes—Perú [Tesis de Ingeniero Forestal y del Medio Ambiente, Universidad Nacional de Tumbes].
EFSA Panel on Plant Health. (2022). Pest categorisation of Pulvinaria psidii (Hemiptera: Coccidae). EFSA Journal, 20(8), 7526. https://doi.org/10.2903/j.efsa.2022.7526
EPPO. (2021). Parasaissetia nigra datasheet
García Morales, M., Denno, B. D., Miller, D. R., Miller, G. L., Ben-Dov, Y., & Hardy, N. B. (2016). ScaleNet: a literature-based model of scale insect biology and systematics. Database: The Journal of Biological Databases and Curation, 2016, bav118. https://doi.org/10.1093/database/bav118
Granara de Willink, María Cristina. (1990). Las cochinillas blandas de la República Argentina. Homoptera: Coccoidea: Coccidae :Vol. 3. Nº1. On Entomology International.
Hamon, A. B. (1984). The soft scale insects of Florida (Homoptera: Coccoidea: Coccidae). Gainesville, Fla. (P.O. Box 1269, Gainesville 32602): Florida Dept. of Agriculture and Consumer Services, Division of Plant Industry.
Hodgson, C. J. (1994). The Scale Insect Family Coccidae: An Identification Manual to Genera. CAB International.
Huamán Tunante, D. E. (2022). Efecto de tres insecticidas orgánicos en la densidad poblacional de Pulvinaria psidii Maskell, en Shinus molle L._Cajamarca. [Tesis de Ingeniero Forestal. Universidad Nacional de Cajamarca].
Júnior, L., Santos, I., & Santos, A. (2019). First Report of Parasaissetia nigra in Khaya ivorensis Seedlings in Brazil. Floresta e Ambiente. https://doi.org/10.1590/2179-8087.015618.
Lever, R.J.A.W. (1946). Insect pest in Fiji. Bulletin Department of Agriculture, Fiji 16, 41-44.
Lin,Y-P.,Cook,D.H.,Gullan,.P.J, & Cook, L.G. (2015)Doeshost-plantdiversityexplain speciesrichnessin insects? Atest using Coccidae (Hemiptera). Ecol. Entomol., 40, 299–306.
Malumphy, C. P. (2002) Diagnostic protocols for regulated pests Parasaissetia nigra. OEPP/EPPO Bulletin 32: 293-298
Mazzeo, G., Nucifora, S., & Longo, S. (2020). Definitive confirmation of establishment of Parasaissetia nigra (Nietner) (Hemiptera, Coccidae) in Sicily (Italy), with notes on its association with a new host, Syzygium myrtifolium Walp. Eppo Bulletin, 50, 295-298. https://doi.org/10.1111/epp.12659
Martínez Cabrera, R. (2022). Presión antrópica y su relación con la susceptibilidad del Santuario Nacional los Manglares de Tumbes, 2000 – 2020. Revista Cátedra Villarreal Posgrado, 1(2), Article 2.
O'Connor (1949). Some insect pests of Tonga. Agricultural Journal, Department of Agriculture, Fiji 20, 47-57.
Pérez, N., Mier Durante, M.P, & Umaran, A. (2015). Orden Hemiptera: Subordenes Cicadomorpha, Fulguromorpha & Sternorhyncha. Revista IDE@-SEA54(1-18).
Reboul, J.L. (1976). Principaux parasites et maladies des plantes cultivèes en Polynèsi Francasise. Service de l`Èconomic Rurales, Research Agronomique. Nº 129/ER/RA 58 pp. Pirae.
Reis, Y. S., Silva, A. G., Santos, J. M., & Peronti, A. L. B. G. (2020). Scale insects (Hemiptera: Coccomorpha) on Brazilian mangroves. Neotropical Entomology, 49(5), 652–660. https://doi.org/10.1007/s13744-020-00791-w
Rull, V. (2023). Rise and fall of Caribbean mangroves. Science of The Total Environment, 885, 163851. https://doi.org/10.1016/j.scitotenv.2023.163851
Santos, Sonia A. P., Santos, C., Silva, S., Pinto, G., Torres, L. M., & Nogueira, A. J. A. (2013). The effect of sooty mold on fluorescence and gas exchange properties of olive tree. Turkish Journal of Biology: 37, 5, Article 14. https://doi.org/10.3906/ biy-1301-81
Sartiami, D., Watson, G. W., Mohamad, M, N., & Idris, A. (2016). New Indonesian Country Records and Species Information for Mealybugs (Hemiptera: Pseudococcidae) in Wirjati’s Historic Collection. Redia, XCIX, 155–161. http://dx.doi.org/10.19263/REDIA-99.16.20
ScaleNet. (2014). Pulvinaria psidii host and distribution records. ITP Node.
Seminario-Córdova, R. A., Barreto, I. B., & Tuesta, Z. E. E. (2022). Coastal wetlands of the north of Peru: Preservation progress. Acta Scientiarum. Biological Sciences, 44, e62571. https://doi.org/10.4025/actascibiolsci.v44i1.62571
Shree.M.P., & Manjunatha,S.(2000).Incidence of black scale insects (Saissetia nigra, N.) infesting mulberry in Kanakapurataluk (Bangalore Rural District, Karnataka State). Entomon. 25, 91–96.
Spalding, M. (2010). World Atlas of Mangroves. Routledge. https://doi.org/10.4324/9781849776608
Sudiarta, I., Saraswati, K., Ngurah, G., Wirya, A., Shinta, P., Wijayanti, F., Getas, M., Wangi, P., Ilmi, M., & Widyasari, A. (2025). New Report of Dysmicoccus brevipes Cockerell (1893) (Hemiptera: Pseudococcidae) on Heliconia sp., Lagenaria sp., and Zea mays L. Root in Bali Indonesia. Journal of Tropical Biodiversity and Biotechnology, 10(1), jtbb13563. https://doi.org/10.22146/jtbb.13563
Takahashi, K., & Grimaldo, A. M. (2015). Impacto de la variabilidad y cambio climático en el ecosistema de Manglares de Tumbes, Perú. Instituto Geofísico del Perú.
Tanaka, H., & Kondo, T. (2015). Description of a new soft scale insect of the genus Pulvinaria Targioni Tozzetti (Hemiptera, Coccoidea, Coccidae) from Bogota, Colombia. ZooKeys, 484, 111-120. https://doi.org/10.3897/zookeys.484.9280
Unión Internacional para la Conservación de la Naturaleza (UICN). (2024, 21 de mayo). Más de la mitad de todos los ecosistemas de manglares en riesgo de colapso para 2050: primera evaluación global de la Lista Roja de Ecosistemas. https://www.iucn.org/press-release/202405/more-half-all-mangrove-ecosystems-risk-collapse-2050-first-global-assessment.
Williams, D. J., & Watson, G. W. (1988). The scale insects of the tropical South Pacific region. Part 2. The mealybugs (Pseudococcidae). CAB International.
Williams, D. J., & Granara de Willink, M. C. (1992). Mealybugs of Central and South America. CAB International.
Zhila, H., Mahmood, H., & Rozainah, M. Z. (2014). Biodiversity and biomass of a natural and degraded mangrove forest of Peninsular Malaysia. Environmental Earth Sciences, 71(11), 4629-4635. https://doi.org/10.1007/s12665-013-2853-6