 |
INTRODUCCIÓN
Osteología mandibular de Graodus boucardi (Pisces: Cyprinodontiformes) con la técnica de diafanización
Mandibular osteology Graodus boucardi (Pisces: Cyprinodontiformes) with the diaphanization technique
Javier Teodoro Reza-Rodríguez1; Mara Erika Paredes-Lira2*
1 Facultad de Ciencias Biológicas, Universidad Autónoma del Estado de Morelos, Av. Universidad 1001, Colonia Chamilpa, C.P. 62209. Cuernavaca, Morelos, México.
2 Centro de Investigaciones Biológicas, Colonia Chamilpa, Cuernavaca, Morelos C.P. 62209, Universidad Autónoma del Estado de Morelos, México.
* Autor corresponsal: mara.paredes@uaem.mx (M. E. Paredes-Lira).
ORCID de los autores:
J. T. Reza-Rodríguez: https://orcid.org/0009-0005-1093-1137 M. E. Paredes-Lira: https://orcid.org/0009-0002-0154-2760
RESUMEN
Se estudió la morfología mandibular y osteológica de Graodus boucardi, “carpita morelense”, especie endémica de Morelos, México. Este pez está en riesgo según la NOM-059 (SEMARNAT, 2010) debido a la contaminación del agua, manejo deficiente del recurso hídrico y la introducción de especies invasoras. Habita cuerpos de agua dulce, fría y cristalina, cumpliendo un papel ecológico importante. La investigación se enfocó en las estructuras óseas del aparato masticador, empleando la técnica de diafanización para observar su organización interna. Se identificaron 29 piezas agrupadas en cuatro conjuntos: arco mandibular, serie hipopalatina, opercular y aparato branquial. Externamente, destaca una boca terminal amplia y estructuras sensoriales redondeadas. Internamente, el premaxilar y el maxilar carecen de articulaciones entre sí y con el dentario, favoreciendo una gran protracción bucal, útil para capturar presas en corrientes rápidas. El aparato branquial presenta branquiespinas y dientes faríngeos que permiten sujetar y procesar presas pequeñas, coincidiendo con su dieta entomófaga. Su morfología mandibular y sensorial está altamente adaptada a su entorno, subrayando la necesidad urgente de su conservación. Estos hallazgos pueden ser de gran utilidad para diseñar estrategias de conservación, ya que permiten identificar rasgos morfológicos clave que facilita a la especie adaptarse y sobrevivir en ambientes lóticos.
Palabras clave: diafanización; morfoanatomía; mandíbula; G. boucardi.
ABSTRACT
The mandibular and osteological morphology of Graodus boucardi, the "carpita morelense", a species endemic to Morelos, Mexico, was studied. This fish is at risk according to NOM-059 (SEMARNAT, 2010) due to water pollution, poor water resource management, and the introduction of invasive species. It inhabits cold, clear freshwater bodies, playing an important ecological role. The research focused on the bony structures of the masticatory apparatus, using the diaphanization technique to observe their internal organization. Twenty-nine pieces were identified, grouped into four sets: mandibular arch, hypopalatine series, opercular, and branchial apparatus. Externally, a wide terminal mouth and rounded sensory structures stand out. Internally, the premaxilla and maxilla lack articulations with each other and with the dentary, favoring a large oral protraction, useful for capturing prey in fast-flowing currents. The gill apparatus features gill rakers and pharyngeal teeth that allow it to grasp and process small prey, consistent with its entomophagous diet. Its mandibular and sensory morphology is highly adapted to its environment, underscoring the urgent need for its conservation. These findings can be very useful for designing conservation strategies, as they allow us to identify key morphological traits that facilitate the species adaptation and survival in lotic environments.
Keywords: diaphanization; morphoanatomy; mandible; G. boucardi.
Recibido: 13-06-2025.
Aceptado: 09-08-2025.
El estudio de la morfología funcional permite comprender cómo la selección natural ha favorecido diseños anatómicos que optimizan el desempeño funcional de los organismos en su entorno (Alexander, 1988; Koehl, 1996). En peces, la forma de las estructuras craneales, mandibulares y branquiales está íntimamente relacionada con sus estrategias tróficas, lo que proporciona información clave sobre su ecología alimentaria (Wainwright, 1994; Labropoulou et al., 1997). Estas variaciones morfológicas están determinadas por procesos biológicos como la adaptación local, el desarrollo ontogenético y la diversificación evolutiva (Zelditch et al., 2004).
El análisis de la ecología alimentaria en especies depredadoras requiere considerar no solo la disponibilidad de presas, sino también la eficiencia del depredador, determinada por su morfología osteológica. De este modo, la forma y disposición de estructuras como la mandíbula o el aparato branquial ofrecen evidencia de adaptaciones tróficas claves (Wainwright, 1994).
En este contexto, Graodus boucardi, conocida como “carpita morelense”, es una especie de agua dulce perteneciente a la familia Leuciscidae, cuya distribución actual se restringe exclusivamente al estado de Morelos, en los municipios de Jiutepec y Temixco, principalmente en la microcuenca de El Texcal y en arroyos localizados al poniente de Cuernavaca. Aunque previamente se pensaba que era endémica de la cuenca del río Balsas, estudios recientes han demostrado que su distribución es mucho más limitada, lo que incrementa su vulnerabilidad (Schönhuth & Doadrio, 2003; Rivas, 2008). Esta especie habita en cuerpos de agua someros, fríos y cristalinos, con vegetación sumergida y sustrato rocoso, condiciones esenciales para su alimentación y reproducción (Contreras-MacBeath, 1990); sin embargo, diversas amenazas ambientales como la urbanización acelerada, el vertido de aguas residuales, la sobreexplotación de acuíferos y la introducción de especies exóticas, han provocado una reducción drástica de su hábitat y número poblacional (Contreras-MacBeath & Rivas, 2007; Preciado, 2014). Esta situación ha llevado a que la NOM-059-SEMARNAT-2010 clasifique a G. boucardi como una especie en riesgo.
Aunque existen estudios clásicos sobre la morfo-logía mandibular de peces (Wainwright, 1994; Koehl, 1996; Harrington, 1955), investigaciones más recientes han resaltado la importancia de abordar estos análisis en contextos ecológicos específicos, especialmente en especies endémicas con hábitats restringidos (Calazans et al., 2021; Fricke et al., 2023). Además, análisis de la microestructura ósea mandibular en trucha arcoíris han mostrado variaciones ligadas al ambiente y la disponibilidad de minerales que afectan la funcionalidad mandibular (Godoy et al., 2022), mientras que estudios en pez cebra revelan cómo la densidad mineral ósea cambia con la edad, afectando directamente la biomecánica del aparato masticador (Kague et al., 2022). Investigaciones comparativas en carácidos y cíclidos del sureste mexicano también han demostrado que la forma mandibular varía según la dieta y el hábitat (Martínez-Mozes et al., 2024; Rodríguez-Ruiz & Granado-Lorencio, 1987).
En el caso particular de la familia Leuciscidae, estudios en Notropis nubilus han identificado variaciones morfológicas mandibulares entre poblaciones relacionadas con presiones ambientales locales (Bennett et al., 2021), y en Leuciscus leuciscus se ha documentado un crecimiento alométrico en la mandíbula vinculado al desarrollo ontogenético y a la especialización trófica (Kupren et al., 2016).
En este contexto, persiste un vacío de conocimiento respecto a la descripción osteológica detallada de Graodus boucardi, una especie endémica de distribución restringida en el estado de Morelos, donde la aplicación de técnicas como la diafanización representa una herramienta valiosa para caracterizar con precisión la organización y funcionalidad de su aparato mandibular y esta contribución adquiere relevancia no solo desde una perspectiva morfofuncional y evolutiva, sino también como base científica para el diseño de estrategias de conservación, considerando que la especie enfrenta múltiples amenazas en su hábitat natural; por tal motivo, el presente estudio ofrece una aproximación integral que articula la des-cripción anatómica con implicaciones ecológicas, consolidando un aporte original en el conocimiento de peces dulceacuícolas mexicanos en riesgo.
METODOLOGÍA
Material biológico
Para llevar a cabo el análisis morfológico de las estructuras óseas involucradas en la obtención de alimento, se utilizaron seis ejemplares de Graodus boucardi provenientes de un poblador de la localidad de Huahuachiles, Jiutepec, Morelos a unos metros de El Texcal, entre las coordenadas 18°53'24" latitud norte y 99°09'32" longitud oeste. Los especímenes fueron fijados en formaldehído al 10% por 7 días y posteriormente conservados en alcohol al 70% durante 20 días para ser sometidos a un proceso de diafanización (Figura 1) propuesta por Hollister (1934) y Davis y Gore (1936), que permiten visualizar detalladamente estructuras osteológicas sin deteriorar la integridad anatómica. Está técnica, tiene la finalidad de transparentar los tejidos blandos de un organismo, lo que permite observar los elementos óseos (Romero-Oliva y González-Rodríguez, 2019), se realiza a través de la digestión alcalina con hidróxidos y colorante rojo de alizarina para la tinción, el cual se fija a los fosfatos de calcio que se encuentran en el tejido óseo (Rejala et al., 2019), dicha técnica permite mejorar la enseñanza de los temas asociados a la anatomía animal (Lázaro-Juárez et al., 2023).
Identificación y acomodo de las piezas óseas
Tomando como base a las ilustraciones realizadas por Kobelkowsky (1998) en su estudio sobre Lutjanus griseus (Figura 2), los ejemplares fueron inicialmente observados y descritos externamente desde la región anterior de la cabeza hasta el opérculo branquial, con el propósito de determinar la posición de la boca, la localización de órganos sensoriales y la disposición de las estructuras relacionadas con la captura de alimento. Posteriormente, se realizó la desar-ticulación cuidadosa del complejo mandibular y branquial, registrando el número, forma y disposición de cada pieza, así como las relaciones articulares que estas mantienen dentro del cráneo; posteriormente la información recolectada fue organizada en una tabla resumen (Tabla 2), la cual incluye funciones y observaciones relevantes que sustentan las interpretaciones posteriores sobre adaptaciones funcionales.
Las piezas óseas fueron analizadas individual-mente bajo un microscopio estereoscópico marca Nikon, equipado con una cámara profesional Canon Rebel T5 para la captura de imágenes de alta resolución. Finalmente, dichas imágenes fueron procesadas digitalmente con el software Adobe Photoshop CS6, con el objetivo de optimizar la calidad fotográfica y preservar con precisión los detalles morfológicos relevantes de cada estructura.
Desarticulación y análisis funcional
Para el análisis osteológico detallado, se realizó La desarticulación del complejo mandibular y branquial bajo microscopio estereoscópica Nikon, utilizando pinzas de disección. Se identificaron cuidadosamente las articulaciones presentes y ausentes, así como la movilidad relativa entre piezas. Las funciones propuestas en la (Tabla 2) se basaron en la disposición observada, analogías biomecánicas con especies previamente descritas de Notropis bifrenatus y Astyanax aeneus, y las
referencias anatómicas estándar de (Kobelkowsky, 1998; Harrington, 1955).

Figura 1. G. boucardi bajo la técnica de transparentación y tinción.
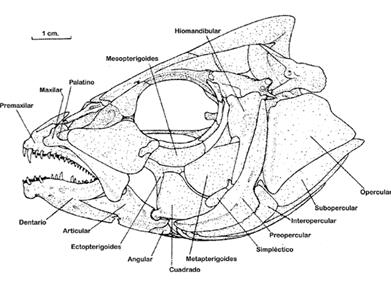
Figura 2. Cráneo de Lutjanus griseus (Tomado de Kobelkowzky, 1998).
RESULTADOS Y DISCUSIÓN
Análisis externo
Graodus boucardi presenta una boca terminal amplia, que alcanza aproximadamente tres cuartas partes de la altura de la cabeza, flanqueada por labios gruesos y una notable cantidad de estructuras redondeadas distribuidas desde los labios hasta la parte dorsal y ventral de la cabeza (Figura 3).
Estas estructuras, presumiblemente sensoriales, disminuyen en número a medida que se alejan de la región cefálica, extendiéndose incluso sobre las aletas pectorales (Tabla 1). Esta disposición sugiere una alta sensibilidad táctil y gustativa, común en especies que habitan en ambientes con baja visibilidad, lo cual ha sido documentado en otros ciprínidos como Cyprinus carpio (Ruiz, 2004).
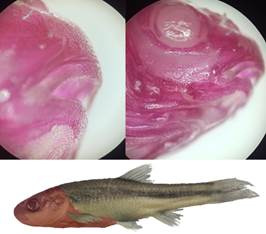
Figura 3. Vista lateral de la cabeza de G. boucardi mostrando la disposición de estructuras sensoriales.
Tabla 1
Distribución y densidad de estructuras sensoriales en diferentes regiones del cuerpo
|
Región anatómica |
Tipo de estructura sensorial |
Forma observada |
Densidad aproximada |
Observaciones |
|
Labios (superior/inferior) |
Papilas o estructuras redondeadas |
Redondeada |
Alta |
Disminuyen hacia la parte posterior de la cabeza |
|
Región cefálica dorsal |
Papilas sensoriales |
Redondeada |
Media |
Posiblemente relacionadas con detección táctil |
|
Región ventral cefálica |
Papilas sensoriales |
Redondeada |
Media |
Asociadas a alimentación |
|
Base de las aletas pectorales |
Estructuras sensoriales |
Redondeada |
Baja |
Extensión lateral limitada |
Descripción osteológica
Se identificaron 29 piezas óseas (Figura 4) divididas en 4 grupos principales.
Arco mandibular: premaxilar, maxilar, dentario, articular, angular y esplenial.
Serie hipopalatina: palatino, mesopterigoides, ectopterigoides, metapterigoides, cuadrado e hiomandibular.
Serie opercular: opercular, preopercular, inter-opercular y subopercular.
Aparato branquial: basibranquiales, hipobran-quiales, ceratobranquiales, epibranquiales, farin-gobranquiales y arcos faríngeos con dientes faríngeos.

Figura 4. Esquema del lado derecho de la cabeza de G. boucardi desde una vista interna que muestra las piezas óseas descritas del arco mandibular, serie hipopalatina y su acomodo.
Esta organización permite visualizar la comple-jidad funcional del aparato masticador y respi-ratorio, y constituye la base para las comparaciones morfofuncionales que se describen más adelante. En la (Tabla 2), se sintetizan las piezas óseas identificadas, su clasificación funcional y observaciones morfológicas claves, donde el cuadrado y el articular forman una articulación móvil que podría facilitar un ligero movimiento mandibular, permitiendo la captura de presas en corrientes rápidas. El preopercular, con su forma curvada y superficie iregular y que sugiere un punto de anclaje muscular importante para la apertura bucal.
Por otro lado, el palatino, el mesopterigoides, el ectopterigoides y el metapterigoides están dis-puestos de forma que canalizan el movimiento de protracción hacia la región anterior, favoreciendo la captura de presas móviles.
La información contenida en esta tabla permite establecer conexiones claras entre la morfología observada y las adaptaciones funcionales tróficas de G. boucardi, sirviendo como base para com-paraciones posteriores con otras especies afines.
Protracción bucal y adaptaciones tróficas
Se observó que el premaxilar y el maxilar no presentan articulación entre sí ni con el dentario, lo que permite una protracción bucal significativa (Figura 5). Esta característica, también reportada por Harrington (1955) en N. bifrenatus (Tabla 2), otorga a G. boucardi una ventaja adaptativa al facilitar la captura de presas móviles en corrientes rápidas. En contraste, especies como Astyanax aeneus presentan mandíbulas firmemente articuladas, lo que restringe la movilidad bucal y sugiere un enfoque trófico más especializado (Mejía-Mojica y Díaz Pardo, 1991). La amplitud mandibular en G. boucardi podría relacionarse con su dieta entomófaga generalista y su hábitat lótico.

Figura 5. Vista lateral de la cabeza G. boucardi mostrando la protracción bucal.
Aparato branquial y procesamiento de presas
Las branquiespinas en forma de triángulo puntiagudo, ubicadas sobre ceratobranquiales y epibranquiales, forman una especie de “jaula” que dirige las presas hacia los dientes faríngeos, los cuales están dispuestos en hileras de cuatro por lado (Figura 6). Esta configuración facilita la fragmentación de insectos, optimizando el paso del alimento hacia el esófago. Esta especialización funcional coincide con lo descrito por Adriaens (2003) para Siluriformes y por Ferry-Graham et al. (2001) en peces mariposa, donde la combinación de morfología y conducta alimentaria determina el grado de especialización trófica.
Tabla 2
Inventario y descripción morfológica de las piezas óseas identificadas
|
Conjunto óseo |
Piezas identificadas |
Función principal |
Observaciones relevantes |
|
Arco mandibular |
Premaxilar, maxilar, dentario, articular, angular, esplenial |
Captura de alimento, movilidad bucal |
Alta protracción bucal; sin articulación fija entre maxilar y dentario |
|
Serie hipopalatina |
Palatino, mesopterigoides, ectopterigoides, metapterigoides, cuadrado, hiomandibular |
Transmisión mecánica y soporte de mandíbula |
Similar a lo descrito en N. bifrenatus |
|
Serie opercular |
Opercular, preopercular, interoperacular, subopercular |
Protección branquial, ventilación |
No se observó supraopercular |
|
Aparato branquial |
Branquiespinas, basibranquiales, hipobranquiales, ceratobranquiales, epibranquiales, faringobranquiales, dientes faríngeos |
Filtración y procesamiento de alimento |
Branquiespinas en forma de triángulo; dientes faríngeos en 4 hileras |
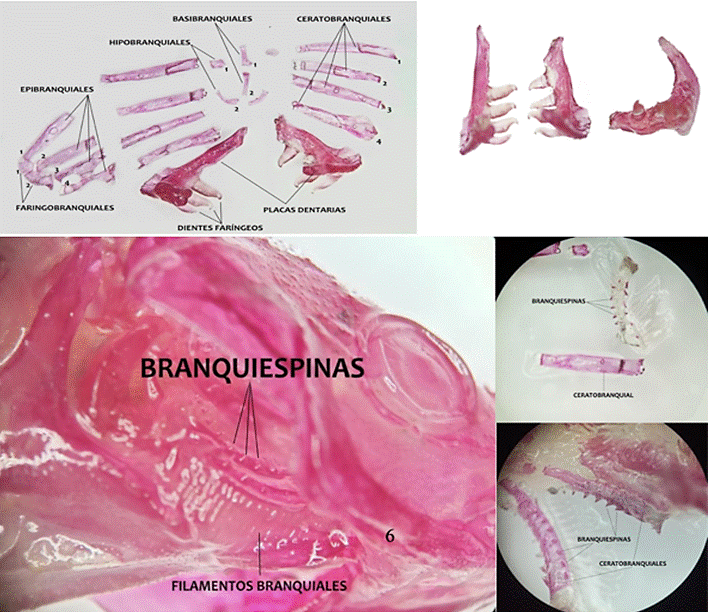
Figura 6. Detalle del aparato branquial y disposición de las branquiespinas y dientes faríngeos.
Comparación con especies relacionadas
En comparación con N. bifrenatus (Harrington, 1955), G. boucardi presenta una disposición similar en la serie hipopalatina, pero difiere notablemente en la ausencia del suprapreopercular, lo que sugiere un diseño morfológico más simple y posiblemente más eficiente en términos de movilidad mandibular. En N. bifrenatus, el maxilar se articula parcialmente con el premaxilar, mientras que en G. boucardi estas piezas permanecen independientes, facilitando una protracción bucal más amplia.
Asimismo, al comparar con Astyanax aeneus, especie adaptada a ambientes menos turbulentos, se observa que esta última posee una articulación mandibular firme que limita la movilidad lateral, reflejando una estrategia trófica más especializada y menos dinámica (Mejía-Mojica y Díaz Pardo, 1991). Por el contrario, la flexibilidad estructural de G. boucardi parece adaptativa para ambientes lóticos con escaces de luz.
Investigaciones recientes en Notropis nubilus evidencian que las presiones ambientales locales pueden inducir variaciones morfológicas en la mandíbula (Bennett et al., 2021), fenómeno que también podría explicar ciertas adaptaciones observadas en G. boucardi. Por otro lado, estudios sobre el desarrollo temprano de Leuciscus leuciscus han demostrado patrones de crecimiento alométrico en la región cefálica, incluyendo estructuras mandibulares, que podrían estar vinculados con adaptaciones funcionales en etapas tempranas de vida y la transición hacia hábitats de corriente rápida (Kupren et al., 2016). Estos hallazgos sugieren que, al igual que en L. leuciscus, el patrón de crecimiento craneal en G. boucardi podría guardar relación con exigencias ambientales específicas, aunque se requiere investigación ontogenética adicional para confirmarlo.
Se recomienda la inclusión futura de esquemas comparativos o imágenes osteológicas de las especies relacionadas, lo que permitiría una mejor visualización de las diferencias estructurales descritas y reforzaría la interpretación funcional del aparato masticador en relación con el hábitat.
CONCLUSIONES
El estudio osteológico de Graodus boucardi permi-tió identificar 29 piezas óseas distribuidas en cua-tro conjuntos: arco mandibular, serie hipopalatina, serie opercular y aparato branquial. Estas estructuras muestran un acomodo que refleja una adaptación funcional al entorno lótico en el que habita la especie. El objetivo de describir e interpretar los rasgos morfológicos externos y osteológicos del aparato masticador se cumplió mediante la caracterización detallada de cada estructura implicada en la captura y procesamiento del alimento.
Uno de los hallazgos más relevantes fue la ausencia de articulación entre el premaxilar y el maxilar, lo que proporciona una notable protactibilidad bucal. Esta movilidad amplia le permite capturar presas móviles con mayor eficacia en corrientes rápidas. Asimismo, se observó que la mayoría de las piezas óseas no presentan articulaciones rígidas, sino que están unidas por tejido, contribuyendo a una estructura ligera y adaptable. Las pocas articula-ciones presentes (articular-cuadrado, palatino-mesopterigoides, hiomandibular-opercular y entre basibranquiales) cumplen funciones mecánicas clave.
El aparato branquial, con branquioespinas y dien-tes faríngeos, forma una estructura que orienta a las presas hacia el esófago, fragmentándolas parcialmente. Este mecanismo, junto con una boca amplia y flexible, confirma la especialización entomófaga de la especie. Aunque se observaron estructuras externas posiblemente sensoriales, no se logró definir su naturaleza. Dado el tipo de hábitat de G. boucardi, es fundamental comprender cómo utiliza estas estructuras para detectar alimento en condiciones de visibilidad reducida y corriente fuerte.
Se sugiere realizar estudios de comportamiento alimentario en condiciones naturales, y posibles análisis histológicos y morfofuncionales de los sistemas sensoriales. Esto permitirá establecer una relación más completa entre estructura, función y ecología trófica, fortaleciendo las estrategias de conservación de esta especie en riesgo.
REFERENCIAS BIBLIOGRÁFICAS
Adriaens, D. (2003). Evolution and development of the actinopterygian feeding apparatus as a model to study the evolution of function. Evolutionary Developmental Biology of the Vertebrate Skeleton, 337–370.
Alexander, R. M. (1988). The working of animals. Cambridge University Press.
Bennett, W. A., Cross, B. A., & Hall, S. A. (2021). Morphological variation in the jaw structure of Notropis nubilus in response to habitat hydrodynamics. Journal of Fish Biology, 98(3), 567–580. https://doi.org/10.1111/jfb.14678
Calazans, A. M., Martínez, P. A., & Jacobina, U. P. (2021). Lentic and lotic environments affect morphological diversity in characiformes fishes in the Neotropical São Francisco River Basin, Brazil. Environmental Biology of Fishes, 104(8), 977–987. https://doi.org/10.1007/s10641-021-01131-6
Contreras-MacBeath, T., & Rivas, C. A. (2007). Distribución y conservación de peces en el estado de Morelos. Revista Mexicana de Biodiversidad, 78(1), 41–49.
Contreras-MacBeath, T. (1990). Caracterización ecológica del hábitat de Notropis boucardi en Morelos, México. Instituto de Biología, UNAM.
Davis, C. C., & Gore, G. O. (1936). A method for clearing and staining fish for the study of bone formation. Journal of Morphology, 59(1), 25–29.
Ferry-Graham, L. A., Wainwright, P. C., & Bellwood, D. R. (2001). Prey capture in long-jawed butterflyfishes (Forcipiger): Role of kinematics and suction forces in feeding performance. Marine Biology, 139(4), 935–944. https://doi.org/10.1007/s002270100634
Fricke, R., Eschmeyer, W. N., & Van der Laan, R. (Eds.). (2023). Eschmeyer's Catalog of Fishes: Genera, Species, References. California Academy of Sciences.
Godoy, K., Sandoval, C., Manterola-Barroso, C., Vásquez, C., Sepúlveda, N., Rojas, M., & Salazar, L. A. (2022). Study of the mandibular bone microstructure and blood minerals bioavailability in rainbow trout (Oncorhynchus mykiss) from freshwater. Animals, 12(12), 1476. https://doi.org/10.3390/ani12121476
Harrington, R. W. (1955). The osteocranium of Notropis bifrenatus (Cope). Journal of Morphology, 96(2), 279–311.
Hollister, G. (1934). Clearing and dyeing fish for bone study. Zoologica, 12(1), 89–101.
Kague, E., et al. (2022). Micro-CT analysis reveals the changes in bone mineral density in zebrafish craniofacial skeleton with age. Journal of Anatomy. https://doi.org/10.1111/joa.13703
Koehl, M. A. R. (1996). When does morphology matter? Annual Review of Ecology and Systematics, 27, 501–542. https://doi.org/10.1146/annurev.ecolsys.27.1.501
Kobelkowsky, A. (1998). Anatomía comparada del aparato digestivo de los peces. II. Osteología del pargo Lutjanus griseus (Perciformes: Lutjanidae). Revista Biología Tropical, 46(3), 565–572.
Kupren, K., Rams, I., Żarski, D., & Kucharczyk, D. (2016). Early development and allometric growth patterns of rheophilic cyprinid common dace Leuciscus leuciscus (Cyprinidae: Leuciscinae). Environmental Biology of Fishes, 99(4), 383–391. https://doi.org/10.1007/s10228-016-0508-9
Labropoulou, M., Machias, A., Tsimenides, N., & Eleftheriou, A. (1997). Feeding habits and ontogenetic diet shift of the picarel (Spicara smaris, Linnaeus, 1758). Fisheries Bulletin, 95(2), 353–367.
Lázaro-Juárez, J. E., García-Grajales, J., & Buenrostro-Silva, A. (2023). Técnicas de transparentación en diferentes especies de vertebrados. Revista Mexicana de Agroecosistemas, X(Supl. 1), 49.
Martínez-Mozes, A., García-Ruiz, R., & Domínguez-Cisneros, S. E. (2024). Morfología funcional comparada de las mandíbulas oral y faríngea en cíclidos del sureste mexicano. Revista Mexicana de Ictiología, 40(1), 22–35. https://doi.org/10.22201/ib.24487791e.2024.1.003
Mejía-Mojica, H., & Díaz-Pardo, E. (1991). Descripción del cráneo de Astyanax fasciatus (Pisces: Characidae). Anales de la Escuela Nacional de Ciencias Biológicas, México, 34, 191-214.
Preciado, L. (2014). Reintroducción de Notropis boucardi en el manantial de Chapultepec, Cuernavaca, Morelos. Tesis de licenciatura. Universidad Autónoma del Estado de Morelos.
Rejala, R., Álvarez-Ramírez, T., Alvarenga, A., Coronel, A., Alborno, Ágata, Sirai, P., Serafini, Y., Ortiz, K. Romero, A. (2019). La diafanización como alternativa metodológica para el estudio anatómico de un pez. Revista Científica Estudios e Investigaciones, 8, 207-208.
Rivas, C. A. (2008). Propuesta de manejo integral para la microcuenca de El Texcal, Morelos. Universidad Autónoma del Estado de Morelos.
Rodríguez-Ruiz, A., & Granado-Lorencio, C. (1987). Mandibular morphometrics and trophic differentiation in Chirostoma spp. (Pisces: Atherinidae). Hydrobiologia, 153(1), 21–30. https://doi.org/10.1007/BF00006107
Romero-Oliva, O. J. & González-Rodríguez, K. A. (2019). Optimización de la técnica diafanización y tinción de Piovesana (2014), aplicada para el pez Gymnocorymbus ternetzi. Pädi Boletín Científico de Ciencias Básicas e Ingenierías Del ICBI, 7(13), 41-46.
Ruiz, J. A. (2004). Estructuras sensoriales en la cabeza de peces dulceacuícolas mexicanos: revisión e implicaciones ecológicas. Revista Mexicana de Biodiversidad, 75(1), 45–56.
Schönhuth, S., & Doadrio, I. (2003). Phylogenetic relationships of Mexican cyprinid fishes of the subgenus Notropis (Actinopterygii: Cyprinidae) based on mitochondrial cytochrome b sequences. Molecular Phylogenetics and Evolution, 27(1), 93–104.
Wainwright, P. C. (1994). Functional morphology as a tool in ecological research. In P. C. Wainwright & S. M. Reilly (Eds.), Ecological morphology: Integrative organismal biology (pp. 42–59). University of Chicago Press.
Zelditch, M. L., Swiderski, D. L., Sheets, H. D., & Fink, W. L. (2004). Geometric morphometrics for biologists: A primer. Elsevier Academic Press.