 |
INTRODUCCIÓN
Establecimiento in vitro de Coffea arabica var. Limaní en medios de cultivos basales
In vitro establishment of Coffea arabica var. Limaní in basal culture media
Juan Rodríguez-Layza1; Javier J. Gonzales-Arteaga1; Ladislao C. Romero-Rivas1*;
Marilyn C. Enciso Waller2
1 Laboratorio de Biotecnología Vegetal, Facultad de Ciencias Agropecuarias, Universidad Nacional Daniel Alcides Carrión, Filial Oxapampa, Carretera Central km 3,5, Barrio Miraflores, Oxapampa, Perú.
2 Universidad Nacional Daniel Alcides Carrión. Oxapampa, Perú.
* Autor corresponsal: lromero@undac.edu.pe (L. C. Romero-Rivas).
ORCID de los autores
J. Rodríguez Layza: https://orcid.org/0009-0008-8521-8629 J. J. Gonzales Arteaga: http://orcid.org/0000-0001-6196-707X
L. C. Romero Rivas: http://orcid.org/0000-0002-6598-3277 M. C. Enciso Waller: https://orcid.org/0000-0002-4790-9938
RESUMEN
El cultivo in vitro de Coffea arabica “café” a partir de microesquejes, es una técnica que permite propagar genotipos de interés agronómico, pero requiere disponer del medio de cultivo adecuado para iniciar la micropropagación. El objetivo fue establecer café Var. Limaní en dos medios de cultivo basales (Murashige & Skoog, MS y Schenk & Hildebrandt, SH) con diferentes cantidades de reguladores de crecimiento; evaluados en un diseño de bloques completos al azar (DBCA). En MS, fue superior t1 (sin regulador), con menor fenolización, y sin diferencias estadísticas en contaminación por hongos. bacterias; y, sobrevivencia; además, en t5 (BAP, 0,5 mgL-1), se obtuvo mejor respuesta en el establecimiento in vitro; mientras que, en SH, todos los tratamientos fueron iguales en presencia de hongos, bacterias, fenolización y sobrevivencia; pero, en longitud de brote, número de nudos y hojas fueron superiores t2 (ANA, 0,2 mgL-1 + BAP, 2,25 mgL-1) y t5 (BAP, 0,5 mgL-1) entre los 18 y 42 días después de la inoculación, se concluye que es posible el establecimiento in vitro de microesquejes provenientes de campo de esta variedad con los medios basales MS y SH con la adición de 0,5 mgL-1 de BAP.
Palabras clave: micropropagación, medio basal, regulador de crecimiento, microesqueje, establecimiento.
ABSTRACT
The in vitro cultivation of Coffea arabica "coffee" from microcuttings is a technique that allows the propagation of genotypes of agronomic interest but requires an appropriate culture medium to initiate micropropagation. The objective was to establish coffee var. Limaní in two basal culture media (Murashige & Skoog, MS and Schenk & Hildebrandt, SH) with different amounts of growth regulators; evaluated in a randomized complete block design (RCBD). In MS, t1 (without regulator) was superior, with lower phenolization, and no statistical differences in fungal contamination, bacteria; and survival; in addition, at t5 (BAP, 0.5 mgL-1), a better response was obtained in the in vitro establishment; while, in SH, all treatments were equal in presence of fungi, bacteria, phenolization and survival; but, in shoot length, number of nodes and leaves were higher t2 (ANA, 0.2 mgL-1 + BAP, 2.25 mgL-1) and t5 (BAP, 0.5 mgL-1) between 18 and 42 days after inoculation, it is concluded that the in vitro establishment of microcuttings from the field of this variety is possible with the basal media MS and SH with the addition of 0.5 mgL-1 of BAP.
Keywords: micropropagation, basal medium, growth regulator, microcutting, establishment.
Recibido: 18-06-2025.
Aceptado: 11-09-2025.
El café, Coffea arabica, se cultiva en unos 80 países en todo el mundo (Kumar et al., 2006), como bebida, está muy generalizada en todo el mundo, es producido en los países tropicales y en muchos de ellos dependen económicamente de este cultivo (Krishnan, 2011). En el Perú, su producción está basada principalmente en las variedades Típica y Caturra, en 70% y 20%, respectivamente (Canet et al., 2016); asimismo, se ha determinado que sus granos tostados contienen concentraciones significativas de flavonoides, ácidos fenólicos y derivados de la quercetina (Górecki & Hallmann, 2020; Muzykiewicz-Szymańska et al., 2021). La biotecnología ayuda a aumentar los rendimientos; también, es una vía para disminuir el uso de pesticidas y mejorar la economía de los agricultores (Mamata & Anuj, 2021); además, se menciona que en el proceso de esta tecnología no es afectado por el cambio climático y pueden producirse plantas de interés agronómico de una manera sostenible (Kim et al., 2025); asimismo, se puede mantener las características de la planta donadora de explante; entre estas, en el caso de la industria farmaceútica de Cannabis sativa 'Cheungsam' con alto contenido de cannabinoides es esencial para obtener una producción uniforme ante la demanda en países que han legalizado su consumo (Baek et al., 2024); por otro lado, para aquellas especies vegetales limitadas por la escasez de germoplasma (Lilium rosthornii Diels) única, de lirio silvestre en China, con valor medicinal y ornamental, mediante la inducción de callos embriogénicos, luego la proliferación de brotes y enraizamiento en medio Murashige y Skoog (MS) con la adición de reguladores de crecimiento facilitan y respaldan el cultivo de tejidos in vitro (Fu et al., 2024); por lo mencionado, se ha demostrado que la micropropagación del cultivo de café, es una necesidad, permite reducir el tiempo de establecimiento de plantaciones de alto valor productivo y de calidad uniforme (Melese, 2016);como en el genotipo Sarchimor LC-1668 llamado Limaní, considerado como fuente de genes de resistencia a la roya del cafeto, Hemileia vastatrix, que podría ser utilizado en el manejo de esta enfermedad (Rodríguez et al., 2020).
Los reguladores de crecimiento, entre ellos, las auxinas y citoquininas, son muy utilizados porque ejercen efecto a nivel celular, modificando el crecimiento y desarrollo de las plantas, esencialmente en bajas concentraciones, teniendo en cuenta las condiciones específicas de la propagación in vitro (Alcantara et al., 2019); en donde, se observa una respuesta sobre el material biológico utilizado, dependiendo de la sensibilidad del genotipo a los efectos de la auxina y citoquinina contenidos en el medio de cultivo (Gutierrez-Rosati & Gonzales, 2019); en tejidos foliares de C. arabica L. se obtuvo mayor porcentaje y peso de callo en el medio “Arabica Calli Medium” (ACM) con 1,0 mgL-1 2,4 D + 1,0 mgL-1 BAP (Arimarsetiowati et al., 2023); por otro lado, en brotes axilares y explantes hipocotílicos de café arábica “Solok Rajo”, en el 25% de medio MS, con 5,0 y 7,5 mgL-1 de BAP, fue capaz de aumentar el número y longitud de los brotes, concentraciones superiores parecen dar una influencia desfavorable (Suliansyah et al., 2021).
En la medida que existen nuevas técnicas en la biología molecular, se necesita de métodos de cultivo de tejidos mucho más eficientes para los cultivares comerciales que permita avanzar en el establecimiento in vitro (Fazuoli et al., 2000); en el futuro, cada vez es más importante contar con plántulas libre de patógenos para llevar a campo, la micropropagación puede garantizar; además, países en desarrollo se carece de centros semilleros para cultivos perennes, por la baja tasa de renovación (Etienne et al., 2018). Durante el establecimiento para el inicio del cultivo in vitro, es muy importante controlar la contaminación y la oxidación fenólica, aún más cuando se trata de especies leñosas (Hernández & González, 2010); para especies forestales, puede evitarse la fenolización con el agregado de 150 mgL-1 de ácido ascórbico al medio de cultivo (Indacochea et al., 2018), como en el caso del café, especie calificada como recalcitrante, con muchos problemas para su establecimiento in vitro.
El establecimiento, es la etapa crítica dentro de la micropropagación de las especies vegetales; de manera que, en este proceso se tiene que tener presente varios factores como el tipo, tamaño y edad del explante, contaminación, medio de cultivo, reguladores de crecimiento, fuentes y la concentración de los nutrientes (Mroginski & Roca, 1991; Mroginski et al., 2010); la contaminación y fenolización está presente durante la micropropagación de C. arabica, en el medio MS + 2,5 mgL-1 de KIN + 1,0 mgL-1 de 2,4-D con 10% y 100%, respectivamente (Quiñones et al., 2020).
El medio para la micropropagación de especies vegetales ampliamente utilizado es Murashige y Skoog, (1962), conocido como MS, para regenerar plantas; pero, también existen otros medios como el desarrollado por Loyd y McCown en 1980, WPM, para plantas leñosas y de Schenk e Hildebrandt 1972, SH, para generar callos, también se utiliza para producir plantas completas, y además tiene menor concentración de sales (Beyl, 2000); en muchos laboratorios de cultivo de tejidos vegetales, se utilizan uno o dos medios para una especie en particular; aunque, el MS, es el más utilizado debido que, en varias especies tiene una mejor respuesta, incluye las variedades de las mismas (Cardoso et al., 2018). Asimismo, en la micropropagación de Panax vietnamensis Ha et Grushv, en SH + 0,5 mgL-1 de ANA + 1,0 mgL-1 BAP + 4 g de sacarosa, produjo 1,6 g de biomasa y 7,44 cm de longitud de vitroplanta (Dinh et al., 2021).
En la brotación de yemas de Gmelina arborea, en medio SH y MS diluído a la mitad de sus sales, fue de 42,50% y 20%, respectivamente, permitió observar que el medio SH fue más eficiente en la morfogénesis, posiblemente porque permite una mejor regulación nutricional frente a otros medios (Álvarez et al., 2011). Se ha encontrado que el desarrollo de plántulas de Panax ginseng Meyer, germinadas in vitro fue mejor en medio 1/2MS seguido de 1/2SH y con mayor vigor (Jung-Woo et al., 2023). Meristemas de rizoma de una planta ornamental (Alstroemeria sp.) fueron instaladas en medio MS con BAP (1,0 mgL-1), ANA (0,2 mgL-1) y la combinación de ambos, se determinó que el 76% de explantes lograron regenerar plántulas completas con la adición de 0,2 mgL-1 de ANA (Tombion et al., 2020). En diferentes variedades de C. arabica, la micropropagación se ha tenido éxito a través de la embriogénesis somática; sin embargo, la regeneración de plantas depende del genotipo, tamaño y tipo de explante y los componentes del medio nutritivo; al respecto, en la Var. Colombia, explantes foliares en MS se ha logrado obtener 51% de embriones cotiledonares en la combinación de BAP (0,25 mgL-1) + AIA (0,25 mgL-1) (Avila-Victor et al., 2023). A partir de callos, previamente obtenidos de fragmentos de láminas foliares expuestos en MS suplementado con 0,48 y 0,96 de 2-4 D, de 20 variedades de café (Coffea spp.), inoculados en MS suplementado con 50 mgL-1 de L-cisteína, 0,1 mgL-1de Kinetina y 0,5 mgL-1 de IBA (Acido indol butírico), se logró generar embriones somáticos en siete de ellas destacándose la variedad Borbón que regeneró mayor cantidad (Calderón & Montes, 2024).
En muchos procesos de morfogénesis in vitro en diferentes especies, la primera fase de establecimiento es muy sensible por la contaminación y fenolización a consecuencia de exposición de los explantes a las sustancias y concentración de éstas (hipoclorito de sodio y de calcio); en “arándano” Vaccinium floribundum Kunth, fue efectivo el control de la contaminación con el biocida PPMTM (Plant Preservative Mixture™) con respecto al uso de etanol e hipoclorito de sodio, a partir de explantes de tallo (1 cm) en inmersión en MS (Murashige & Skoog) líquido y 5% (v/v) PPMTM por 5h con agitación constante, luego transferidos al medio WPM (Woody Plant Media) con 2 mLL-1 de PPMTM (Moreno-Peña et al., 2025); en el caso muy particular en café, sus tejidos son muy vulnerables a la oxidación biológica por efecto abrasivo de los agentes desinfectantes y los cortes que sufren los órganos en la obtención de explantes (Suescún et al., 2020). Por la necesidad de disponer germoplasma selecto de café, en menor espacio, tiempo, y en cualquier momento del año; de genotipos uniformes y en forma masiva, se recurre a las técnicas del cultivo de tejidos vegetales in vitro, para contar con material vegetal de buena calidad fitosanitaria, agronómica y organoléptica (Cabrera et al., 2022).
En C. liberica, el uso de medio MS + 0,5 mgL-1 de BAP combinado con 0,5 mgL-1 de IAA produjo un buen desarrollo de brotes (Ardiyani et al., 2021). Por otro lado, en C. arabica, híbrido MCH2, en 5,0 mgL-1 de BAP + hemisulfato de adenina, comparado a BAP solo, se determinó una reducción en la proliferación de brotes, con 2,82 brotes por explante, pero aumentó la longitud del entrenudo (Gebremariam, 2017).
En los últimos años, en los países productores de café, hubo un incremento en el consumo interno, basado en las investigaciones de las propiedades beneficiosas, que califican como un producto saludable (Canet et al., 2016); frente a esto, es necesario que las plantas que se llevan a campo estén libre de patógenos para expresar todas las características de la variedad en el producto final; pero, a pesar de existir un gran desarrollo de la micropropagación es difícil tener estas plantas a nivel de laboratorio (Suárez-Padrón, 2020). Considerando que la introducción y establecimiento in vitro, es una etapa muy crítica en la micropropagación de café. La presente investigación tuvo como objetivo el establecimiento in vitro de C. arabica Var. Limaní de explantes obtenidos de campo, utilizando como medios, el MS y el SH.
METODOLOGÍA
Localización
El trabajo fue realizado en las instalaciones de la Universidad Nacional Daniel Alcides Carrión, filial Oxapampa, en el invernadero y laboratorio de Biotecnología vegetal, carretera central, km 3,5, Miraflores, distrito y provincia Oxapampa, Pasco-Perú.
Colecta del material biológico
Establecimiento en medio MS
El material biológico, fueron plantas jóvenes de café, var. Limaní, de diez meses de edad, obtenidas de un vivero, del sector de Alto Gramazú, 10°31'24"S y 75°27'06"W, distrito de Chonta-bamba, provincia de Oxapampa, Pasco.
Se seleccionaron los mejores plantones, Figura 1, que estuvieron en bolsas plásticas con sustrato, fueron trasladados al invernadero, donde se mantuvieron por 21 días bajo tratamiento fitosanitario, con aplicaciones de 500 mgL-1 de sulfato de cobre pentahidratado, cada 7 días; de éstas, se obtuvo con una hoja de bisturí N°10 desinfectada en etanol 96%, esquejes de ramas del tercio superior, constituido por la yema terminal con tres nudos subyacentes, luego se colocaron sobre papel toalla estéril y se trasladaron al laboratorio de biotecnología dentro de una bolsa de polipropileno rotulada.

Figura 1. Elección de plantones de café Var. ‘Limani’.
Establecimiento en medio SH
En campo, 10°32'22"S y 75°26'42"W, de plantas de 4 años de edad, vigorosas y de apariencia saludable, Figura 2, fueron obtenidos los esquejes, de las ramas del tercio superior, conformado por la yema terminal con dos nudos subyacentes, Figura 3, y colocados en papel toalla humedecido con una solución de benomilo al 1,0% e introducidos en bolsas de polipropileno rotuladas y luego trasladadas al laboratorio.

Figura 2. Plantas donadoras de explantes.

Figura 3. Rama donadora de esqueje.
Desinfección
En el laboratorio, los esquejes fueron defoliados con ayuda de un bisturí # 10 y se desechó una pequeña sección basal del tallo, fueron colocados en un vaso de precipitados de 1,0 L. Luego, se procedió a un lavado con detergente al 1%, seguidamente se dejaron reposar en una solución de Benomilo 1,0 gL-1 y Gentamicina 500 gL-1 durante 30 min, seguidamente un triple enjuague con agua destilada estéril, luego en la cámara de flujo laminar, se realizó una inmersión de los esquejes en hipoclorito de sodio al 1,3% adicionando 3 gotas de tween20 por cada 100 mL de solución; posteriormente, los explantes se enjuagaron 5 veces con agua destilada estéril y se dejaron reposar en una solución antioxidante de 300 mgL-1 de ácido ascórbico y 100 mgL-1 de ácido cítrico durante 10 min. Finalmente, los explantes, nudos apicales (microesqueje) de aproximadamente 0,8 a 1,0 cm de longitud, se sembraron cuidadosamente en tubos de ensayo de 15 x 125 mm, conteniendo 7 mL de medio de cultivo. La incubación se realizó a una temperatura ambiente de 20 °C, con 59,32 μmol m-2s de luminosidad, 60% de humedad relativa y fotoperiodo de 16 horas luz.
Medios de cultivo
Se utilizaron 5 tratamientos (medios de cultivo), Tabla 1, cada uno estuvo compuesto de sales MS y SH, ambos con vitaminas y diferentes concen-traciones de BAP y ANA. A todos se adicionaron 30 gL-1 de sacarosa, agar 9 gL-1 y pH ajustado a 5,6. La esterilización se realizó en autoclave a 121°C y 0,1 MPa por 20 min.
Diseño estadístico
Se utilizó el diseño de bloques completamente al azar (Steel & Torrie, 1985), cinco tratamientos y tres repeticiones, la unidad experimental conformada por seis tubos de ensayo con un microesqueje en cada uno.
Las variables fueron: contaminación (el número de explantes con la presencia de micelios y colonias de bacterias); fenolización (número de explantes con más del 50% de tejido que cambió de color verde a marrón oscuro opacado); sobrevivencia; longitud de brote (cm, desde la base del explante hasta el extremo final del ápice, se consideró la longitud inicial para ser restada a la longitud total); número de nudos (N°, los nudos nuevos que se formaron) y número de hojas (N°). Las lecturas fueron realizadas a los 17, 21, 25 y 38 días después de la inoculación (ddi), en el medio MS y para el medio SH a los 18, 29, 36 y 42 ddi.
El procesamiento de los datos fue realizado con el software estadístico R v4.0.4, se aplicó Q de Cochran y la prueba de Dunn (α = 0,05) para presencia de hongos y bacterias; fenolización y sobrevivencia; asimismo, el análisis de variancia y la comparación múltiple de Duncan (α = 0,05), en la longitud de microesqueje, número de nudos y de hojas. Los datos fueron transformados mediante raíz cuadrada de x+1.
Tratamientos (Medios MS y SH + reguladores en mgL-1) para establecimiento de microesquejes de café var. Limaní
|
Tratamientos |
Descripción |
|
Murashige & Skoog (MS) |
|
|
t1 |
Sin reguladores |
|
t2 |
ANA (0,2) + BAP (2,25) |
|
t3 |
ANA (0,2) |
|
t4 |
BAP (0,2) |
|
t5 |
BAP (0,5) |
|
Schenk & Hildebrandt (SH) |
|
|
t1 |
Sin reguladores |
|
t2 |
ANA (0,2) + BAP (2,25) |
|
t3 |
ANA (0,2) |
|
t4 |
BAP (0,2) |
|
t5 |
BAP (0,5) |
RESULTADOS Y DISCUSIÓN
Establecimiento en medio MS
La prueba Q de Cochran (Anexo 1), a los 17, 21 y 25 ddi, determinó que no hubo diferencias significativas en las variables contaminación por hongos y bacterias, fenolización y sobrevivencia; mientras que, a los 38 ddi sólo se encontró diferencias significativas en fenolización; igualmente, la prueba de Dunn, α = 0,05 (Anexo 1, Figura 4), donde t1 fue superior al resto de tratamientos; mientras que, el ANOVA, (Anexo 2), para número de nudos y de hojas encontró diferencias significativas a los 17 y 21 ddi; sin embargo, con la prueba múltiple de Duncan, α = 0,05 (Anexo 2, Figura 5), determinó que t1 y t5 fueron superiores e iguales a t4. Por otro lado, a los 25 ddi, el N° de nudos y hojas, t5 fue superior a t2 y t3 e igual al resto de tratamientos; a los 38 ddi, t5 fue superior a t3 e igual a los demás tratamientos en número de nudos; y, en número de hojas, t5 fue igual a t1 y ambos superiores a t2 e igual a t3 y t4.
Establecimiento en medio SH
La prueba de comparación de Cochran y Dunn, α=0,05 (Anexo 3, Figura 6), determinaron que no hubo diferencias significativas para contaminación por hongos y bacterias, fenolización y sobrevivencia, a los 18, 29, 36 y 42 ddi; mientras que, con el ANOVA, (Anexo 4), determinó diferencias significativas para longitud de brotes a los 36 ddi y altamente significativa a los 42 ddi y significativa para número de hojas a los 29 ddi. La prueba múltiple de Duncan, α = 0,05 (Anexo 4, Figura 7), determinó en longitud de brotes a los 29, 36 y 42 ddi que t5, t4 y t2 fueron superiores a los demás; en número de nudos y hojas, t3 fue inferior a los demás tratamientos a los 29 y 36 ddi; sin embargo, a los 18 y 42 ddi, todos los tratamientos fueron iguales, en las variables evaluadas, excepto para longitud de brotes, a los 42 ddi.
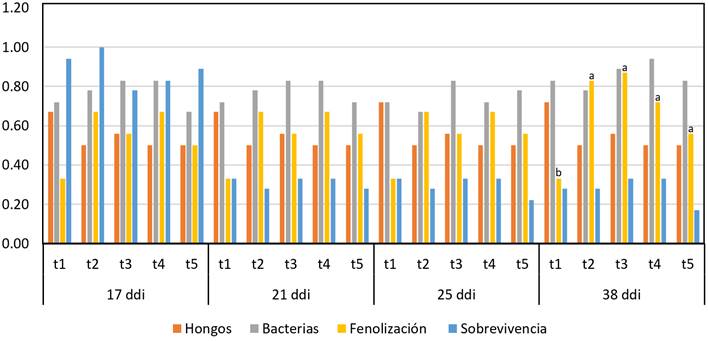
Figura 4. Variables de desinfección en el establecimiento in vitro de microesquejes de café Var. Limaní en MS + reguladores de crecimiento, Dunn α=0,05. Nota. Las variables sin letra, indica que no existe diferencias significativas entre los tratamientos.
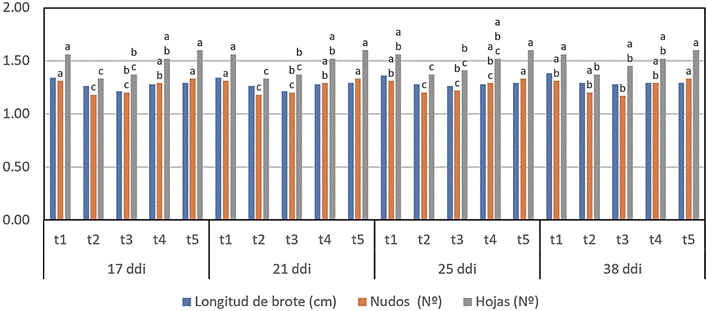
Figura 5. Formación de vástago en el establecimiento in vitro de microesquejes de café Var. Limaní en MS + reguladores de crecimiento, Duncan α=0,05. Nota. Las variables sin letra, indica que no existe diferencias significativas entre los tratamientos.
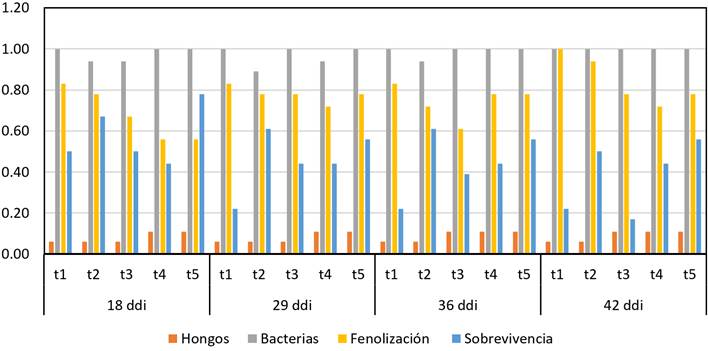
Figura 6. Variables de desinfección en el establecimiento in vitro de microesquejes de café Var. Limaní en SH + reguladores de crecimiento, Dunn α=0,05. Nota. Las variables sin letra, indica que no existe diferencias significativas entre los tratamientos.
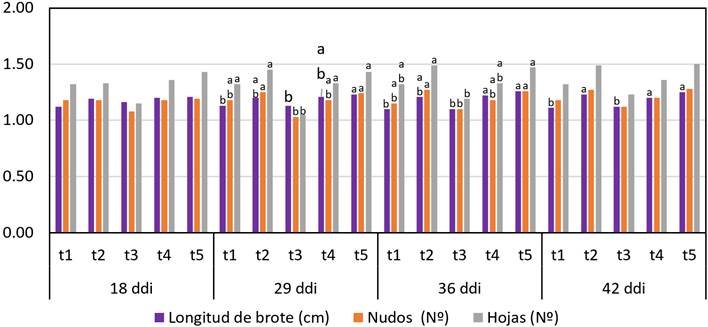
Figura 7. Formación de vástago en el establecimiento in vitro de microesquejes de café Var. Limaní en SH + reguladores de crecimiento, Duncan α=0,05. Nota. Las variables sin letra, indica que no existe diferencias significativas entre los tratamientos.
Varias especies vegetales de interés agronómico, ornamentales, en peligro de erosión genética, entre otras, se han logrado propagar in vitro; sin embargo, ha sido necesario establecer protocolos desde la elección del explante, componentes y reguladores de crecimiento adecuados en el medio nutritivo para la micropropagación respectiva; en café, el método de regeneración de plantas, se obtiene generalmente mediante la embriogénesis somática; sin embargo, es importante evaluar otro tipo de explantes , como los que se han utilizado en esta investigación, a partir de microesquejes. Vitroplantas de C. arabica de cuatro pares de hojas, se tomaron como explantes los brotes apicales de dos pares de hojas, y fueron sembradas en medios MS con reducción de 25% de sus componentes, en donde al 50%, se obtuvo el 85% de supervivencia de plántulas; y, con 4,5 hojas en promedio entre cuatro a seis meses de cultivo (Castilla-Valdés et al., 2020). En explantes de Tillandsia takizawae Ehlers & H. Luther, bromelia epífita, inoculados en medio MS la mayor cantidad de brotes (41,4) por explante fue con 1,0 mgL-1 de BA y 0,25 mgL-1 de ANA, la longitud de brotes se logró con la adición de 1,0 mgL-1 de AG3 (Hernández-Meneses et al., 2024). En Malus domestica, explantes in vitro, inoculados en medios de cultivo MS y WPM (woody plant medium) a diferentes concentraciones de BAP e IBA, presentaron la mayor cantidad (36) de brotes por explante a la dosis de 1,5 mgL-1 de BAP en ambos medios; sin embargo, se determinó que el medio de cultivo MS influye en el desarrollo vegetativo (Cabral-Miramontes et al., 2022).
El medio MS, es considerado importante en la micropropagación de diferentes especies vegetales de interés; en Rubus glaucus Benth. para su establecimiento resultó con el medio MS en combinación con 2,0 mgL-1 de ácido giberélico (Andrade et al., 2021); sin embargo, en Croton lechleri Mull. Arg. con propiedades terapéuticas, embriones cigóticos fueron inoculados en cuatro medios de cultivo, se determinó que, en WPM y QL sin carbón activado proporcionaron un desarrollo promedio superior al 90% (de Oliveira et al., 2020). En el establecimiento de Hibiscus moscheutos L. ‘Berry Awesome’ en MS + 0,1 mgL−1 N-(2-chloro-4-pyridinyl)- N’-phenylurea (CPPU), produjo una sobrevivencia 73,3% superior a MS + 0,1 mgL−1 de BAP con 67,2%, ambos a los 11 ddi (Sereda et al., 2024), En Panax ginseng Meyer, con 1/2 MS facilitó un buen desarrollo de los brotes en comparación al medio con 1/2 SH (Jung-Woo et al., 2023). En Polylepis rugulosa Bitter, se usaron 3 concentraciones de ANA y 5 concentraciones de BAP en medio MS, siendo el de mejor respuesta la combinación de 0,25 μM ANA + 2 μM BAP con 15,8 brotes, de 9 mm de tamaño y 2,7 hojas en promedio por explante y no presentaron formación de callo (Mollohuanca et al., 2021).
Por otro lado, el crecimiento de los explantes de plantas es afectado por la aplicación de reguladores de crecimiento, la contaminación y fenolización a consecuencia de exposición de los explantes a las sustancias y concentración de éstas (hipoclorito de sodio y de calcio). El BAP tiene un efecto directo sobre la generación de brotes, se sintetizan principalmente en raíces, ausente en los explantes utilizados en el establecimiento in vitro, por lo cual, es fundamental su adición en los medios de cultivo (Hoyos et al., 2008). A partir de brotes axilares de café, utilizando diferentes concentraciones de BAP se determinó que hasta 5,0 mgL-1 se obtuvo el mayor número de brotes (4,0); pero, se reduce la longitud del mismo (Suliansyah et al., 2021). Cuando se utilizaron medio SH con 4 y 8 mgL-1 de BAP en combinación con 8,0 mgL-1 de kinetina, la reactivación de ápices de C. arabica Var. Catuai, fue de un 100%; asimismo, valores de BAP superiores a este valor (8,0 mgL-1) tiende a disminuir el número de hojas (González et al., 1998). En la inducción de microesquejes de C. arabica, cv ‘Benan’ explantes de plántulas in vitro, de 0,5 cm de altura, en MS basal, produjo un brote y una altura de 2,0 cm, a los 90 ddi, inferior a cuando se añade BAP al MS; enfatizando, que la mejor respuesta obtenida con mayor número de nudos y hojas en los explantes de café Var. Limani, fue a los 25 ddi en MS + 0,5 mgL-1 de BAP; y, a los 29 ddi en SH + ANA (0,2 mgL-1) + BAP (2,25 mgL-1) y en SH + BAP (0,5 mgL-1). También se determinaron que los medios de cultivo para diferentes cultivares son específicos cuando regeneraron explantes de diferentes cultivares (AL-Azab et al., 2015). Por lo expuesto, se puede mencionar que la respuesta bajo condiciones in vitro es diversa, varía dependiendo de la especie, explante, variedad o el genotipo que se utilice. Vale decir que, en Uncaria gambier, de alto valor económico, en microesquejes de tercer nudo, la adición de 2,0 mgL-1 de BAP influye en la formación de los brotes y con 6,0 mgL-1 de BAP para aumentar el número de hojas y brotes (Zainal et al., 2023); y, en la regeneración in vitro a partir de puntas de brote de Lycium barbarum L, con propiedades nutracéuticas, se obtuvo el mayor número de brotes (4,33) con 2,0 mgL-1 de BAP + 0,25 mgL-1 IBA en comparación a los explantes de hoja y segmentos nodales (Ucar et al., 2024). Por otro lado, en C. arabica, el hipoclorito de sodio es utilizado como desinfectante; en algunos explantes a partir de meristemas y órganos son muy susceptibles a la oxidación biológica, sin embargo, con hipoclorito de calcio y meta bisulfito de sodio como antioxidante, resultó muy efectivo para el control respectivo (Suescún et al., 2020); el tratamiento que presentó los mejores resultados en la desinfección de los explantes fue el 20% de cloro (NaClO) activo durante 20 min, con un 98 y 92% de explantes sanos en las variedades Caturra y SL-28, respectivamente (Montes-Cruz et al., 2017). En segmentos nodales de Salix babylonica L., con una doble desinfección con NaClO (1,0%) y HgCl2 (0,1%) por 20 y 10 min, respectivamente, instaladas en medio MS, se obtuvo el 71% de desinfección y la mejor respuesta en establecimiento (31,6%) se logró con la adición de BAP (2,0 mgL-1) (Silva et al., 2020). Sin embargo, en la presente investigación se encontró que solo a los 38 ddi en medio MS sin regulador, hubo una respuesta inferior en fenolización con respecto a los medios con ANA y BAP.
CONCLUSIONES
El café C. arabica Var. Limaní es resistente a roya H. vastatrix. El establecimiento in vitro es una fase crítica en la micropropagación, donde a partir de microesquejes obtenidos de campo, se logró establecer en los medios MS y SH, con 0,5 mgL-1de BAP, para continuar con las fases de multiplicación y enraizamiento.
Se recomienda realizar investigaciones en otras variedades de café, con estos mismos medios basales con la adición de BAP.
AGRADECIMIENTOS
Al Instituto Central de Investigación de la Universidad Nacional Daniel Alcides Carrión, por el financiamiento del proyecto “Desarrollo de protocolos en la propagación in vitro de Orquídeas y cultivos de importancia económica para la provincia de Oxapampa”, a través del cual se realizó el presente trabajo como parte de sus objetivos.
A la Bach. Odalyz L. Zúñiga Salcedo e Ing. Mayra Y. Monago Curi por el soporte técnico brindado.
REFERENCIAS BIBLIOGRÁFICAS
AL-Azab, A., Habib, S., Hussein, M., & El-Sherif, F. (2015). Micropropagation of Four Coffee Cultivars (Coffea arabica L.) from Yemen through Shoot Tip Culture. Hortscience Journal of Suez Canal University, 4(1), 25–31. https://doi.org/10.21608/hjsc.2015.6472
Alcantara, J., Acero, J., Alcántara, J., & Sánchez, R. (2019). Principales reguladores hormonales y sus interacciones en el crecimiento vegetal. NOVA, 17(32), 109–129.
Álvarez, J. C., Beltran, D. M., & Mesa, N. (2011). Evaluación de reguladores de crecimiento vegetal en la organogénesis de Gmelina arborea roxb. Tumbaga, 1(6), 107–124.
Andrade, A., Gómez, L., Torres, Y., & Aguilera-Arango, G. (2021). Evaluación de medios de cultivo para el establecimiento, multiplicación y enraizamiento in vitro de mora (Rubus glaucus Benth.). Chilean Journal of Agricultural and Animal Sciences, Ex Agro-Ciencia, 37(2), 117–127. https://doi.org/10.29393/CHJAAS37-14EMAG40014
Ardiyani, F., Setiti Wida Utami, E., & Purnobasuki, H. (2021). Optimation of Auxin and Cytokinin on Enhanced Quality and Weight of Coffea liberica Somatic Embryos. Pelita Perkebunan (a Coffee and Cocoa Research Journal), 37(1). https://doi.org/10.22302/iccri.jur.pelitaperkebunan.v37i1.460
Arimarsetiowati, R., Putra, A. C. D. S., Suwastono, M. R., Umami, L. A., Daryono, B. S., Astuti, Y. T. M., & Semiarti, E. (2023). The effect of 2,4-D, thidiazuron and BAP on calli induction of arabica coffee (Coffea arabica L.). IOP Conference Series: Earth and Environmental Science, 1133(1). https://doi.org/10.1088/1755-1315/1133/1/012010
Avila-Victor, C. M., Ordaz-Chaparro, V. M., Arjona-Suárez, E. de J., Iracheta-Donjuan, L., Gómez-Merino, F. C., & Robledo-Paz, A. (2023). In vitro mass propagation of coffee plants (Coffea arabica L. var. Colombia) through indirect somatic embryogenesis. Plants, 12(1237). https://doi.org/10.3390/plants12061237
Baek, S. C., Jeon, S. Y., Choi, Y. J., Byun, B. H., Kim, D. H., Yu, G. R., Kim, H., & Lim, D. W. (2024). Establishment of an In Vitro Micropropagation System for Cannabis sativa ‘Cheungsam.’ Horticulturae, 10, 1–14. https://doi.org/10.3390/horticulturae10101060
Beyl, C. A. (2000). Getting started with tissue culture - Media prepraration, sterile technique, and laboratory equipment. In Plant Tissue Culture Concepts and Laboratory Exercises (pp. 21–38). CRC Press.
Cabral-Miramontes, J. P., Chávez-Simental, J. A., Pulido-Diaz, C., González-Telles, J. R., Goche-Télles, J. R., & Barragán-Hernández, V. M. (2022). Propagación in vitro de manzano a partir de embriones eigóticos maduros. Rev. Mex. Cienc. Agríc., 13(4), 603.
Cabrera, R. M., Sánchez, K. J., & Guzmán, L. L. (2022). Regeneración de plántulas de café embriogénesis somática. Ministerio de Desarrollo Agrario y Riego.
Calderón, H. O., & Montes, M. E. (2024). Respuesta de veinte variedades de café (Coffea spp.) a la reproducción vía embriogénesis somática. Producción Agropecuaria y Desarrollo Sostenible, 13.
Canet, G., Soto, C., Ocampo, P., Rivera, J., Navarro, A., Guatemala, G., & Villanueva, S. (2016). La Situación y tendencias de la producción de café en América Latina y el Caribe. IICA.
Cardoso, J. C., Sheng, L. T., & Teixeira, J. A. (2018). Micropropagation in the Twenty-First Century. In Plant Cell Culture Protocols, Methods in Molecular Biology (Vol. 1815, pp. 17–46). Springer Nature. https://doi.org/10.1007/978-1-4939-8594-4_2
Castilla-Valdés, Y., González-Vega, M. E., & Espinosa-Torres, L. (2020). Conservación in vitro de cafeto (Coffea arabica L.) mediante la disminución de sales minerales en el medio de cultivo. Cultivos Tropicale, 41(1), 1–13.
de Oliveira, J. B., Pedroza, C. M., da Silva, H., da Silva, F. H., & Scherwinski, onny E. (2020). Protocol for development of zygotic embryos in vitro and acclimatization of Dragon’s Blood plantlets. Research, Society and Development, 9(9), 1–13. https://doi.org/10.33448/rsd-v9i9.7031
Dinh, T. X., Nguyen, M. L., Vu, D. D., & Hoang, G. T. (2021). High efficient micropropagation of Panax vietnamensis Ha et Grushv. From immature zygotic embryos. Sel’skokhozyaistvennaya Biologiya, 56(5), 924–933. https://doi.org/10.15389/AGROBIOLOGY.2021.5.924ENG
Etienne, H., Breton, D., Breitler, J.-C., Bertrand, B. B., Déchamp, E., Awada, R., Marraccini, P., Léran, S., Alpizar, E., Campa, C., Courtel, P., Georget, F. F., & Ducos, J.-P. (2018). Coffee somatic embryogenesis: how did research, experience gained and innovations promote the commercial propagation of elite clones from the two cultivated species? Frontiers in Plant Science, 9(1), 1–21. https://doi.org/10.3389/fpls.2018.01630
Fazuoli, L. C., Perez, M., Guerreiro, O., Medina, H., & Silvarolla, M. B. (2000). Breeding and biotechnology of coffe. In T. Sera, C. R. Soccol, A. Pandey, & S. Roussoos (Eds.), Coffee Biotechnology and Quality (pp. 27–45).
Fu, Y., Liang, X., Zhang, H., Cheng, S., Li, A., Liao, M., Tan, L., Yang, L., & Qi, X. (2024). Establishment of an efficient regeneration system and in vitro polyploid induction based on the bulblet centre in Lilium rosthornii Diels. In Vitro Cellular and Developmental Biology - Plant, 60(4), 508–522. https://doi.org/10.1007/s11627-024-10438-9
Gebremariam, E. (2017). In vitro propagation of Coffea arabica cv. MCH2 Using Nodal Explants. Journal of Natural Sciences Research, 7(1), 17–21.
González, M., Morejón, R., & Portilla, M. (1998). Establecimiento de las concentraciones óptimas de hormonas para el cultivo In Vitro de ápices de Coffea arabica L. Cultivos Tropicales, 19(2), 37–40.
Górecki, M., & Hallmann, E. (2020). The antioxidant content of coffee and its in vitro activity as an effect of its production method and roasting and brewing time. Antioxidants, 9(308), 1–10. https://doi.org/10.3390/antiox9040308
Gutierrez-Rosati, A., & Gonzales, P. (2019). Reguladores de crecimiento en el cultivo in vitro de tres cultivares portainjertos de vid (Vitis vinifera) para su uso en la industria del pisco. Scientia Agropecuaria, 10(4), 461–468. https://doi.org/10.17268/sci.agropecu.2019.04.02
Hernández, Y., & González, M. E. (2010). Efectos de la contaminación microbiana y oxidación fenólica en el establecimiento in vitro de frutales peremnes. Cultivos Tropicales, 31(4), 58–69.
Hernández-Meneses, E., Rangel-Estrada, S. E., Canul-Ku, J., & Barrios-Gómez, E. J. (2024). Regeneración in vitro de Tillandsia takizawae Ehlers & H. Luther}. Polibotánica, 0(57). https://doi.org/10.18387/polibotanica.57.10
Hoyos, J. L., Perea, C., & Velasco, R. (2008). Evaluación del efecto de diferentes concentraciones de fitohormonas en la micropropagación del plátano dominico (Musa AAB Simmonds). Facultad de Ciencias Agropecuarias, 6(2), 100–104.
Indacochea, B., Parrales, J., Hernández, A., Castro, C., Vera, M., Zhindón, A., & Gabriel, J. (2018). Evaluación de medios de cultivo in vitro para especies forestales nativas en peligro de extinción en Ecuador. Agronomía Costarricense, 42(1), 63–89. https://doi.org/10.15517/rac.v42i1.32203
Jung-Woo, L., Jang-Uk. Kim, Kyong-Hwan, B., Kwon, N., Young-Chang, K., Ick-Hyun, J., & Young-Doo, P. (2023). Efficient Somatic Embryogenesis, Regeneration and Acclimatization of Panax ginseng Meyer: True-to-Type Conformity of Plantlets as Confirmed by ISSR Analysis. Plants, 12(1). https://doi.org/10.3390/plants12061270
Kim, H. J., Yun, C. M., Lee, S., Gu, H. S., Kim, Y. H., Kim, J. H., Kim, K. K., Kim, S. B., Lee, K. M., Hong, C. O., Son, H. J., Park, H. C., & Kim, Y. J. (2025). Establishment of in vitro cell culture and caffeine production from coffee (Coffea arabica L.). Journal of Applied Biological Chemistry, 68(1), 24–30. https://doi.org/10.3839/jabc.2025.004
Krishnan, S. (2011). Coffee biotechnology: Implications for crop improvement and germplasm conservation. Acta Horticulturae, 894, 33–44. https://doi.org/10.17660/ActaHortic.2011.894.2
Kumar, V., Madhava, M., & Ravishankar, G. A. (2006). Developments in coffee biotechnology - In vitro plant propagation and crop improvement. Plant Cell, Tissue and Organ Culture, 87(1), 49–65. https://doi.org/10.1007/s11240-006-9134-y
Mamata, K., & Anuj, L. (2021). Advances In Agricultural Biotechnology. Nepal Journal of Biotechnology, 9(1), 85–92. https://doi.org/10.3126/njb.v9i1.38643
Melese, K. (2016). The Role of Biotechnology on Coffee Plant Propagation: A Current topics paper. Journal of Biology, Agriculture and Healthcare, 6(5), 13–19.
Mollohuanca, C., Mayta, L., & Bardales, R. (2021). Growth Regulators (BAP and ANA) for in vitro Propagation of Queñoa (Polylepis rugulosa Bitter). Manglar, 18(2), 207–213. https://doi.org/10.17268/manglar.2021.028
Montes-Cruz, S., Lalama-Aguirre, J. M., Echeverría-Félix, J. M., Toromoreno-Arévalo, L., Salazar-Torres V, S. M., Benavides-Burgos, E. S., & Atiaja-Llamba, J. A. (2017). Obtención de embriones somáticos de cafeto a partir de explantes de hojas de las variedades de Bourbón, Caturra Rojo y SL-28 de plantaciones establecidas en la Provincia del Carchi, Zona 1, Ecuador. Revista Científica Dominio de las Ciencias, 3(2), 918–942. https://doi.org/10.23857/dom.cien.pocaip.2017.3.2.918-942
Moreno-Peña, L., Hidalgo-Escobar, K., Cevallos-Cevallos, J. M., & Sanchez-Timm, E. (2025). An effective disinfection protocol for contamination control in vitro establishment of Mortiño (Vaccinium floribundum Kunth) and identification of endogenous microbes. Scientia Agropecuaria, 16(3), 375–384. https://doi.org/10.17268/sci.agropecu.2025.028
Mroginski, L. A., & Roca, W. M. (1991). Establecimiento de cultivos de tejidos vegetales in vitro. In Cultivo de tejidos en la agricultura: Fundamentos y aplicaciones. (pp. 17–40).
Mroginski, L., Sansberro, P., & Flaschland, E. (2010). Establecimiento de cultivos de tejidos vegetales. In G. Levitus, V. Echenique, C. Rubinstein, E. Hopp, & L. Mroginski (Eds.), Biotecnología y Mejoramiento Vegetal II (pp. 17–25).
Muzykiewicz-Szymańska, A., Nowak, A., Wira, D., & Klimowicz, A. (2021). The Effect of Brewing Process Parameters on Antioxidant Activity and Caffeine Content in Infusions of Roasted and Unroasted Arabica Coffee Beans Originated from Different Countries. Molecules (Basel, Switzerland), 26(12), 1–20. https://doi.org/10.3390/molecules26123681
Quiñones, M., Yafac, N., Garavito-Salini, R., & Principe, L. (2020). Desdiferenciación celular in vitro de Coffea arabica L. “cafè” Var. Caturra a partir de explantes foliares. Scientia, 22(22), 141–148.
Rodríguez, R. del P., González, W., & Bosques, O. (2020). Identificación de líneas interespecíficas de cafetos con resistencia a Hemileia vastatrix Berk. et Br. y adaptabilidad a la región de Puerto Rico. J. Agric. Univ. P.R., 104(2), 165–180. https://doi.org/10.46429/jaupr.v104i2.19040
Sereda, M., Petrenko, V., Kapralova, O., Chokheli, V., Varduni, T., Dmitriev, P., Minkina, T., Sushkova, S., Barbashev, A., Dudnikova, T., Singh, R., Seth, C., & Rajput, V. (2024). Establishment of an In vitro Micropropagation Protocol for Hibiscus moscheutos L. ‘Berry Awesome.’ Horticulturae, 10(21), 1–12. https://doi.org/10.3390/horticulturae10010021
Silva, J. J., Pérez, R., Fonseca, Y., & Rodríguez, S. (2020). Propagación in vitro de Salix babylonica L. a partir de segmentos nodales. Revista Cubana de Ciencias Forestales, 8(3), 410–424.
Steel, R., & Torrie, J. (1985). Bioestadistica: Principios y Procedimientos (2da Ed.). ((2da ed.)). McGraw-Hill Inc. https://n9.cl/a1zt4
Suárez-Padrón, I. E. (2020). Cultivo de tejidos vegetales. Fondo Editorial Universidad de Córdoba.
Suescún, L., Herrera, J. C., & Acuña-Zornosa, J. R. (2020). Estudio de los factores limitantes para la obtención de plantas haploides de Coffea arabica. Cenicafé, 71(1), 32–47. https://doi.org/10.38141/10778/1118
Suliansyah, I., Yusniwati, Resigia, E., Febjislami, S., Warnita, Amanda, C. P., & Rahimah, L. (2021). Multiplication of arabica “solok Rajo” coffee through bio cellular technology. IOP Conference Series: Earth and Environmental Science, 741(1), 1–8. https://doi.org/10.1088/1755-1315/741/1/012053
Tombion, L., Soto, M. S., Mori, M., Mira, A., & Facciuto, G. (2020). Propagación in vitro de Alstroemedia var. “Fiesta de 15 INTA” a partir del cultivo de meristemas de rizoma. Chilean Journal of Agricultural and Animal Sciences, 36(2), 110–116. https://doi.org/10.29393/CHJAAS36-8PL50008
Ucar, E., Karaköy, T., & Aasim, M. (2024). Optimizing benzylami-nopurine (BAP) and naphthalene acetic acid (NAA) concentration for in vitro micropropagation of Goji Berry (Lycium barbarum L.) using various optimizing tools. Pakistan Journal of Agricultural Sciences, 61(1), 85–91. https://doi.org/10.21162/PAKJAS/24.95
Zainal, A., Anwar, A., Gustian, Fitriawati, & Yunita, R. (2023). The effects of several concentrations of BAP and source of explants to gambier shoot induction (Uncaria gambier (Hunter) Roxb). IOP Conference Series: Earth and Environmental Science, 1160(1). https://doi.org/10.1088/1755-1315/1160/1/012021
Anexo 1
Prueba de Cochran y Dunn, α=0,05, en variables de desinfección en el establecimiento in vitro en MS + reguladores de crecimiento de microesquejes de café Var. Limaní
|
ddi |
Fuente |
Hongos |
Bacterias |
Fenolización |
Sobrevivencia |
|
Repeticiones |
18 |
18 |
18 |
18 |
|
|
gl |
4 |
4 |
4 |
4 |
|
|
Valor Q |
1,42 |
1,94 |
5,28 |
5,26 |
|
|
17 |
p value |
0,841 |
0,746 |
0,260 |
0,261 |
|
Tratamientos |
|
|
Promedios |
|
|
|
t1 |
0,67 |
0,72 |
0,33 |
0,94 |
|
|
t2 |
0,50 |
0,78 |
0,67 |
1,00 |
|
|
t3 |
0,56 |
0,83 |
0,56 |
0,78 |
|
|
t4 |
0,50 |
0,83 |
0,67 |
0,83 |
|
|
|
t5 |
0,50 |
0,67 |
0,50 |
0,89 |
|
Repeticiones |
18 |
18 |
18 |
18 |
|
|
gl |
4 |
4 |
4 |
4 |
|
|
Valor Q |
1,45 |
1,21 |
5,11 |
0,32 |
|
|
21 |
p value |
0,836 |
0,876 |
0,276 |
0,989 |
|
Tratamientos |
|
|
Promedios |
|
|
|
t1 |
0,67 |
0,72 |
0,33 |
0,33 |
|
|
t2 |
0,50 |
0,78 |
0,67 |
0,28 |
|
|
t3 |
0,56 |
0,83 |
0,56 |
0,33 |
|
|
t4 |
0,50 |
0,83 |
0,67 |
0,33 |
|
|
|
t5 |
0,50 |
0,72 |
0,56 |
0,28 |
|
Repeticiones |
18 |
18 |
18 |
18 |
|
|
gl |
4 |
4 |
4 |
4 |
|
|
Valor Q |
2,55 |
1,37 |
5,11 |
0,82 |
|
|
25 |
p value |
0,635 |
0,850 |
0,277 |
0,936 |
|
Tratamientos |
|
Promedios |
|
||
|
t1 |
0,72 |
0,72 |
0,33 |
0,33 |
|
|
t2 |
0,50 |
0,67 |
0,67 |
0,28 |
|
|
t3 |
0,56 |
0,83 |
0,56 |
0,33 |
|
|
t4 |
0,50 |
0,72 |
0,67 |
0,33 |
|
|
|
t5 |
0,50 |
0,78 |
0,56 |
0,22 |
|
Repeticiones |
18 |
18 |
18 |
18 |
|
|
gl |
4 |
4 |
4 |
4 |
|
|
Valor Q |
2,55 |
2,17 |
10,40 |
1,58 |
|
|
38 |
p value |
0,635 |
0,706 |
0,034* |
0,812 |
|
Tratamientos |
|
Promedios |
|
||
|
t1 |
0,72 |
0,83 |
0,33 b |
0,28 |
|
|
t2 |
0,50 |
0,78 |
0,83a |
0,28 |
|
|
t3 |
0,56 |
0,89 |
0,87a |
0,33 |
|
|
t4 |
0,50 |
0,94 |
0,72a |
0,33 |
|
|
|
t5 |
0,50 |
0,83 |
0,56a |
0,17 |
Nota. *: Existe diferencias significativas; Letras diferentes muestra que existe diferencias significativas.
Anexo 2
Cuadrados medios y comparación múltiple de Duncan (α = 0,05), en formación de vástago en establecimiento in vitro de microesquejes de café Var. Limaní, en MS + reguladores de crecimiento
|
Análisis de varianza (ANOVA) |
Prueba múltiple de Duncan |
||||||||
|
ddi |
Fuente de variación |
gl |
Longitud de brote |
Nudos |
Hojas |
Trat. |
Longitud de brote (cm) |
Nudos (Nº) |
Hojas (Nº) |
|
Bloques |
2 |
0,0067ns |
0,0034ns |
0,0101ns |
t1 |
1,34 |
1,31a |
1,56a |
|
|
Tratamiento |
4 |
0,0066ns |
0,0142* |
0,0416* |
t2 |
1,26 |
1,18 c |
1,33 c |
|
|
CV% |
8,226 |
4,035 |
5,829 |
t3 |
1,21 |
1,20 bc |
1,37 bc |
||
|
17 |
Promedio |
1,277 |
1,263 |
1,478 |
t4 |
1,28 |
1,29ab |
1,52ab |
|
|
Mínimo |
1,118 |
1,155 |
1,291 |
t5 |
1,29 |
1,33a |
1,60a |
||
|
Máximo |
|
1,489 |
1,414 |
1,732 |
|
|
|
|
|
|
Bloques |
2 |
0,0067ns |
0,0034ns |
0,0101ns |
t1 |
1,34 |
1,31a |
1,56a |
|
|
Tratamiento |
4 |
0,0066ns |
0,0142* |
0,0416* |
t2 |
1,26 |
1,18 c |
1,33 c |
|
|
CV% |
8,226 |
4,035 |
5,829 |
t3 |
1,21 |
1,20 bc |
1,37 bc |
||
|
21 |
Promedio |
1,277 |
1,263 |
1,478 |
t4 |
1,28 |
1,29ab |
1,52ab |
|
|
Mínimo |
1,118 |
1,155 |
1,291 |
t5 |
1,29 |
1,33a |
1,60a |
||
|
Máximo |
|
1,489 |
1,414 |
1,732 |
|
|
|
|
|
|
Bloques |
2 |
0,0054ns |
0,0019ns |
0,0053ns |
t1 |
1,36 |
1,31ab |
1,56ab |
|
|
Tratamiento |
4 |
0,0048ns |
0,0096ns |
0,0277ns |
t2 |
1,28 |
1,20 c |
1,37 c |
|
|
CV% |
7,884 |
3,992 |
5,734 |
t3 |
1,26 |
1,22 bc |
1,41 bc |
||
|
25 |
Promedio |
1,293 |
1,272 |
1,494 |
t4 |
1,28 |
1,29abc |
1,52abc |
|
|
Mínimo |
1,169 |
1,155 |
1,291 |
t5 |
1,29 |
1,33a |
1,60a |
||
|
Máximo |
|
1,494 |
1,414 |
1,732 |
|
|
|
|
|
|
Bloques |
2 |
0,0019ns |
0,0114ns |
0,0067ns |
t1 |
1,38 |
1,31ab |
1,56a |
|
|
Tratamiento |
4 |
0,0054ns |
0,0150ns |
0,0241ns |
t2 |
1,29 |
1,20ab |
1,37 b |
|
|
CV% |
8,461 |
6,146 |
5,983 |
t3 |
1,28 |
1,17 b |
1,45ab |
||
|
38 |
Promedio |
1,308 |
1,261 |
1,502 |
t4 |
1,29 |
1,29ab |
1,52ab |
|
|
Mínimo |
1,169 |
1,000 |
1,291 |
t5 |
1,29 |
1,33a |
1,60a |
||
|
Máximo |
|
1,511 |
1,414 |
1,732 |
|
|
|
|
|
Nota. *: diferencias significativas; ns: sin diferencias significativas; los promedios en columna, que no comparten la misma letra son significativamente diferentes. Trat.: tratamiento.
Anexo 3
Prueba de Cochran y Dunn, α=0,05, en variables de desinfección en el establecimiento in vitro en SH + reguladores de crecimiento de microesquejes de café Var. Limaní
|
ddi |
Fuente |
Hongos |
Bacterias |
Fenolización |
Sobrevivencia |
|
Repeticiones |
18 |
18 |
18 |
18 |
|
|
gl |
4 |
4 |
4 |
4 |
|
|
Valor Q |
1,09 |
3,00 |
5,47 |
5,60 |
|
|
18 |
p value |
0,896 |
0,558 |
0,242 |
0,231 |
|
Tratamientos |
|
|
Promedios |
|
|
|
t1 |
0,06 |
1,00 |
0,83 |
0,50 |
|
|
t2 |
0,06 |
0,94 |
0,78 |
0,67 |
|
|
t3 |
0,06 |
0,94 |
0,67 |
0,50 |
|
|
t4 |
0,11 |
1,00 |
0,56 |
0,44 |
|
|
|
t5 |
0,11 |
1,00 |
0,56 |
0,78 |
|
Repeticiones |
18 |
18 |
18 |
18 |
|
|
gl |
4 |
4 |
4 |
4 |
|
|
Valor Q |
1,09 |
5,33 |
0,714 |
6,26 |
|
|
29 |
p value |
0,896 |
0,255 |
0,950 |
0,180 |
|
Tratamientos |
|
|
Promedios |
|
|
|
t1 |
0,06 |
1,00 |
0,83 |
0,22 |
|
|
t2 |
0,06 |
0,89 |
0,78 |
0,61 |
|
|
t3 |
0,06 |
1,00 |
0,78 |
0,44 |
|
|
t4 |
0,11 |
0,94 |
0,72 |
0,44 |
|
|
|
t5 |
0,11 |
1,00 |
0,78 |
0,56 |
|
Repeticiones |
18 |
18 |
18 |
18 |
|
|
gl |
4 |
4 |
4 |
4 |
|
|
Valor Q |
0,92 |
4,00 |
2,97 |
6,25 |
|
|
36 |
p value |
0,921 |
0,406 |
0,563 |
0,181 |
|
Tratamientos |
|
Promedios |
|
||
|
t1 |
0,06 |
1,00 |
0,83 |
0,22 |
|
|
t2 |
0,06 |
0,94 |
0,72 |
0,61 |
|
|
t3 |
0,11 |
1,00 |
0,61 |
0,39 |
|
|
t4 |
0,11 |
1,00 |
0,78 |
0,44 |
|
|
|
t5 |
0,11 |
1,00 |
0,78 |
0,56 |
|
Repeticiones |
18 |
18 |
18 |
18 |
|
|
gl |
4 |
4 |
4 |
4 |
|
|
Valor Q |
0,92 |
0,92 |
7,23 |
8,82 |
|
|
42 |
p value |
0,921 |
0,921 |
0,124 |
0,066 |
|
Tratamientos |
|
Promedios |
|
||
|
t1 |
0,06 |
1,00 |
1,00 |
0,22 |
|
|
t2 |
0,06 |
1,00 |
0,94 |
0,50 |
|
|
t3 |
0,11 |
1,00 |
0,78 |
0,17 |
|
|
t4 |
0,11 |
1,00 |
0,72 |
0,44 |
|
|
|
t5 |
0,11 |
1,00 |
0,78 |
0,56 |
Nota. Promedios sin grupos (letras), no hay diferencias significativas.
Anexo 4
Cuadrados medios y comparación múltiple de Duncan (α = 0,05), en formación de vástago en establecimiento in vitro de microesquejes de café Var. Limaní, en SH + reguladores de crecimiento
|
Análisis de varianza (ANOVA) |
Prueba múltiple de Duncan |
||||||||
|
ddi |
Fuente de variación |
gl |
Longitud de brote |
Nudos |
Hojas |
Trat. |
Longitud de brote (cm) |
Nudos (Nº) |
Hojas (Nº) |
|
Bloques |
2 |
0,0205* |
0,0238ns |
0,1076* |
t1 |
1,12 |
1,18 |
1,32 |
|
|
Tratamientos |
4 |
0,0048ns |
0,0063ns |
0,0333ns |
t2 |
1,19 |
1,18 |
1,33 |
|
|
CV% |
4,845 |
9,124 |
11,474 |
t3 |
1,16 |
1,08 |
1,15 |
||
|
18 |
Promedio |
1,177 |
1,160 |
1,320 |
t4 |
1,20 |
1,18 |
1,36 |
|
|
Mínimo |
1,041 |
1,00 |
1,000 |
t5 |
1,21 |
1,19 |
1,43 |
||
|
|
Máximo |
|
1,285 |
1,414 |
1,732 |
|
|
|
|
|
Bloques |
2 |
0,0221** |
0,0244ns |
0,0776ns |
t1 |
1,13 b |
1,18ab |
1,32a |
|
|
Tratamientos |
4 |
0,0070ns |
0,0235ns |
0,0768* |
t2 |
1,20ab |
1,25a |
1,45a |
|
|
CV% |
3,646 |
6,827 |
10,483 |
t3 |
1,13 b |
1,03 b |
1,05 b |
||
|
29 |
Promedio |
1,181 |
1,173 |
1,318 |
t4 |
1,21ab |
1,18ab |
1,33a |
|
|
Mínimo |
1,049 |
1,000 |
1,000 |
t5 |
1,23a |
1,24a |
1,43a |
||
|
|
Máximo |
|
1,323 |
1,414 |
1,732 |
|
|
|
|
|
Bloques |
2 |
0,0279* |
0,0375* |
0,1325** |
t1 |
1,10 b |
1,15ab |
1,32ab |
|
|
Tratamientos |
4 |
0,0150* |
0,0155ns |
0,0454ns |
t2 |
1,21ab |
1,27a |
1,49a |
|
|
CV% |
4,844 |
5,583 |
8,951 |
t3 |
1,10 b |
1,10 b |
1,19 b |
||
|
36 |
Promedio |
1,180 |
1,192 |
1,361 |
t4 |
1,22a |
1,18ab |
1,33ab |
|
|
Mínimo |
1,033 |
1,000 |
1,000 |
t5 |
1,26a |
1,26a |
1,47a |
||
|
|
Máximo |
|
1,329 |
1,414 |
1,732 |
|
|
|
|
|
Bloques |
2 |
0,0333** |
0,0514* |
0,1615* |
t1 |
1,11 b |
1,18 |
1,32 |
|
|
Tratamientos |
4 |
0,0124** |
0,0130ns |
0,0402ns |
t2 |
1,23a |
1,27 |
1,49 |
|
|
CV% |
3,095 |
7,644 |
11,524 |
t3 |
1,12 b |
1,12 |
1,23 |
||
|
42 |
Promedio |
1,182 |
1,210 |
1,382 |
t4 |
1,20a |
1,20 |
1,36 |
|
|
Mínimo |
1,033 |
1,000 |
1,000 |
t5 |
1,25a |
1,28 |
1,50 |
||
|
|
Máximo |
|
1,348 |
1,472 |
1,826 |
|
|
|
|
Nota. **: diferencias altamente significativas *: diferencias significativas; ns: sin diferencias significativas; los promedios en columna, que no comparten la misma letra son significativamente diferentes. Trat.: tratamiento.